在电离辐射技术应用中,因违章作业所致的放射事故时有发生[1]。2016年11月15日,苏州大学附属第二医院收治1名放射损伤患者。该患者从事工业探伤操作3年,事发当天自行将辐射报警器置于关闭状态,致使其受到192Ir源照射。患者于受照后第21天入住苏州大学附属第二医院,住院治疗59 d,现将有关临床综合处理情况报道如下。
资料与方法1.一般资料:患者“任”,男,43岁,湖南省某工业探伤公司驻江苏某市办事处工作人员,从事工业探伤操作3年,接触192Ir源,工作期间定期接受辐射防护培训,有放射性工作上岗证。患者既往“血吸虫”病史30余年,否认其他慢性病、传染病及手术外伤史。
2.事故经过:2016年10月25日20 :30至凌晨3 :30工作期间,患者因意外操作进入操作间,进入房间时,探伤机已处于工作状态而受照。操作过程中,患者右手拿探伤机,右手拇指、食指、中指与机身接触,内装有192Ir放射源,每次接触时间为2~3 min,总共接触10余次,总接触时间约为2 h左右,当时放射源活度为8.14×1011 Bq(22 Ci),此后患者未再接触放射源。
3.剂量估算方法
(1) 生物剂量估算[2]:入院后立即抽取静脉血行外周血淋巴细胞染色体畸变分析,培养采用加秋水仙素法,淋巴细胞混合培养液(广州拜迪生物医药有限公司)含RPMI 1640、胎牛血清、植物血凝素(PHA)、双抗、秋水仙素。秋水仙素终浓度为0.04 μg/ml。每瓶5 ml混合培养液加0.5 ml肝素锂抗凝,37℃恒温箱培养48~50 h。使用HANABI PIII染色体收获系统(美国Transgenomic公司)制备细胞悬液,HANABI染色体分散仪(美国Transgenomic公司)滴片,姬姆萨染色。染色后使用Metafer 4(V 3.1 1.6)染色体扫描分析系统(德国MetaSystems公司),进行全玻片自动中期分裂相寻找及全玻片高倍图像采集。对采集的高倍数字图像借助Ikaros染色体核型分析软件(德国MetaSystems公司),选择染色体(46±1)条、长度适中、分散良好、很少重叠的中期分裂相,分析和记录“双着丝粒+环”(“dic+r”)畸变,根据外周血淋巴细胞染色体“dic+r”畸变情况估算患者全身生物剂量。
(2) 物理剂量估算[3]:基于东亚人体素体模和受照者主要生理特征,利用蒙特卡罗模拟软件包MCNP建立模型,采用体素体模(voxel phantom)和蒙特卡罗模拟相结合的方法来进行剂量估算,估算患者右手受照部位部位物理剂量。
4.医学检查:采用“一对一”和“多对一”的方法采集病史,详细记录和观察患者的临床症状和体征,开展血常规、生化功能、内分泌生殖系统、造血系统等实验室检查及影像学检查。
5.临床救治:患者入院后以全身治疗和局部治疗并重,全身治疗主要包括完善各系统检查及病情评估,给予抗感染、增强免疫功能、增加营养支持、补充维生素、改善微循环、心理疏导及其他对症支持治疗。局部治疗包括局部镇痛治疗、受照射皮肤维生素B12湿敷、减压引流、右手指清创术以及局部血管基质层细胞(SVF)、脂肪源性间充质干细胞(ADSCs)[4-5]注射。具体手术过程如下:①制备自体脂肪干细胞:于腹部共收集12 ml的脂肪,用1 ml的注射器进行分装,术区滚动式挤压出积血及游离的溶脂液,腹壁多层无菌加压包扎。收集的脂肪组织颗粒经过胶原酶或者胰酶消化、过滤、震荡离心后获得SVF,SVF通过直接离心法纯化后可获得ADSC。②脂肪干细胞植入术:在右手指清创部位注射分离后的SVF及ADSCs,共2 ml,皮下注射。再次冲洗右手指创面3遍,后敷以无菌敷料后加压包扎在位。术后常规予以创面换药、抗感染、营养神经、改善末梢循环等治疗。
6.心理测评[6]:采用卡特尔16种个性因素测验(16PF)、抑郁自评量表(SDS)、焦虑自评量表(SAS)对患者进行心理测评。
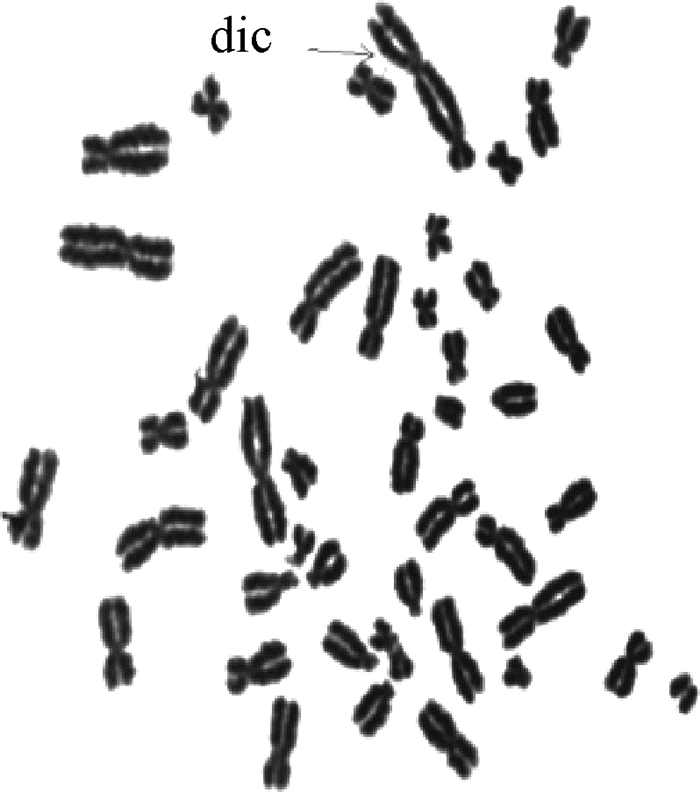
结果1.生物剂量估算:泊松分布检验结果显示,患者“dic+r”畸变偏离泊松分布,为过离散分布,属于局部不均匀照射。患者外周血染色体标本分析细胞数共2 655个,其中双着丝粒(dic)25个,着丝粒环(r)0个,染色体畸变率为0.938%。根据外周血淋巴细胞染色体畸变分析结果,患者相当于1次全身均匀受照0.43 Gy(95%CI:0.31~0.58 Gy)。考虑该患者入院时为受照后21 d,因此存在畸变自然衰减导致估算剂量偏低的可能。
|
图 1 患者外周血淋巴细胞染色体“dic+r”畸变 Figure 1 Chromosome "dic+r" aberration in peripheral blood lymphocytes of patients |
2.物理剂量估算:计算得出患者右手各手指拇指骨、拇指肌肉、拇指皮肤、食指骨、食指肌肉、食指皮肤、中指骨、中指肌肉、中指皮肤各部位物理剂量及手掌等效剂量估算结果分别为97.08、155.20、115.50、148.70、156.40、164.20、131.00、138.30、145.80和36.04 Gy。
3.诊断:结合患者的受照剂量、临床表现和辅助检查结果,诊断为192Ir过量外照射;右手食指急性放射性皮肤损伤Ⅲ度。
4.全身临床经过与治疗
(1) 临床症状:患者受照初期略感乏力,无发热、头晕、恶心、呕吐、腹痛、纳差、腹泻、脱发、失眠等症状。
(2) 实验室检查结果:患者入院后第1天完善血常规检查示:血红蛋白145 g/L,白细胞计数7.2×109/L,中性粒细胞数5.5×109/L,中性粒细胞比率76.9%,淋巴细胞数1.2×109/L,淋巴细胞比率16.4%,嗜酸性粒细胞数0.02×109/L,嗜酸性粒细胞比率0.3%,嗜碱性粒细胞数0.03×109/L,嗜碱性粒细胞比率0.4%,血小板计数114×109/L。血红蛋白数、白细胞数及中性粒细胞数、淋巴细胞数、嗜酸性粒细胞数、嗜碱性粒细胞数均在正常值范围内,中性粒细胞比率增高,血小板数、淋巴细胞比率、嗜酸性粒细胞比率较正常值降低。
入院后予每日复查血常规,自入院第2天复查示中性粒细胞比率恢复正常;血小板数逐渐降低,至入院第4天降至最低,为94 g/L,后复查血小板数逐渐恢复正常;血红蛋白自入院第2天出现降低,为128 g/L,入院第4天降至最低,为118 g/L,后复查血红蛋白恢复至正常水平;入院第2天及第3天复查血常规示嗜酸性粒细胞数及嗜酸性粒细胞比率进一步降低,均降为0,入院第4天及以后复查嗜酸性粒细胞数逐渐恢复至正常。至2017年1月12日复查血常规,各项指标均在正常范围内,见表 2。
|
|
表 2 患者住院期间血常规变化情况 Table 2 Changes in complete blood count during hospitalization |
患者入院第1天行生化功能检查示肝肾功能及电解质各项指标均正常;入院第15天复查生化功能提示球蛋白20.9 g/L、肌酸激酶34 U/L,较正常值偏低,丙氨酸氨基转移酶375 U/L,天门冬氨酸氨基转移酶74 U/L,γ谷氨酰转移酶143 U/L,较正常值偏高。入院第21天复查生化功能示球蛋白23.5 g/L,丙氨酸氨基转移酶432 U/L,天门冬氨酸氨基转移酶138 U/L,γ谷氨酰转移酶255 U/L、总胆汁酸11.05 μmol/L、总胆固醇6.00 mmol/L, 肝酶较前进一步升高。后予隔日复查肝功能,肝酶较前逐渐下降,至出院前最后一次复查生化功能提示球蛋白19.7 g/L较正常偏低,γ谷氨酰转移酶76 U/L较正常增高,余指标均恢复正常,见表 3。
|
|
表 3 患者住院期间血生化指标变化情况 Table 3 Changes in blood biochemical indicators during hospitalization |
患者入院第1天行甲状腺功能检查示反三碘甲状腺原氨酸(rT3)较正常升高,为1.03 ng/ml,余三碘甲状腺原氨酸(T3)、游离三碘甲状腺原氨酸(FT3)、甲状腺素(T4)、游离甲状腺素(FT4)、促甲状腺激素(TSH)、抗甲状腺球蛋白抗体(TGAb)、促甲状腺激素受体抗体(TRAb)、甲状腺球蛋白(HTg)各项指标结果均正常。2017年1月12日再次复查甲状腺功能,各项指标均在正常值范围内,见表 4。
|
|
表 4 患者住院期间甲状腺激素水平 Table 4 Thyroid hormone levels during hospitalization |
患者入院完善血清性激素检查,泌乳素水平较正常值偏低,为2.28 ng/ml,余雌二醇(E2)、孕酮(Pg)、睾酮(T)、促黄体生成素(LH)、促卵泡刺激素(FSH)等均在正常值范围内(表 5)。
|
|
表 5 患者住院期间血清性激素水平 Table 5 Serum sex hormone levels during hospitalization |
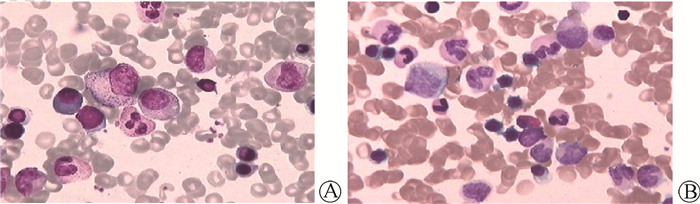
患者入院(2016年11月15日)行骨髓穿刺显示骨髓细胞形态正常,骨髓增生活跃,粒、红、巨3系细胞无明显异常;浆细胞比例增高,占6.0%。2017年1月13日再次行骨髓穿刺检查,提示骨髓增生活跃,粒红比例偏低(图 2)。
|
图 2 “任”骨髓穿刺骨髓细胞形态图A.2016年11月15日;B.2017年1月13日 Figure 2 Morphological chart of bone marrow cells by bone marrow puncture A.The first bone marrow puncture cell morphology after admission(2016-11-15); B.The second bone marrow puncture cell morphology after admission(2017-01-13) |
(3) 影像学检查结果:肝胆胰脾门静脉彩超检查,肝脏未见异常,胆囊、肝外胆管上段、肝内胆管、脾脏未见明显异常,门静脉彩色血流正常。X射线检查,未见明显骨质破坏征象,右手食指软组织肿胀。上肢血管造影,右手食指血管显影良好,未见明显狭窄、闭塞及造影剂外溢征象。磁共振(MRI):右前臂扫描范围内未见明显异常。右腕关节:①三角纤维软骨盘损伤。②少量积液。右手扫描显示指周围软组织弥漫性异常水肿,拇指、中指及环指周围软组织轻度水肿。
(4) 全身治疗情况:保持普通病房环境清洁,全身给予营养支持、改善微循环及增强免疫功能、保护肝功能等综合性治疗,患者血液系统、内分泌系统、消化系统各项指标均在出院前恢复至正常水平。
5.局部放射性皮肤损伤临床观察与治疗
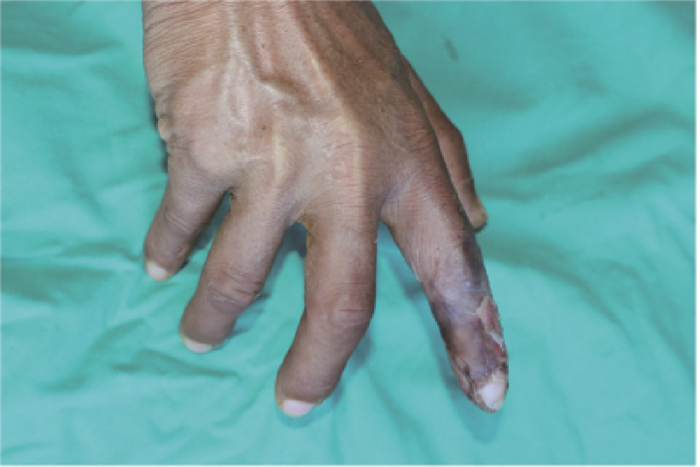
(1) 局部皮肤改变:受照后3 d感右手食指皮肤发红,轻度压痛,后红肿范围扩大,自行予风油精外涂后无好转;照后12 d右手食指出现水疱,右手拇指及中指出现红肿,伴有烧灼样疼痛及麻木感,手指活动度差,后水疱范围不断扩大,无渗液,无破溃。受照后21 d至本院就诊,右手食指远端指节及第2指节掌面、桡侧面及背面均被一直径约5 cm水疱覆盖,周边见红肿,无破溃渗液,右手拇指及中指可见红肿,部分皮肤可见色素沉着(图 3)。

|
图 3 患者受照射后右手局部表现A.患者右手食指皮肤色素沉着;B.受照射21 d患者右手食指出现水疱伴周围红肿 Figure 3 Local manifestations of the right hand after irradiation A.The patient′s right index finger skin pigmentation; B.The right index finger showed blisters with surrounding redness on the 21st day after exposure |
(2) 治疗:入院后予口服药物镇痛,局部创面维生素B12湿敷、减压引流、伤口规律换药治疗,后于2016年11月16日(受照后22 d)行右手指清创术+脂肪抽吸术+SVF注射手术。术后患者局部创面恢复良好,末梢血运可,感觉正常,出院时创面已基本愈合(图 4)。
|
图 4 患者受照75 d右手皮肤恢复情况 Figure 4 Skin recovery of right hand at 75 d after of exposure |
(3) 心理测评:16PF结果显示“任”具有良好的心理健康人的各因素,心理卫生测试在正常范围内。SDS评分总分为30分,标准分为37分;SAS评分总分为29分,标准分为36分。测评结果提示患者无明显焦虑、抑郁等表现,目前情绪状态较稳定,对自己的肢体功能恢复充满希望。
讨论放射损伤患者在受到急性外照射后,除表现全身不同程度的临床症状,以及各系统功能的损伤[7],常伴有局部放射性皮肤损伤,在全身综合治疗的基础上,局部皮肤放射损伤的治疗往往是救治的关键[1, 8-9]。
本例192 Ir源外照射致合并Ⅲ度急性放射性皮肤损伤患者,其全身临床症状较轻,诊断符合192Ir过量外照射;右手(拇、食、中、无名指)急性放射性皮肤损伤Ⅲ度。
患者受照射部位主要位于右手食指及拇指,表现为局部伤口疼痛、红肿、破溃及活动度改变。在开展临床综合救治的同时,治疗过程中着重进行了右手指局部皮肤损伤的治疗,给予局部伤口湿敷、清创换药、抗感染等处理,在入院后第2天(受照射后22 d)行右手指清创术+脂肪抽吸术+ SVF、ADSCs注射手术治疗,使局部伤口得到良好控制,避免伤口扩大、感染,改善了患者的整体愈后。经过积极治疗,患者于受照后40 d进入了恢复期,局部伤口愈合较慢,未遗留功能性损伤。
该例患者局部损伤救治中应用到局部SVF、ADSCs注射技术,SVF是脂肪组织经胶原酶消化后提取的细胞成分总和,包含ADSCs、血管内皮祖细胞、成纤维细胞及细胞外基质等许多其他具有促进血管生成作用的细胞[4, 10-12]。SVF可直接参与血管重建,通过SVF中已分解细胞成分的再循环利用和血管内皮细胞之间的动态重组,促使SVF快速形成血管网[13]。也可以通过ADSCs直接分化为血管内皮细胞、平滑肌细胞和周细胞调节血管生长、稳定、成熟[5]。
ADSCs属于成体干细胞的一种,具有自我更新、活力持久及多向分化潜能等特征,同时因其具有取材方便、来源充足、创伤小、体外培养方便及稳定生长和增殖、促进组织修复的能力,被认为是脂肪组织中具有干细胞特性的细胞群。一般情况下,大部分ADSCs处于静止阶段,只有少数细胞处于活跃的增长期,当机体出现炎症、创伤等应激因素时,ADSCs被激活,发挥修复重建的作用。
ADSC在脂肪移植后,可有效地分泌大量促血管生成因子和抗凋亡因子,如HGF、bFGF、VEGF、PDGF-B和TGF-β等[14-15],这些细胞因子与血管内皮细胞或相应细胞上的受体结合后,活化内皮祖细胞,诱导内皮细胞表达,抑制内皮细胞凋亡,能够分泌多种组织蛋白酶,降解细胞外基质,促进内皮细胞的增殖、迁移和新生血管的融合,发挥促血管生成效应[16-17]。创伤能够刺激成纤维细胞(FB)活化,ADSCs可通过影响FB来促进创面愈合和组织修复[18],通过增殖、迁移、合成和分泌细胞外基质等方式,参与肉芽组织及瘢痕形成和创面的重塑。将脂肪来源干细胞植入皮肤组织缺损处,诱导ADSCs的分化,修复组织创面,可以及时覆盖创面、减少创面收缩和瘢痕增生,为皮肤组织创面修复提供了简单、安全、有效的途径,在临床上有着广阔的应用前景。
近10年来,大量的研究证实,无论是新鲜分离的异质性的SVF,还是培养扩增后相对同质性的ADSCs,都具有自我更新与多向分化潜能。越来越多的动物实验研究及临床应用均证实了SVF和ADSCs在多种疾病治疗中的有效性[19-20],如在整形美容及创面修复、缺血性疾病、骨组织病、神经系统疾病和自身免疫性疾病治疗等领域[21-22]。此外,应用自体SVF细胞辅助脂肪移植,手术可一期完成,且无需体外培养,安全性高,更易于临床推广,这些研究结果均为脂肪来源干细胞的临床应用提供了证据支持。
核与辐射技术研究成果在国民经济各个领域的广泛应用,但与此同时,国内外核与辐射事故时有发生,自1990年以来,我国陆续发生了多起放射损伤事故,包括1990年上海“6.25”事故、1996年吉林“1.5”事故、1999年河南“4.26”事故、2004年山东济宁“10.21”事故、2014年南京“5.7”事故等[1, 7],放射损伤事故的案例较少、各具特点,能参考与借鉴的资料较少。近年来在对每起事故进行深入的总结归纳的基础上,在急性放射损伤救治方面已经取得较为成熟的救治经验。特别是南京“5.7”事故,在卫生应急、剂量估算、临床救治及新技术、新方法的采用方面,丰富了临床救治案例。核与辐射事故发生后,只有全面了解受照人员的临床表现,及早进行物理剂量和生物剂量估算,开展系统的医学观察和处理,才能制定出有效的诊断和救治方案。本例192 Ir源外照射致Ⅲ度急性放射性皮肤损伤患者在受照射后及时地进行了剂量估算,较为系统地开展了临床综合救治,重点进行了局部放射损伤的处理,控制了局部病灶的进展。根据患者病情采取局部重点处理联合全身综合救治措施,是本例患者救治成功的关键,它也为局部放射损伤救治提供了新的诊疗思路。
利益冲突 作者无利益冲突,排名无争议。作者的配偶、工作伙伴或子女不存在影响研究结果的财务关系作者贡献声明 侯雨含负责论文的设计及撰写;刘玉龙主持患者的临床救治工作,并在论文撰写过程中给予指导;王优优、卞华慧、陈炜博、戴宏、冯骏超、崔冉、王睿昊、杜云、王敏和姚振在患者住院期间均参与了临床诊断与救治工作
| [1] |
刘玉龙, 王优优, 余道江, 等. 南京"5.7"192Ir源放射事故患者的临床救治[J]. 中华放射医学与防护杂志, 2016, 36(5): 324-330. Liu YL, Wang YY, Yu DJ, et al. Medical management of the victim exposed to 192Ir source at "5.7" accident in Nanjing[J]. Chin J Radiol Med Prot, 2016, 36(5): 324-330. DOI:10.3760/cma.j.issn.0254-5098.2016.05.003 |
| [2] |
戴宏, 刘玉龙, 王优优, 等. 南京"5.7"192Ir放射事故患者三种生物剂量估算指标的衰变规律探讨[J]. 中华放射医学与防护杂志, 2016, 36(5): 355-358. Dai H, Liu YL, Wang YY, et al. Dynamic analysis on three indexes of biological dose estimation of the victim exposed to 192Ir radiation source at "5.7" accident in Nanjing[J]. Chin J Radiol Med Prot, 2016, 36(5): 355-358. DOI:10.3760/cma.j.issn.0254-5098.2016.05.009 |
| [3] |
孙亮, 刘玉龙, 郭凯琳, 等. 南京"5.7"192Ir源放射事故患者早期物理剂量估算[J]. 中华放射医学与防护杂志, 2016, 36(5): 340-344. Sun L, Liu YL, Guo KL, et al. Physical dose estimation for the patient in early stage of "5.7"192Ir source accident in Nanjing[J]. Chin J Radiol Med Prot, 2016, 36(5): 340-344. DOI:10.3760/cma.j.issn.0254-5098.2016.05.006 |
| [4] |
Bourin P, Bunnell BA, Casteilla L, et al. Stromal cells from the adipose tissue-derived stromal vascular fraction and culture expanded adipose tissue-derived stromal/stem cells:a joint statement of the International Federation for Adipose Therapeutics and Science (IFATS) and the International Society for Cellular Therapy (ISCT)[J]. Cytotherapy, 2013, 15(6): 641-648. DOI:10.1016/j.jcyt.2013.02.006 |
| [5] |
Gimble JM, Katz AJ, Bunnell BA. Adipose-derived stem cells for regenerative medicine[J]. Circ Res, 2007, 100(9): 1249-1260. DOI:10.1161/01.RES.0000265074.83288.09 |
| [6] |
陈炜博, 刘玉龙, 卞华慧, 等. 南京"5.7"192Ir源放射事故患者的神经行为及心理健康改变[J]. 中华放射医学与防护杂志, 2016, 36(5): 372-376. Chen WB, Liu YL, Bian HH, et al. Nervous behavior and mental health changes in a case exposed to 192Ir source at "5.7"accident in Nanjing[J]. Chin J Radiol Med Prot, 2016, 36(5): 372-376. DOI:10.3760/cma.j.issn.0254-5098.2016.05.013 |
| [7] |
卞华慧, 刘玉龙, 陈炜博, 等. 辐射事故中五例192Ir外照射人员的医学处理和随访[J]. 中华放射医学与防护杂志, 2015, 35(11): 862-864. Bian HH, Liu YL, Chen WB, et al. Medical treatment and follow-up of five 192Ir exposure personnel in radiation accidents[J]. Chin J Radiol Med Prot, 2015, 35(11): 862-864. DOI:10.3760/cma.j.issn.0254-5098.2015.11.015 |
| [8] |
余道江, 刘玉龙, 王优优, 等. 南京"5.7"事故受照者急性放射性皮肤损伤的修复[J]. 中华放射医学与防护杂志, 2016, 36(5): 368-371. Yu DJ, Liu YL, Wang YY, et al. Therepair of acute radiation skin injury from 192Ir source at "5.7" radiation accident in Nanjing[J]. Chin J Radiol Med Prot, 2016, 36(5): 368-371. DOI:10.3760/cma.j.issn.0254-5098.2016.05.012 |
| [9] |
郑旭, 刘玉龙, 王优优, 等. 南京"5.7"放射事故急性放射病患者局部损伤感染的防治[J]. 中华放射医学与防护杂志, 2016, 36(5): 359-363. Zheng X, Liu YL, Wang YY, et al. Prevention and treatment of a case with acute radiation sickness combined with severe local radiation injury infection at "5.7" accident in Nanjing[J]. Chin J Radiol Med Prot, 2016, 36(5): 359-363. DOI:10.3760/cma.j.issn.0254-5098.2016.05.010 |
| [10] |
Kilinc MO, Santidrian A, Minev I, et al. The ratio of ADSCs to HSC-progenitors in adipose tissue derived SVF may provide the key to predict the outcome of stem-cell therapy[J]. Clin Transl Med, 2018, 7(1): 5. DOI:10.1186/s40169-018-0183-8 |
| [11] |
Wolf DA, Beeson W, Rachel JD, et al. Mesothelial stem cells and stromal vascular fraction for skin rejuvenation[J]. Facial Plast Surg Clin North Am, 2018, 26(4): 513-532. DOI:10.1016/j.fsc.2018.06.011 |
| [12] |
Guo J, Nguyen A, Banyard DA, et al. Stromal vascular fraction:a regenerative reality? Part 2:Mechanisms of regenerative action[J]. J Plast Reconstr Aesthet Surg, 2016, 69(2): 180-188. DOI:10.1016/j.bjps.2015.10.014 |
| [13] |
Koh YJ, Koh BI, Kim H, et al. Stromal vascular fraction from adipose tissue forms profound vascular network through the dynamic reassembly of blood endothelial cells[J]. Arterioscler Thromb Vasc Biol, 2011, 31(5): 1141-1150. DOI:10.1161/ATVBAHA.110.218206 |
| [14] |
Kondo K, Shintani S, Shibata R, et al. Implantation of adipose-derived regenerative cells enhances ischemia-induced angiogenesis[J]. Arterioscler Thromb Vasc Biol, 2009, 29(1): 61-66. DOI:10.1161/ATVBAHA.108.166496 |
| [15] |
Kwon HM, Hur SM, Park KY, et al. Multiple paracrine factors secreted by mesenchymal stem cells contribute to angiogenesis[J]. Vascul Pharmacol, 2014, 63(1): 19-28. DOI:10.1016/j.vph.2014.06.004 |
| [16] |
Hao C, Shintani S, Shimizu Y, et al. Therapeutic angiogenesis by autologous adipose-derived regenerative cells:comparison with bone marrow mononuclear cells[J]. Am J Physiol Heart Circ Physiol, 2014, 307(6): 869-879. DOI:10.1152/ajpheart.00310.2014 |
| [17] |
Murohara T, Shintani S, Kondo K. Autologous adipose-derived regenerative cells for therapeutic angiogenesis[J]. Curr Pharm Des, 2009, 15(24): 2784-2790. DOI:10.2174/138161209788923796 |
| [18] |
Kim WS, Park BS, Sung JH, et al. Wound healing effect of adipose-derived stem cells:a critical role of secretory factors on human dermal fibroblasts[J]. J Dermatol Sci, 2007, 48(1): 15-24. DOI:10.1016/j.jdermsci.2007.05.018 |
| [19] |
van Dongen JA, Harmsen MC, van der Lei B, et al. Augmentation of dermal wound healing by adipose tissue-derived stromal cells (ASC)[J]. Bioengineering (Basel), 2018, 5(4): 1-13. DOI:10.3390/bioengineering5040091 |
| [20] |
Pallua N, Baroncini A, Alharbi Z, et al. Improvement of facial scar appearance and microcirculation by autologous lipofilling[J]. J Plast Reconstr Aesthet Surg, 2014, 67(8): 1033-1037. DOI:10.1016/j.bjps.2014.04.030 |
| [21] |
黄绮梨, 夏琼平, 肖薇, 等. 自体脂肪颞部多层次移植填充整形[J]. 实用医学杂志, 2013, 29(7): 1129-1130. Huang QL, Xia QP, Xiao W, et al. Transplant from body fat multi-level temporal filled shaping[J]. J Pract Med, 2013, 29(7): 1129-1130. DOI:10.3969/j.issn.1006-5725.2013.07.035 |
| [22] |
谭赵云, 雷岳崇, 冯有支, 等. 自体脂肪颗粒移植填充额颞部凹陷的临床效果[J]. 中华医学美学美容杂志, 2015, 21(1): 11-14. Tan ZY, Lei YC, Feng YZ, et al. Clinical effect of autologous fat grafting in the frontotemporal augmentation[J]. Chin J Med Aesth Cosmet, 2015, 21(1): 11-14. DOI:10.3760/cma.j.issn.1671-0290.2015.01.004 |
 2019, Vol. 39
2019, Vol. 39


