2. 230031 合肥, 中国科学院合肥物质科学研究院医学物理与技术中心医学物理与技术安徽省重点实验室;
3. 230031 合肥, 解放军第一○五医院肿瘤诊疗中心
2. Anhui Province Key Laboratory of Medical Physics and Technology, Center of Medical Physics and Technology, Hefei Insitutes of Physical Science, Chinese Academy of Sciences, Hefei 230031, China;
3. Radiotherapy Center, Chinese People's Liberation Army No. 105 Hospital, Hefei 230031, China
碳素纤维治疗床因其密度低,机械强度高,不含金属,可以更好地实现图像引导放射治疗等优点而得到广泛使用[1]。在碳素纤维治疗床应用于临床的初期,曾一度被认为其对于患者剂量分布的改变是可以忽略的[2]。近年来,不断有研究报道碳素纤维治疗床导致肿瘤靶区的欠剂量、剂量建成区的改变及患者近床侧皮肤剂量的增加[3-7]。国际辐射单位与测量委员会(ICRU)第24号报告中指出,恶性肿瘤原发灶剂量的准确性应好于±5%,否则有可能造成局部复发,达不到预期的治疗效果。本研究基于XiO计划系统来定量分析碳素纤维治疗床对剂量分布的影响,并试图在XiO计划系统中构建虚拟治疗床来模拟这种影响,以便临床医生和物理师可以更准确地评估患者的放疗计划,使患者接受更加准确的照射剂量。
材料与方法1.实验设备:瑞典Elekta公司Axesse医用直线加速器,配备80对多叶光栅(MLC),在等中心处的投影宽度5 mm,可以开展调强放疗和三维适形放疗, 6维碳素纤维治疗床采用德国Medical Intelligence公司iBEAM evo Couchtop床板,为三明治夹层结构,外层和内层分别由碳素纤维(carbon fiber,CF)和填充泡沫(foam core,FC)构成。采用瑞典Elekta公司XiO 4.80.03计划系统完成计划设计。德国PTW公司Octavius 4D圆柱形固体水旋转模体,配套OCTAVIUS® Detector 729二维矩阵电离室,共729个电离室,每个电离室有效探测面积5 mm × 5 mm,两个电离室中心间距10 mm,配合PTW公司VeriSoft 5.1剂量分析软件,可以开展三维剂量验证。采用荷兰Philips公司16排大孔径螺旋CT模拟定位机进行CT扫描。PTW公司30013型指型电离室测量模体中心的绝对剂量,有效测量体积0.6 cm3。
2.构建虚拟治疗床模型:用Philips公司16排大孔径螺旋CT扫描加速器治疗床的延长板(iBEAM evo Extension 650),将扫描图像传输至瑞典Elekta公司Focal 4.80.00医生工作站,分别勾画CF和FC的轮廓,并保存为床模型。用大孔径螺旋CT扫描10.5 cm厚的固体水模(RW3),指型电离室的有效测量点置于水模下5 cm深度处,将扫描图像传输至Focal医生工作站,勾画电离室的有效测量体积并定义为PTV,将床模型添加到CT图像中,调节床模型的位置,使固体水模恰位于床模型左右位置的正中,并使水模的底面恰好和床模型的上表面相重合。将CT图像传输至XiO计划系统,在100°~180°范围内,每间隔5°,以PTV中心为射野等中心设计一个10 cm × 10 cm射野,准直器0°,100 MU的单野计划,采用Superposition算法[8],分别记录等中心点的剂量计算值。在相同的条件下,在加速器上执行上述计划,得到实测值。计算值与实测值的偏差μ由式(1)表示,不断调整CF和FC的相对电子密度(relative electron density,RED)值,当偏差μ最小时,即认为得到了最优化的RED值[9]。
| $ \mu = \frac{{{D_{{\rm{cal}}}} - {D_{{\rm{mea}}}}}}{{{D_{{\rm{mea}}}}}} \times 100\% $ | (1) |
式中,Dcal为TPS的计算值,cGy;Dmea为指型电离室的测量值,cGy。
3.入组病例:选取符合临床剂量学要求的10例肺癌患者的静态调强放疗计划,所有计划均在XiO计划系统中设计,采用Superposition算法[8]、2 mm计算网格。其中,每例计划的后斜野(定义为100°~260°范围内射野)的剂量贡献均占靶区总剂量的65%以上,目的是以此来验证XiO计划系统通过构建虚拟治疗床来模拟真实治疗床剂量衰减的准确性。
4.检测并校准:测量前检测加速器的各项机械参数、剂量输出特性等,确保机器可以稳定、良好运行,然后按要求连接Octavius 4D验证系统,并进行校准。
(1) 绝对剂量校准:机架角和准直器均置0°,指型电离室的有效测量点置于固体水模5 cm深度处,调节源皮距(SSD)为95 cm,使电离室的有效测量点位于加速器等中心处,采用10 cm × 10 cm射野,出束3次,每次100 MU,记录电离室读数平均值。将二维矩阵电离室有效测量面置于固体水模5 cm深度处,相同测量条件下,记录中心电离室3次测量平均值。由上述两值,得到绝对剂量校准因子。
(2) 相对剂量校准:基于Octavius 4D模体的CT图像制定一个0°单野计划,10 cm × 10 cm射野,准直器0°,200 MU,模体中心定义为射野等中心,计算等中心点剂量值作为期望值,同时在加速器上执行该计划,得到测量值,比较两值,得到相对剂量校准因子。
5.剂量验证:将选取的10例患者计划以DICOM格式传输至MOSAIQ网络,在加速器上执行计划,并以Octavius 4D旋转模体实时采集并保存剂量数据。同时,将患者计划分别移植到Octavius 4D模体加入和未加入床模型的CT图像上,进行质量保证(QA)剂量计算,分别导出计算得到的剂量分布。在VeriSoft软件中,以3 mm/3%的标准进行γ剂量分析,γ≤1.0的点占有效测量点≥90.0%即为验证通过, 评估在剂量计算时考虑治疗床对计划验证通过率的改善。
6.统计学处理:数据以x±s表示。采用SPSS 19.0软件进行数据分析,对剂量计算包含床模型前后,射野等中心剂量计算值与电离室实测值偏差μ的差值和10例患者剂量验证γ通过率的差值分别进行Shapiro-Wilk正态性检验,P>0.20为资料服从正态分布。若服从正态分布,进行配对t检验,否则,进行Wilcoxon符号秩检验。P < 0.05为差异有统计学意义。
结果1.加入治疗床前后不同机架角度的剂量计算偏差:最优化的CF和FC的RED值分别为0.75和0.10 g/cm3。机架角100°~180°范围内,固体水模中电离室的测量值Dmea,计划系统的计算值Dcal,计算偏差μ列于表 1,不加床模型时的计算偏差μ即为治疗床的剂量衰减系数。由表 1可见,加入床模型前后μ值由(2.54±1.48)%减小至(-0.04±0.36)%,对前后μ值的差值行Shapiro-Wilk正态性检验,资料不满足正态分布(P < 0.20),再对前后的μ值行Wilcoxon符号秩检验,差异有统计学意义(Z=-3.621,P < 0.05)。在加和不加床模型的情况下,分别对Dcal与Dmea的差值进行Shapiro-Wilk正态性检验,资料均满足正态分布(P>0.20),再对Dcal与Dmea行配对t检验,不加床模型,差异有统计学意义(t=-8.749,P < 0.05);加入床模型,差异无统计学意义(P>0.05)。
|
|
表 1 TPS加入床模型前后计算值与测量值在不同机架角的偏差 Table 1 The deviation between the calculated value and the measured value with or without the treatment couch in TPS at different gantry angles |
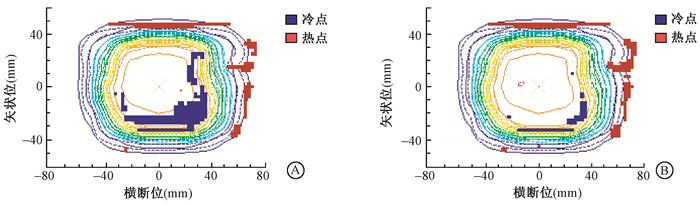
2.剂量计算考虑治疗床对计划通过率的改善:试验中选择的10例患者计划,在剂量计算加入床模型后,计划γ通过率由(91.79±1.25)%提高至(94.74±1.69)%,差异有统计学意义(t=6.027,P < 0.05,表 2)。选取10例患者中的1例,图 1显示了该例患者γ剂量分析中未通过的点(γ>1),容易看出冷点大部分分布于靶区内,热点大多分布于靶区外围的低剂量点,且冷点数目多于热点。加入床模型之后,容易看出靶区内的剂量冷点大大减少,靶区外围热点数目略微有所增加。这主要是由于未加入床模型时,剂量计算未考虑治疗床的剂量衰减,靶区剂量计算值相比患者实际接收的剂量较高,靶区剂量被高估,因此靶区内出现较多剂量冷点。本研究所用的二维矩阵电离室,分辨率较低(10 mm),在靶区外低剂量区较靶区内高剂量区存在更大的重建误差[10],结果显示,剂量计算考虑治疗床,靶区外未验证通过的低剂量点的通过率未见明显改善。对该例患者计划剂量分析全部有效测量点的γ值做量化统计,不加床模型时:γ≤1.0的点中,剂量热点和冷点分别占54.2%和36.0%,γ>1.0的点中,剂量热点和冷点分别占4.1%和5.7%;加入床模型后:γ≤1.0的点中,剂量热点和冷点分别占55.9%和38.1%,γ>1.0的点中,剂量热点和冷点分别占4.4%和占1.6%。总体来看,考虑治疗床,可以减少靶区内的剂量冷点,提高治疗计划验证通过率。
|
|
表 2 剂量计算考虑治疗床前后10例患者计划的三维剂量验证γ通过率(%) Table 2 Three-dimensional dose verification γ pass rate of the plans of 10 cases with or withoutthe treatment couch during the dose calculation(%) |
|
图 1 γ剂量分析未通过点分布图 A.不考虑治疗床;B.加入治疗床 Figure 1 Distribution of failed points in γ dose analysis A. Without the treatment couch; B. Inclusion of the treatment couch |
讨论
医用直线加速器治疗床目前多采用外层碳素纤维加内层泡沫相组合的结构,对于治疗床的剂量衰减国内外已有报道[11-15]。本研究在测量iBEAM evo Couchtop碳素纤维治疗床在不同机架角度对剂量衰减的基础上,在XiO计划系统中构建虚拟治疗床来模拟这种衰减,并通过实测临床病例评估了所构建的虚拟治疗床剂量计算的可靠性。
Vanetti等[12]基于Eclipse计划系统研究了治疗床对光子束的衰减,得出治疗床对6 MV光子束的衰减比10 MV光子束更明显,加入治疗床前后三维剂量验证通过率由(92.4±6.1)%提高到(94.9±2.6)%,本研究与上述结果相符合。Mihaylov等[13]基于Pinnacle计划系统研究了能模拟治疗床剂量衰减的最佳RED值,得出CF和FC最优化的RED值分别为0.70和0.10 g/cm3。本研究结果与之基本吻合。Yu等[14]基于Eclipse计划系统用不同算法模拟治疗床的剂量衰减,得出各向异性分析算法(anisotropic analytical algorithm,AAA)比笔形束卷积(pencil-beam convolution,PBC)算法模拟效果更好。Smith等[15]研究了iBEAM evo Couchtop的剂量衰减特性,发现随着后斜野机架角度的变化,治疗床对6 MV光子的衰减从2.7%到4.6%变化,且使用Superposition算法可以很好地模拟这种衰减,本研究的结果与其基本一致。
本研究选取的病例后斜野的剂量贡献均占靶区总剂量的65%以上,因此,在剂量计算未考虑治疗床的衰减时,计划通过率不高,剂量计算中考虑治疗床的衰减后,计划通过率均有所提高。本研究结果表明,不同的病例对计划通过率的改善程度却并不相同,推测这可能是不同病例射野和剂量分布不同,因此治疗床对剂量的衰减也不同而造成的。有关剂量计算,考虑治疗床对计划通过率的改善程度和治疗计划射野分布的关系可作为进一步的研究方向。此外,由于本研究所用的二维矩阵电离室的分辨率较低(10 mm),在靶区周边低剂量点的剂量重建误差较大,也是造成总体计划通过率不高的原因[10]。若采用更高分辨率的矩阵电离室,计划通过率或有改善,对此可做进一步研究。
综上所述,可见通过在XiO计划系统中构建虚拟治疗床模型来提高剂量计算的准确性,是合理、可行的,且是必要的,对临床医生和物理师更准确地评估患者的放疗计划及改善患者的治疗效果意义重大。
利益冲突 本研究全体作者无利益冲突,未因进行该研究而接受任何不正当的利益,在此对本研究的独立性和科学性予以保证作者贡献声明 郭红博负责完成实验,撰写并修改论文;李兵兵协助完成剂量验证相关实验;费振乐提出实验思路并对论文提出了修改意见;刘苓苓协助完成虚拟治疗床构建相关实验;王宏志负责病例选择并对论文提出了一些修改意见
| [1] |
Spezi E, Angelini AL, Romani F, et al. Evaluating the influence of the Siemens IGRT carbon fibre tabletop in head and neck IMRT[J]. Radiother Oncol, 2008, 89(1): 114-122. DOI:10.1016/j.radonc.2008.06.011 |
| [2] |
McCormack S, Diffey J, Morgan A. The effect of gantry angle on megavoltage photon beam attenuation by a carbon fiber couch insert[J]. Med Phys, 2005, 32(2): 483-487. DOI:10.1118/1.1852792 |
| [3] |
Aldosary G, Nobah A, Al-Zorkani F, et al. A practical method of modeling a treatment couch using cone-beam computed tomography for intensity-modulated radiation therapy and RapidArc treatment delivery[J]. Med Dosim, 2015, 40(4): 304-313. DOI:10.1016/j.meddos.2015.03.008 |
| [4] |
Gerig LH, Niedbala M, Nyiri BJ. Dose perturbations by two carbon fiber treatment couches and the ability of a commercial treatment planning system to predict these effects[J]. Med Phys, 2010, 37(1): 322-328. DOI:10.1118/1.3271364 |
| [5] |
Mihaylov IB, Bzdusek K, Kaus M. Carbon fiber couch effects on skin dose for volumetric modulated arcs[J]. Med Phys, 2011, 38(5): 2419-2423. DOI:10.1118/1.3576106 |
| [6] |
付庆国, 朱小东, 杨海明, 等. 加速器碳素纤维床对三维治疗计划剂量分布的影响[J]. 中华放射肿瘤学杂志, 2014, 23(6): 505-509. Fu QG, Zhu XD, Yang HM, et al. The effect of carbon fiber couch on dose distribution of conformal intensity modulated plan[J]. Chin J Radiat Oncol, 2014, 23(6): 505-509. DOI:10.3760/cma.j.issn.1004-4221.2014.06.012 |
| [7] |
Duggar WN, Nguyen A, Stanford J, et al. Modeling treatment couches in the Pinnacle treatment planning system:Especially important for arc therapy[J]. Med Dosim, 2016, 41(1): 34-41. DOI:10.1016/j.meddos.2015.07.001 |
| [8] |
Ulmer W, Pyyry J, Kaissl W. A 3D photon superposition/convolution algorithm and its foundation on results of Monte Carlo calculations[J]. Phys Med Biol, 2005, 50(8): 1767-1790. DOI:10.1088/0031-9155/50/8/010 |
| [9] |
Njeh CF, Parker J, Spurgin J, et al. A validation of carbon fiber imaging couch top modeling in two radiation therapy treatment planning systems:Philips Pinnacle3 and BrainLAB iPlan RT Dose[J]. Radiat Oncol, 2012, 7: 190. DOI:10.1186/1748-717X-7-190 |
| [10] |
Allgaier B, Schüle E, Würfel J. Dose reconstruction in the OCTAVIUS 4D phantom and in the patient without using dose information from the TPS[Z]. Freiburg, Germany:White paper PTW, 2013.
|
| [11] |
甘家应, 胡银祥, 罗元强, 等. Elekta Precise直线加速器新型全碳素纤维治疗床床板对放疗剂量的影响[J]. 中华放射医学与防护杂志, 2012, 32(4): 386-389. Gan JY, Hu YX, Luo YQ, et al. Effect of the new carbon fiber bed board of Elekta Precise linear accelerator on the radiation dose[J]. Chin J Radiol Med Prot, 2012, 32(4): 386-389. DOI:10.3760/cma.j.issn.0254-5098.2012.04.013 |
| [12] |
Vanetti E, Nicolini G, Clivio A, et al. The impact of treatment couch modelling on RapidArc[J]. Phys Med Biol, 2009, 54(9). DOI:10.1088/0031-9155/54/9/N03 |
| [13] |
Mihaylov IB, Corry P, Yan Y, et al. Modeling of carbon fiber couch attenuation properties with a commercial treatment planning system[J]. Med Phys, 2008, 35(11): 4982-4988. DOI:10.1118/1.2982135 |
| [14] |
Yu CY, Chou WT, Liao YJ, et al. Impact of radiation attenuation by a carbon fiber couch on patient dose verification[J]. Sci Rep, 2017, 7: 43336. DOI:10.1038/srep43336 |
| [15] |
Smith DW, Christophides D, Dean C, et al. Dosimetric characterization of the iBEAM evo carbon fiber couch for radiotherapy[J]. Med Phys, 2010, 37(7): 3595-3606. DOI:10.1118/1.3451114 |
 2018, Vol. 38
2018, Vol. 38


