2. 福建医科大学医学影像学院,福州 350122;
3. 清华大学工程物理系,北京 100084;
4. 福建省漳浦县医院放疗科,漳浦 363299
2. School of Medical Imaging, Fujian Medical University, Fuzhou 350122, China;
3. Department of Engineering Physics, Tsinghua University, Beijing 100084, China;
4. Department of Radiation Oncology, Zhangpu County Hospital, Zhangpu 363299, China
乳腺癌已成为全球最常见的癌症之一[1-2],我国女性乳腺癌的发病率和死亡率将持续上升[3]。乳腺癌的主要治疗方法包括手术、放射治疗、化疗和内分泌治疗等[4],放射治疗在乳腺癌综合治疗中具有重要地位。放射治疗过程中的摆位误差可能导致辐照剂量与预期不符,进而影响治疗效果和患者的生存率[5]。研究表明图像引导放疗可减小摆位误差,提高局部控制率,降低复发率,减少心脏损伤及放射性肺炎的发生率[6]。目前,医院现有放射治疗设备中常见的为二维kV-kV、三维锥形束计算机体层摄影(cone beam CT, CBCT)及光学图像引导验证模式等,各有优缺点[7-11]。
图像引导放疗的频率是确保放疗精确性的关键因素,指南通常推荐每周至少进行1次图像引导,以校正患者解剖位置的变化。然而,对于某些患者或特定类型的肿瘤,每天图像引导可能更为合适,尤其是在治疗过程中肿瘤位置或患者体态变化较大的情况下。因此,本研究探讨乳腺癌术后放疗不同正交图像引导频率下对摆位误差校正的影响情况,为实际临床工作中乳腺癌术后放疗患者提供正交图像引导频率参考建议。
资料与方法 1、资料收集本研究纳入福建医科大学附属协和医院放疗科2021年1月至2022年1月期间收治的80例乳腺肿瘤患者,左乳患者36例,右乳患者44例。患者年龄范围26~67岁,中位年龄47.5岁。入选标准为:①经病理证实的乳腺癌患者。②乳腺癌术后需接受调强放射治疗(intensity-modulated radiation therapy, IMRT)、放疗靶区剂量40 Gy/15次,且疗程内每分次均使用正交图像引导系统进行体位验证的患者。③双臂可上举并能充分暴露患侧乳房的患者。④KPS评分 > 80的患者。排除标准为:①患有其他影响放射治疗的疾病的患者。②手臂支撑困难且无法满足热塑膜定位的患者。③其他方面不适或无法完成整个研究过程的患者。研究获福建医科大学附属协和医院医学伦理委员会审批(审批号:2022QH018)。
2、体位固定、模拟定位及计划设计采用一体架联合或不联合热塑膜固定患者,采用荷兰Philips16排大孔径螺旋CT扫描,扫描层厚5 mm。使用美国瓦里安治疗计划系统(Eclipse V.15.6) 进行调强计划设计,射线能量为6 MV的X射线,计算网格为2.5 mm。
3、治疗实施及数据获取在治疗过程中,两名治疗师负责协同完成患者的摆位工作。治疗前,使用正交图像引导定位系统(第三方kV级二维图像引导系统),从45°和135°角度获取实时摆位图像,以进行体位验证。高年资的治疗师运用正交图像引导系统的软件,将捕获的图像与治疗计划中生成的同角度数字重建图像(digital reconstructed radiography, DRR)进行自动配准。若自动配准未能成功,便转而使用手动配准。配准以治疗靶区为中心设置配准框,同时参考胸壁、肋骨、胸椎及锁骨解剖位置为感兴趣区配准得出左右(x)、头脚(y)、腹背(z)方向的摆位误差进行记录。
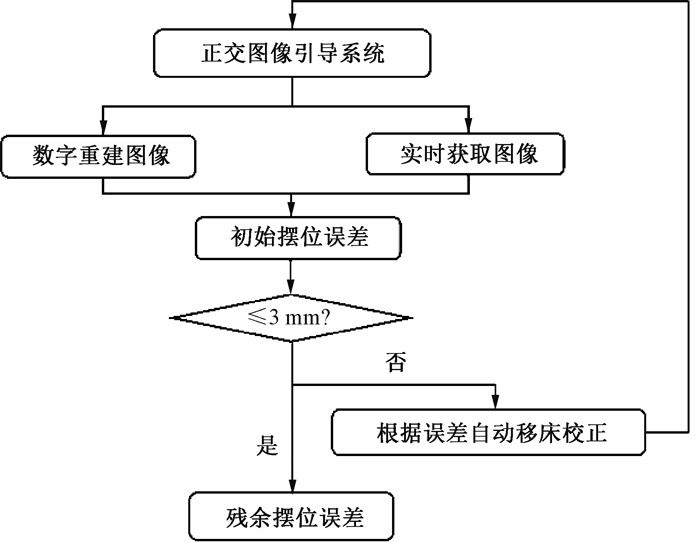
在每次图像引导验证中,首次获取的摆位误差定义为初始摆位误差,设定的误差容忍范围根据机构及参照指南标准为3 mm。若超过3 mm则利用图像引导系统校正软件自动移动治疗床进行校正,校正后再次获取实时图像并验证,直到误差均在误差范围内方可实施治疗。治疗前还存在的误差定义为残余误差,如图 1所示。若初始误差已经满足治疗要求,则无须校正,初始误差等于残余误差。
|
图 1 乳腺癌术后调强放疗患者初始误差及残余误差获取示意图 Figure 1 Schematic diagram showing the determination of initial error and residual set-up error |
4、数据分组
80例患者每例进行15次图像引导验证,即获取15组初始误差及残余误差,共1 200个,按不同频率提取数据分组,定义A、B、C、D、E、F组图像引导验证频率分别为每1、2、3、4、5 d和不校正,分别提取初始摆位误差和残余摆位误差组合为假定频率下实际摆位误差。
5、观测指标对比观测6组在x、y、z方向上的误差差异及分布情况。根据van Herk[12]推荐的计划靶体积(planning target volume, PTV)外放边界公式M=2.5Σ+0.7δ计算6组实际误差下PTV的外放边界,其中Σ为每个患者分次误差的平均值的标准差值,δ为每个患者分次误差的标准差的均方根。
6、统计学处理计量资料符合正态分布,应用SPSS 22.0软件,数据以x±s表示,计量资料的平均值进行配对样本t检验。P < 0.05为差异有统计学意义。
结果 1、平移误差差异分析统计分析得到A~F组乳腺癌患者在x、y、z 3个方向的摆位误差基本情况见表 1,结果表明每天进行图像引导校正的摆位误差最小,不校正的最大,在x方向表现最明显。并且随着间隔天数的增加,误差呈逐渐增加的趋势。
|
|
表 1 各组乳腺癌患者在x、y、z 3个方向的摆位误差(mm,x±s) Table 1 Set-up errors in the x, y, and z directions for breast cancer patients in various groups (mm, x±s) |
将A、B、C、D、E、F组不同摆位误差按x、y、z方向进行两两比较,结果得出,C组与D组在x方向和z方向、D组与E组在x方向和y方向差异无统计学意义(P > 0.05),其余组在x、y、z 3个方向上两两之间差异均具有统计学意义(t=-19.122~-2.127,P < 0.05)。
2、平移误差分布A~F组摆位误差在≤3 mm和 > 3 mm范围的分布情况如表 2所示。通过每天图像引导校正可以将摆位误差全部控制在3 mm以内,随着拍片间隔的增加,> 3 mm的摆位误差次数逐步增加,如果完全不进行图像引导校正,在x、y、z方向 > 3 mm的摆位误差分别为799、882、854次,占全部摆位误差的66.58%、73.50%、71.17%。随着引导频率的增加,能有效减少 > 3 mm的摆位误差占比。
|
|
表 2 各组乳腺癌患者不同方向初始摆位误差在不同误差范围的分布 Table 2 Distribution of initial set-up errors across different error ranges for breast cancer patients in various groups |
3、外放边界计算
以A~F组乳腺癌患者摆位误差的系统误差和随机误差计算x、y、z 3个方向的外放边界,结果表明计算出的PTV外放边界值在x、y、z 3个方向均呈现递增趋势。其中每天验证下摆位误差计算的PTV外放参考值由初始摆位误差(不校正)的6.60、6.29、4.22 mm降低到1.27、1.37、1.28 mm。其余每3、4、5 d验证频率之间相差不大,均在3~6 mm之间,最大差距表现在y方向,每3天和每5天校正相差0.81 mm。
讨论乳腺癌发病率不断升高,放射治疗扮演重要角色,不同图像引导技术对乳腺肿瘤靶区的分辨率、运动监测效果、摆位验证精确度及频率设置的相关问题一直是该领域的研究热点[13-15]。临床过程需根据患者的具体情况、肿瘤特性、治疗计划以及设备的性能特点,综合评估并选择最适宜的图像引导放射治疗(IGRT)技术或组合,并在使用频率间做出衡量,寻找最适合的图像引导频率,实现最佳临床治疗效果。
Peng等[16]在每日光学体表追踪联合不同周次频率的CBCT引导研究中,得出CBCT引导的频率越高,其误差越小,计算的PTV外放边界越小。本研究结果与此类似,通过对获取的摆位误差根据不同摄片频率分组进行统计分析,显示不同正交图像引导频率对乳腺癌术后放疗的摆位误差校正以及外放边界设置有较为显著的影响。随着图像引导频率的增加,尤其是每天进行图像引导校正,能有效减小摆位误差。但在间隔3 d以上,校正频率的改变对结果影响逐渐减小。研究进一步对6组摆位误差在不同误差范围的分布情况进行深入分析,观察到一个明显的趋势:从A组到F组,三维方向的摆位误差≤3 mm的次数和比例逐渐减少,而 > 3 mm的次数和比例则逐渐增加,A组未出现 > 3 mm的摆位误差,而F组在左右方向上 > 3 mm的摆位误差比例超过了30%。这一对比凸显了A组,即每天进行拍片的图像引导频率,在确保治疗精度方面的优势。因此,为了最大化治疗效果,建议采用A组的图像引导频率,即每天进行图像引导校正,以维持高水平的摆位精度。有研究报道利用正交图像引导系统能有效校正患者治疗过程中的摆位误差,如果能在每分次治疗中增加一次校正可明显减少分次内摆位误差,并获得更好的剂量学结果[6]。本研究具有相似的结论。
对于乳腺肿瘤,由于乳腺的特殊位置和形态,在治疗准备和执行过程中由于呼吸运动、几何形变、摆位误差等带来的位移误差更明显,容易导致乳腺癌靶区的剂量不足,影响剂量分布的准确性[17-20]。因此,为了确保处方剂量能够充分覆盖肿瘤靶区,需要在临床靶区周围设置适当的外放边界以形成PTV,选择合适的PTV外放边界对治疗实施至关重要[21]。本研究结果也提示每天图像引导频率下所计算的PTV外放边界最小,随着间隔时间的增加,需要更大的PTV外放边界来修正摆位误差带来的影响。有研究提示,乳腺癌临床靶体积(CTV)-PTV的边界取决于患者自身、放疗方式、验证频率等,一般需要5~10 mm的PTV外放边界[22-24]。值得注意的是,在Hoekstra等[25]的研究中,利用射波刀正交图像实时引导追踪,其外放边界根据单次治疗时间的长短,仅需要1~3 mm。结合本研究与现有研究结果,针对每天以及分次内增加一次图像引导验证频率的患者,PTV外放边界可适当缩小为3~5 mm。具体临床应用时,临床医生和物理师需结合各单位情况、特定的图像验证频率及其他因素,适当调整PTV外放边界,以提高放射治疗的准确性。
此外,本研究还存在进一步的探索空间,如获取的摆位误差是以靶区为中心设定配准框,通过自动配准(骨配准)或参考胸壁、肋骨、胸椎及锁骨解剖位置为感兴趣区手动配准得出。考虑到乳腺肿瘤靶区的位置和正交图像引导摄片对软组织的分辨能力,该方法所测量的误差可能存在一定偏差。针对该问题,本研究前期在体表铅点辅助正交图像引导系统在乳腺癌术后调强放疗的应用做了相应研究,结果表明,骨性配准和利用体表铅点为主的金标配准,在总体误差上具有一致性[26],同时也考虑到体表铅点在使用时会带来一定的误差,在选择时需结合临床进一步探究。此外,相比CBCT,kV级二维图像在图像质量方面还需进一步验证。随着新技术和新设备的发展,对于摆位误差的验证方式的选择,可考虑将正交图像引导方式结合光学体表引导或在每天正交图像引导过程中辅助每周进行CBCT引导,提高摆位误差获取及验证的准确性[27-28]。值得注意的是,正交图像引导在手动配准时,仅能获取到三维平移误差,对于旋转误差的分析还需进一步探索,在刘姝言等[29]研究中提到,三维和六维配准的结果差异具有统计学意义,建议使用六维配准方法对误差进行修正,而在Yamauchi等[30]研究中提出图像配准误差的得出通过金属标记配准应至少参考3张正交图像配准获得更具有准确性,这也是后续研究的一个重要方向。
综上所述,本研究证实了每天图像引导在乳腺癌放疗过程中的重要性和必要性。与其他校正频率相比,每天图像引导验证能够显著减少摆位误差和PTV外放边界,在选择图像引导摄片频率时,需综合考虑其正当性、最优化以及剂量限值,以期为患者和工作人员提供合理的参考依据。
利益冲突 无
作者贡献声明 董芳芬负责研究设计实施、数据分析及论文撰写;吴冰、王志新、黎嘉明负责收集临床数据、文献查找、论文修改;黄妙云负责计划审核;杨勇、徐本华负责临床靶区确认;李小波负责技术指导及论文修改
| [1] |
Sung H, Ferlay J, Siegel RL, et al. Global cancer statistics 2020: GLOBOCAN estimates of incidence and mortality worldwide for 36 cancers in 185 countries[J]. CA Cancer J Clin, 2021, 71(3): 209-249. DOI:10.3322/caac.21660 |
| [2] |
Arnold M, Morgan E, Rumgay H, et al. Current and future burden of breast cancer: Global statistics for 2020 and 2040[J]. Breast, 2022, 66: 15-23. DOI:10.1016/j.breast.2022.08.010 |
| [3] |
Lei S, Zheng R, Zhang S, et al. Breast cancer incidence and mortality in women in China: temporal trends and projections to 2030[J]. Cancer Biol Med, 2021, 18(3): 900-909. DOI:10.20892/j.issn.2095-3941.2020.0523 |
| [4] |
Chowaniec H, Ślubowska A, Mroczek M, et al. New hopes for the breast cancer treatment: perspectives on the oncolytic virus therapy[J]. Front Immunol, 2024, 15: 1375433. DOI:10.3389/fimmu.2024.1375433 |
| [5] |
王玮, 梅长文, 宫尚明, 等. 摆位误差对左乳癌术后放射治疗剂量分布的影响[J]. 安徽医学, 2024, 45(2): 168-173. Wang W, Mei CW, Gong SM, et al. The influence of setup errors on the dose distribution of postoperative radiotherapy for left breast cancer[J]. Anhui Med, 2024, 45(2): 168-173. DOI:10.3969/j.issn.1000-0399.2024.02.007 |
| [6] |
梁广立, 李岩, 徐翠玲, 等. 实时图像引导系统对乳腺癌保乳术后放疗摆位误差的影响[J]. 中国肿瘤临床, 2023, 50(03): 145-149. Liang GL, Li Y, Xu CL, et al. Impact of real-time image guidance system on setup errors in breast cancer radiother-apy after breast-conserving surgery[J]. Chin J Clin Oncol, 2023, 50(3): 145-149. DOI:10.12354/j.issn.1000-8179.2023.20221040 |
| [7] |
Duan YH, Gu HL, Yang XH, et al. Evaluation of IGRT-induced imaging doses and secondary cancer risk for SBRT early lung cancer patients in silico study[J]. Technol Cancer Res Treat, 2021, 20: 15330338211016472. DOI:10.1177/15330338211016472 |
| [8] |
Quinn A, Holloway L, Cutajar D, et al. Megavoltage cone beam CT near surface dose measurements: potential implications for breast radiotherapy[J]. Med Phys, 2011, 38(11): 6222-6227. DOI:10.1118/1.3641867 |
| [9] |
Ding GX, Alaei P, Curran B, et al. Image guidance doses delivered during radiotherapy: quantification, management, and reduction: report of the AAPM therapy physics committee task group 180[J]. Med Phys, 2018, 45(5): e84-e99. DOI:10.1002/mp.12824 |
| [10] |
de Crevoisier R, Lafond C, Mervoyer A, et al. Image-guided radiotherapy[J]. Cancer Radiother, 2022, 26(1-2): 34-49. DOI:10.1016/j.canrad.2021.08.002 |
| [11] |
Liu X, Geng LS, Huang D, et al. Deep learning-based target tracking with X-ray images for radiotherapy: a narrative review[J]. Quant Imaging Med Surg, 2024, 14(3): 2671-2692. DOI:10.21037/qims-23-1489 |
| [12] |
van Herk M. Errors and margins in radiotherapy[J]. Semin Radiat Oncol, 2004, 14(1): 52-64. DOI:10.1053/j.semradonc.2003.10.003 |
| [13] |
邓金慧, 梁恒坡, 刘文举, 等. 乳腺癌放疗中扇形束CT和锥形束CT图像引导放疗的比较研究[J]. 实用肿瘤杂志, 2023, 38(6): 582-586. Deng JH, Liang HP, Liu WJ, et al. Comparative study of fan-beam CT and cone-beam CT image-guided radiotherapy in breast cancer radiotherapy[J]. J Pract Oncol, 2023, 38(6): 582-586. DOI:10.13267/j.cnki.syzlzz.2023.093 |
| [14] |
Dekker J, Essers M, Verheij M, et al. Dose coverage and breath-hold analysis of breast cancer patients treated with surface-guided radiotherapy[J]. Radiat Oncol, 2023, 18(1): 72. DOI:10.1186/s13014-023-02261-0 |
| [15] |
Mankinen M, Virén T, Seppälä J, et al. Interfractional variation in whole-breast VMAT irradiation: a dosimetric study with complementary SGRT and CBCT patient setup[J]. Radiat Oncol, 2024, 19(1): 21. DOI:10.1186/s13014-024-02418-5 |
| [16] |
Peng H, Yang H, Lei J, et al. Optimal fractionation and timing of weekly cone-beam CT in daily surface-guided radiotherapy for breast cancer[J]. Radiat Oncol, 2023, 18(1): 112. DOI:10.1186/s13014-023-02279-4 |
| [17] |
Costin IC, Marcu LG. Factors impacting on patient setup analysis and error management during breast cancer radiotherapy[J]. Crit Rev Oncol Hematol, 2022, 178: 103798. DOI:10.1016/j.critrevonc.2022.103798 |
| [18] |
Kammerer E, Le Guévelou J, Jacob S, et al. Cardiac complications of breast radiation therapy[J]. Bull Cancer, 2019, 106(4): 379-388. DOI:10.1016/j.bulcan.2019.01.020 |
| [19] |
Sarkar B, Munshi A, Ganesh T, et al. Rotational positional error corrected intrafraction set-up margins in stereotactic radiotherapy: a spatial assessment for coplanar and noncoplanar geometry[J]. Med Phys, 2019, 46(11): 4749-4754. DOI:10.1002/mp.13810 |
| [20] |
张彦新, 方浩, 陈冰, 等. ExacTrac X-射线图像引导系统在体部肿瘤放疗中的摆位误差和残余误差分析[J]. 中华放射医学与防护杂志, 2019, 39(2): 95-100. Zhang YX, Fang H, Chen B, et al. Analysis of the setup errors and residual errors for ExacTrac X-ray image-guidance system for radiotherapy of somal tumors[J]. Chin J Radiol Med Prot, 2019, 39(2): 95-100. DOI:10.3760/cma.j.issn.0254-5098.2019.02.003 |
| [21] |
申正文, 李师, 谭霞, 等. 乳腺癌根治术后放疗靶区外放边界的分析及验证[J]. 中国医学物理学杂志, 2021, 38(7): 804-808. Shen ZW, Li S, Tan X, et al. Analysis and verification of target margin for post-mastectomy radiotherapy for breast cancer[J]. Chin J Med Phys, 2021, 38(7): 804-808. DOI:10.3969/j.issn.1005-202X.2021.07.003 |
| [22] |
Hlavka A, Vanasek J, Odrazka K, et al. Tumor bed radiotherapy in women following breast conserving surgery for breast cancer-safety margin with/without image guidance[J]. Oncol Lett, 2018, 15(4): 6009-6014. DOI:10.3892/ol.2018.8083 |
| [23] |
Buschmann M, Kauer-Dorner D, Konrad S, et al. Stereoscopic X-ray image and thermo-optical surface guidance for breast cancer radiotherapy in deep inspiration breath-hold[J]. Strahlenther Onkol, 2024, 200(4): 306-313. DOI:10.1007/s00066-023-02153-y |
| [24] |
Tamponi M, Poggiu A, Dedola MF, et al. Random and systematic set-up errors in three-dimensional conformal radiotherapy-impact on planning target volume margins: the experience of the Radiation Oncology Centre of Sassari[J]. J Radiother Pract, 2014, 13(2): 166-179. DOI:10.1017/S1460396913000204 |
| [25] |
Hoekstra N, Habraken S, Swaak-Kragten A, et al. Intrafraction motion during partial breast irradiation depends on treatment time[J]. Radiother Oncol, 2021, 159: 176-182. DOI:10.1016/j.radonc.2021.03.029 |
| [26] |
董芳芬, 戴立言, 黄妙云, 等. 体表铅点标记辅助iSCOUT图像引导定位系统在乳腺癌术后调强放疗应用研究[J]. 中华放射肿瘤学杂志, 2021, 30(10): 1059-1064. Dong FF, Dai LY, Huang MY, et al. Study of setup error and dosimetry of postoperative intensity-modulated radiotherapy for breast cancer using skin lead marker and iSCOUT image-guided positioning system[J]. Chin J Radiat Oncol, 2021, 30(10): 1059-1064. DOI:10.3760/cma.j.cn113030-20210317-00111 |
| [27] |
林漳华, 邓显智, 董芳芬, 等. 光学引导跟踪系统在放疗应用中的准确性研究[J]. 中华放射医学与防护杂志, 2023, 43(9): 698-704. Lin ZH, Deng XZ, Dong FF, et al. Accuracy of the optically guided tracking system in radiotherapy[J]. Chin J Radiol Med Prot, 2023, 43(9): 698-704. DOI:10.3760/cma.j.cn112271-20230412-00116 |
| [28] |
Lai J, Luo Z, Jiang L, et al. Skin marker combined with surface-guided auto-positioning for breast DIBH radiotherapy daily initial patient setup: An optimal schedule for both accuracy and efficiency[J]. J Appl Clin Med Phys, 2024, 25(7): e14319. DOI:10.1002/acm2.14319 |
| [29] |
刘姝言, 高兴旺, 刘懿梅, 等. 锥形束CT图像引导乳腺癌放疗中不同配准方法研究[J]. 中国医学物理学杂志, 2023, 40(1): 7-12. Liu SY, Gao XW, Liu YM, et al. Comparison of different registration methods in cone beam CT image guided radiotherapy for breast cancer[J]. Chin J Med Phys, 2023, 40(1): 7-12. DOI:10.3969/j.issn.1005-202X.2023.01.002 |
| [30] |
Yamauchi R, Murayoshi N, Akiyama S, et al. Residual image registration error by fiducial markers in accelerated partial breast irradiation using C-arm linac: a phantom study[J]. Phys Eng Sci Med, 2022, 45(3): 769-779. DOI:10.1007/s13246-022-01142-2 |
 2025, Vol. 45
2025, Vol. 45


