2. 军事科学院军事医学研究院辐射医学研究所,北京 100850
2. Institute of Radiation Medicine, Academy of Military Medical Sciences, Beijing 100850, China
微波辐射作为一种新型污染源,对人类健康的影响已引起广泛关注。研究表明,脑是微波辐射敏感的重要靶器官之一[1-2]。一定剂量的微波辐射可导致焦虑样情绪行为、脑组织病理学改变、钙信号异常等[3],但对于微波辐射敏感的靶部位及其作用机制尚未明确。新近的研究表明次级视觉皮层参与情绪行为改变[4],然而,关于微波辐射对次级视觉皮层组织结构和功能的影响尚未见报道。为此,本研究在前期工作基础上,建立微波辐射动物模型,综合利用神经行为学、组织病理学以及遗传编码钙成像技术,研究微波辐射对小鼠焦虑情绪、次级视觉皮层组织结构以及神经元钙活动的影响,以期进一步揭示微波辐射神经生物学效应及其作用机理,为电磁辐射脑损伤医学防护提供参考。
材料与方法 1、实验动物及分组采用8~10周龄SPF级C57BL/6N小鼠共36只,体重22~25 g,由北京维通利华实验技术有限公司提供,许可证号:SCXK(京)2021-0006。动物饲养于军事医学研究院实验动物中心。将小鼠进行行为学训练后,按照随机数表法分为对照组和微波辐射组,其中单纯行为学检测对照组8只,辐射组7只;光纤记录结合行为学实验对照组8只,辐射组7只;苏木素-伊红(HE)染色每组各3只。
2、微波辐射方法采用军事医学研究院自建的X波段高功率微波模拟源,中心频率9.375 GHz、平均功率密度12 mW/cm2。将小鼠置于方形透明带孔有机玻璃盒中,自由体位,全身辐照,辐射15 min,对照组进行同等条件伪辐射。
3、旷场实验采用40 cm × 40 cm × 40 cm旷场箱,旷场中央16 cm × 16 cm设置为中央区域。实验前3天将小鼠放置于实验室内,并对其抓取抚摸,适应环境30 min/d,连续3 d。采用Any maze(Version 7.1, 美国Stoelting公司)视频分析软件记录5 min内小鼠的运动轨迹,计算小鼠进入中央区域的次数。
4、高架十字迷宫实验采用长30 cm、宽5 cm、高15 cm的高架十字迷宫,距离地面高度50 cm。实验前3天将小鼠放置于实验室内,并对其抓取抚摸,适应环境30 min/d, 连续3 d。采用Any maze(Version 7.1, 美国Stoelting公司)视频分析软件记录5 min内小鼠的运动轨迹,计算小鼠进入开放臂的次数。
5、脑组织病理学分析微波辐射后7 d,小鼠经腹腔注射0.5%戊巴比妥钠(50 mg/kg)麻醉后,采用10%缓冲甲醛经心脏灌注固定后取脑,脑组织依次经4%多聚甲醛固定、梯度乙醇脱水、二甲苯透明、浸蜡、石蜡包埋和切片,切片厚度3 μm,经HE染色后,利用光学显微镜观察次级视觉皮层组织形态结构,并进行显微摄像。
6、AAV-GCaMP定位注射和光纤植入小鼠经异氟烷吸入麻醉,采用脑立体定位仪、微量注射泵分别于左侧或右侧次级视觉皮层(前囟后3.30 mm,旁开1.50 mm,颅骨表面下0.5 mm),注射含基因编码钙离子指示剂(GCaMP)的腺相关病毒(rAAV-hSyn-jGCaMP7f),注射体积100 nl,留针10 min。然后,埋置光纤陶瓷插芯,牙科水泥封固。手术后3周,待病毒稳定表达之后,小鼠经心脏灌注固定及脑组织冰冻切片,通过荧光显微镜观察,验证注射部位的精确性。
7、基于遗传编码钙成像技术检测次级视觉皮层神经元钙活动采用光纤记录系统(千奥星科南京生物科技有限公司),结合旷场、高架十字迷宫行为学实验范式,分别对小鼠探索旷场中央区域、高架十字迷宫开放臂行为进行标记,记录小鼠发生打标行为时,次级视觉皮层神经元钙活动的变化。利用光纤记录系统基于Matlab的数据分析软件,采用Z-score算法分析钙信号变化幅度,并计算钙信号线下面积(area under curver, AUC)的变化。
8、统计学处理应用SPSS 26.0软件进行统计学分析,GraphPad Prism 8软件作图。数据经正态性检验符合正态分以x ± s表示。行为学数据组间比较采用独立样本t检验,组内比较采用配对样本t检验,钙信号数据分析采用独立样本t检验。P < 0.05为差异具有统计学意义。
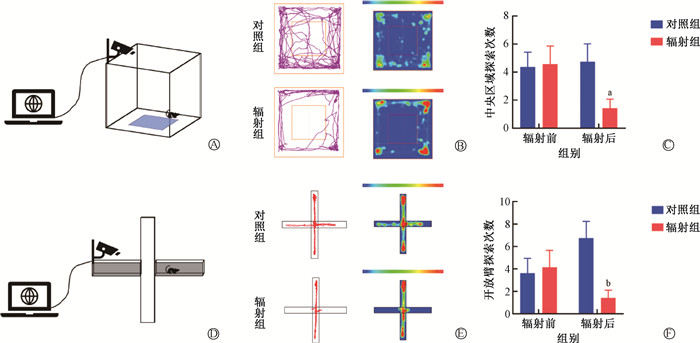
结果 1、微波辐射对小鼠焦虑样行为的影响旷场实验结果显示,微波辐射前,辐射组与对照组相比,小鼠探索旷场中央区域次数差异无统计学意义(P>0.05)。微波辐射后,辐射组小鼠探索旷场中央区域次数较对照组减少,差异有统计学意义(t=2.24, P < 0.05)。但对照组辐射(伪辐射)前后变化不明显,差异无统计学意义(P>0.05)。实验结果显示,微波辐射前,辐射组与对照组相比,小鼠探索高架十字迷宫开放臂区域次数差异无统计学意义(P>0.05)。微波辐射后,辐射组小鼠探索开放臂次数较对照组减少,差异有统计学意义(t=3.10, P < 0.01)。但对照组辐射(伪辐射)前后变化不明显,差异无统计学意义(P>0.05)。以上结果表明,微波辐射可导致小鼠焦虑样行为发生,见图 1。
|
注:与对照组比较,at=2.24, P < 0.05; bt=3.10, P < 0.01 图 1 微波辐射对小鼠焦虑样行为的影响 A. 旷场实验模式图;B. 小鼠探索旷场轨迹图与热度图;C. 微波辐射对小鼠探索旷场中央区域次数的影响;D. 高架十字迷宫实验模式图;E. 小鼠探索高架十字迷宫轨迹图与热度图;F. 微波辐射对小鼠探索高架十字迷宫开放臂次数的影响 Figure 1 Effects of microwave radiation on anxiety-like behavior of mice A. Nomogram of open-field test; B. Trajectory diagram and heat map of mice when exploring the open field; C. Effects of microwave radiation on the frequency of the mice′s exploration into the central region of the open field; D. Nomogram of elevated plus maze test; E. Trajectory diagram and heat map of mice when exploring elevated plus maze; F. Effects of microwave radiation on the frequency of mice′s exploration into the open arm of the elevated plus maze |
2、小鼠次级视觉皮层组织形态结构的影响
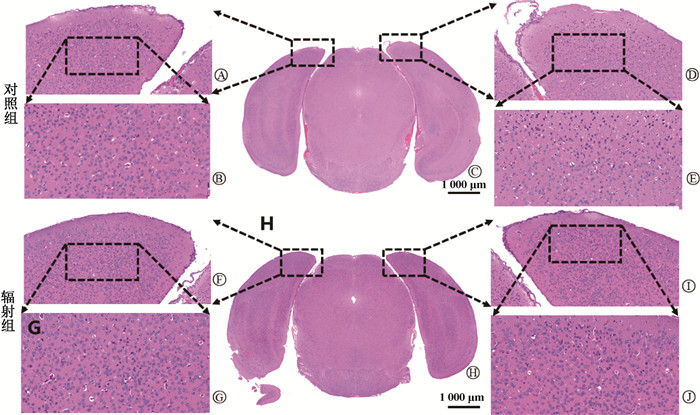
微波辐射后7 d,对照组小鼠次级视觉皮层组织结构基本正常,辐射组可见次级视觉皮层部分神经元变性、凋亡,主要表现为神经元胞体皱缩、核固缩深染,血管周间隙略增宽。表明微波辐射可导致次级视觉皮层组织病理学改变,见图 2。
|
图 2 微波辐射对小鼠次级视觉皮层组织形态结构的影响 A. 对照组左侧次级视觉皮层组织× 20;B. 对照组左侧次级视觉皮层组织× 40;C. 对照组大脑组织切片× 2;D. 对照组右侧次级视觉皮层组织× 20;E. 对照组右侧次级视觉皮层组织× 40;F. 辐射组左侧次级视觉皮层组织× 20;G. 辐射组左侧次级视觉皮层组织× 40;H. 辐射组大脑组织切片× 2;I. 辐射组右侧次级视觉皮层组织× 20;J. 辐射组右侧次级视觉皮层组织× 40 Figure 2 Effects of microwave radiation on histomorphology of the secondary visual cortex A. Left secondary visual cortex tissue in the control group, × 20; B. Left secondary visual cortex tissue in the control group, × 40; C. Brain tissue section of the control group, × 2; D. Right secondary visual cortex tissue in the control group, × 20; E. Right secondary visual cortex tissue in the control group, × 40; F. Left secondary visual cortex tissue in the radiation group, × 20; G. Left secondary visual cortex tissue in the radiation group, × 40; H. Brain tissue section of the radiation group, × 2; I. Right secondary visual cortex tissue in the radiation group, × 20; J. Right secondary visual cortex tissue in the radiation group, × 40 |
3、小鼠次级视觉皮层AAV-hSyn-GCaMP注射靶部位确证
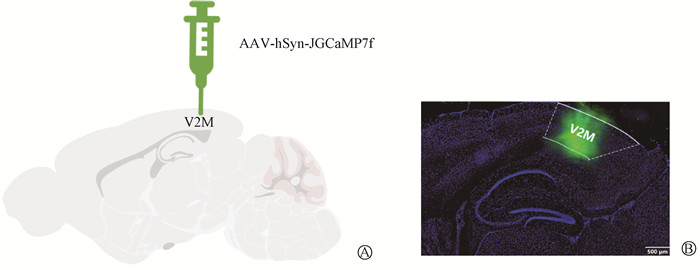
AAV-hSyn-JGCaMP7f注射后3周,小鼠经心脏灌注固定后,取脑组织冰冻切片,采用激光扫描共聚焦显微镜观察荧光蛋白表达,参照小鼠脑立体定位图谱,可见小鼠次级视觉皮层内侧区(medial area of secondary visual cortex, V2M)GCaMP绿色荧光蛋白的特异表达,表明次级视觉皮层V2M区立体定位注射靶部位准确,见图 3。
|
图 3 小鼠次级视觉皮层V2M区AAV-hSyn-JGCaMP7f注射靶部位验证 A. V2M区AAV-hSyn-JGCaMP7f注射模式图;B. V2M区GCaMP绿色荧光蛋白表达 Figure 3 Confirmation of the target site of the AAV-hSyn-JGCaMP7f injection in V2M A. Injection mode diagram of the AAV-hSyn-JGCaMP7f in V2M region; B. Green fluorescent protein expression of GCaMP in V2M region |
4、微波辐射对小鼠次级视觉皮层神经元钙活动的影响
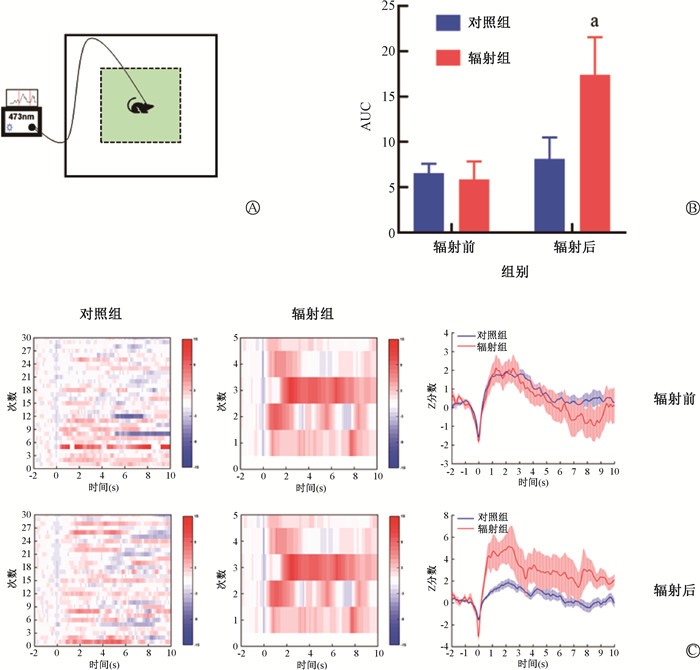
光纤记录结合旷场实验结果显示,微波辐射前,当小鼠探索旷场中央区域时,与对照组相比,辐射组小鼠次级视觉皮层神经元钙活动不明显,差异无统计学意义(P>0.05)。微波辐射后,当小鼠探索旷场中央区域时,辐射组小鼠次级视觉皮层神经元钙活动较辐射前增强,差异有统计学意义(t=-2.75, P < 0.05),但对照组辐射(伪辐射)前后变化不明显(P>0.05,图 4)。
|
图 4 光纤记录结合旷场实验检测微波辐射对次级视觉皮层神经元钙活动的影响 A. 光纤记录结合旷场行为学模式图;B. 微波辐射后小鼠探索旷场中央区域时V2M区神经元钙信号AUC的变化;C. 小鼠探索旷场中央区域时钙信号热度图及信号幅度变化图 Figure 4 Effects of microwave radiation on calcium activity in neurons of the secondary visual cortex as detected using fiber optic recording combined with elevated plus maze test A. Nomogram of optical fiber recording combined with behavior in the open field; B. Changes in the AUC of calcium signals in neurons in the V2M region of mice when exploring the central region of the open field after microwave irradiation; C. Heat map of calcium signals of mice when exploring the central region of the open field and the diagram showing the variations in the signal amplitude |
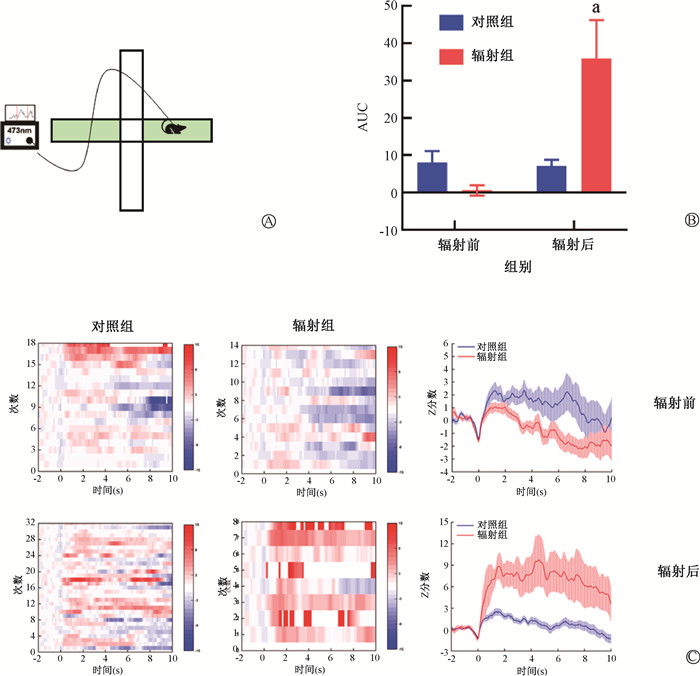
光纤记录结合高架十字迷宫实验结果显示,微波辐射前,当小鼠探索高架十字迷宫开放臂区域时,与对照组相比,辐射组小鼠次级视觉皮层神经元钙活动变化不明显,差异无统计学意义(P>0.05)。微波辐射后,当小鼠进入高架十字迷宫开放臂时,辐射组小鼠次级视觉皮层神经元钙活动较辐射前(t=-3.41, P < 0.05)和对照组(t= -2.77, P < 0.05)均增强,差异有统计学意义,但对照组辐射(伪辐射)前后变化不明显,差异无统计学意义(P>0.05,图 5)。
|
注:a与对照组或同组辐射前比较,t=-2.77、-3.41,P < 0.05;AUC. 曲线下面积 图 5 光纤记录结合高架十字迷宫实验检测微波辐射对V2M区神经元钙活动的影响 A. 光纤记录结合高架十字迷宫行为学模式图;B. 微波辐射后小鼠探索高架十字迷宫开放臂时V2M区神经元钙信号AUC的变化;C. 小鼠探索旷场高架十字迷宫开放臂时钙信号热度图及变化图 Figure 5 Effects of microwave radiation on calcium activity in neurons of the secondary visual cortex as detected using fiber optic recording combined with elevated plus maze test A. Nomogram of optical fiber recording combined with behavior in the elevated plus maze behavior; B. Changes in the AUC of calcium signals in neurons in the V2M region of mice when exploring the open arm of the elevated plus maze after microwave irradiation; C. Heat map of calcium signals of mice when exploring the open arm of the elevated plus maze and the diagram showing variations in the signal amplitude |
以上结果表明,次级视觉皮层神经元钙活动增强参与微波辐射致小鼠焦虑样行为发生,提示次级视觉皮层神经元活性增强是微波辐射致焦虑情绪改变的重要机制。
讨论流行病学调查显示,长期低剂量的微波辐射可导致电磁环境工作人员或学生产生焦虑、头疼、注意力分散、学习记忆能力下降等症状[5-6]。多项动物实验研究也表明,一定剂量的微波辐射可引起动物焦虑样行为发生[7-9]。徐茜等[10]研究发现,频率900 MHz、平均功率密度90 μW/cm2的微波辐射可在一定程度上影响小鼠对外界环境的兴奋性,旷场结果显示,辐射组小鼠的活动时间减少,活动总路程和平均速度增加,休息时间减少。Júnior等[11]将大鼠暴露于频率1.8 GHz,场强2 V/m的全球移动通信系统手机产生的射频辐射中,连续3 d,旷场实验结果表明,辐射组大鼠的静止时间和站立次数均较对照组明显增加。Zhang等[12]研究表明,中心频率2.856 GHz,平均功率密度30 mW/cm2微波辐射Wistar大鼠15 min,辐射后大鼠旷场中央区域路程占比、活动总路程、平均速度均显著下降。Deshmukh等[13]分别采用900、1 800、2 450 MHz 3种不同频率的微波连续辐射雄性Fischer大鼠90 d,发现辐射后大鼠进入高架十字迷宫闭合臂时间增加。以上研究均表明,一定条件下微波辐射可引起小鼠焦虑情绪发生。与以往研究报道一致,本研究首次采用频率9.375 GHz、平均功率密度12 mW/cm2微波辐射,发现辐射后小鼠产生焦虑样情绪行为改变。
视觉皮层可分为初级视觉皮层与次级视觉皮层。视觉皮层神经元的活性决定了视觉加工的程度[14]。与初级视觉皮层相比,除了方向选择性外,次级视觉皮层的神经元拥有更复杂的空间特征选择性[15]。Sun等[16]发现大鼠能将识别的运动信息分配给次级视觉皮层,并促进次级视觉皮层的发育。新近研究发现,利用化学遗传抑制次级视觉皮层神经元时,小鼠表现出社交指数下降,强迫游泳静止时间延长,进入高架十字迷宫开放臂、旷场中央区域次数减少等焦虑抑郁样行为,而利用光遗传激活次级视觉皮层神经元后上述情绪行为异常可明显缓解[4]。
以往许多研究发现,一定剂量的微波辐射可引起脑组织结构损伤,主要涉及血脑屏障、大脑皮层、海马、纹状体等部位等[9, 17-23]。但关于电磁辐射对视觉皮层结构和功能的影响及其行为学改变的关系尚未见研究报道。本研究以次级视觉皮层为切入点,分析微波辐射对次级视觉皮层组织形态结构以及神经元钙活动的影响,并探讨其在辐射致情绪行为改变中的作用。与以往报道的微波辐射脑损伤病理学变化特点相似,本研究中微波辐射所致次级视觉皮层组织病理学改变主要表现为神经元胞体皱缩、核固缩深染以及血管周隙增宽。提示次级视觉皮层组织形态结构损伤参与微波辐射致神经行为改变。
钙信号异常是微波辐射神经生物学效应的重要机制。通常认为,细胞膜是电磁辐射作用的主要靶部位,并且含有丰富的离子通道和介导下游信号转导的受体。关于电磁辐射对细胞钙信号的影响,已有的研究报道多集中于钙通道相关的信号通路,电磁辐射可改变细胞膜上的钙离子通道和受体,使钙离子分布及细胞膜通透性发生变化[24-25]。本研究基于遗传编码钙成像技术,利用光纤记录结合神经行为学范式研究发现,次级视觉皮层神经元钙活动增强参与微波辐射致小鼠焦虑样行为发生,提示次级视觉皮层神经元活性增强是微波辐射致焦虑情绪改变的重要机制。
综上所述,本研究揭示了微波辐射对次级视觉皮层组织形态结构及神经元钙活动的影响,次级视觉皮层神经元钙活动增强参与微波辐射致焦虑样行为发生,提示次级视觉皮层神经元参与构成微波辐射致焦虑情绪行为的神经环路,并可能在微波辐射致神经行为改变中发挥重要作用。对于次级视觉皮层神经元在微波辐射致神经行为改变中的作用机制,尚需结合光遗传、化学遗传、病毒示踪等神经科学前沿技术,进一步阐明微波辐射作用敏感的次级视觉皮层神经元类型及其神经环路精细调节机制。总之,本研究对于从神经环路水平揭示微波辐射影响焦虑情绪的机制提供了线索,为电磁辐射脑损伤医学防护提供了实验依据和参考。
利益冲突 无
作者贡献声明 冯志华负责实验操作、数据分析和论文撰写;潘婷、何钢华、常晨旭负责实验操作;崔智琳、杨镁楹负责采集数据;郝延辉、柳峰松、李杨、左红艳负责指导实验设计和论文撰写
| [1] |
Miller AB, Sears ME, Morgan LL, et al. Risks to health and well-being from radio-frequency radiation emitted by cell phones and other wireless devices[J]. Front Public Health, 2019, 7: 223. DOI:10.3389/fpubh.2019.00223 |
| [2] |
Mumtaz S, Rana JN, Choi EH, et al. Microwave radiation and the brain: mechanisms, current status, and future prospects[J]. Int J Mol Sci, 2022, 23(16): 9288. DOI:10.3390/ijms23169288 |
| [3] |
Narayanan SN, Jetti R, Kesari KK, et al. Radiofrequency electromagnetic radiation-induced behavioral changes and their possible basis[J]. Environ Sci Pollut Res Int, 2019, 26(30): 30693-30710. DOI:10.1007/s11356-019-06278-5 |
| [4] |
Lu J, Zhang Z, Yin X, et al. An entorhinal-visual cortical circuit regulates depression-like behaviors[J]. Mol Psychiatry, 2022, 27(9): 3807-3820. DOI:10.1038/s41380-022-01540-8 |
| [5] |
Durusoy R, Hassoy H, Özkurt A, et al. Mobile phone use, school electromagnetic field levels and related symptoms: a cross-sectional survey among 2150 high school students in Izmir[J]. Environ Health, 2017, 16(1): 51. DOI:10.1186/s12940-017-0257-x |
| [6] |
Zhi WJ, Wang LF, Hu XJ. Recent advances in the effects of microwave radiation on brains[J]. Mil Med Res, 2017, 4(1): 29. DOI:10.1186/s40779-017-0139-0 |
| [7] |
Van Eeghe V, El Arfani A, Anthoula A, et al. Selective changes in locomotor activity in mice due to low-intensity microwaves amplitude modulated in the EEG spectral domain[J]. Neuroscience, 2017, 359: 40-48. DOI:10.1016/j.neuroscience.2017.06.056 |
| [8] |
闵霞. 900 MHz微波辐射对小鼠情绪、记忆及肠道菌群影响研究[D]. 北京: 军事科学院, 2019. Min X. Investigation of the impact of 900 MHz microwave radiation tothe emotion, memory and gut microbiome of mice[D]. Beijing: Academy of Military Sciences, 2019. |
| [9] |
胡翠翠. 基于海马胆碱能神经元调控研究微波辐射致神经行为改变的机制[D]. 合肥: 安徽医科大学, 2023. Hu CC. Studies on the mechanism of neurobehavioral changes induced by microwave radiation based on hippocampal cholinergic neuron[D]. Hefei: Anhui Medical University, 2023. |
| [10] |
徐茜, 柴栋, 孟谦谦, 等. 900 MHz微波辐射对小鼠头部表面温度及神经行为的影响[J]. 环境与职业医学, 2009, 26(2): 148-151. Xu Q, Chai D, Meng QQ, et al. Effects of 900 MHz microwave radiation on the head surface temperature and neurobehavior of mice[J]. J Environ Occup Med, 2009, 26(2): 148-151. DOI:10.13213/j.cnki.jeom.2009.02.021 |
| [11] |
Júnior LC, Guimarães Eda S, Musso CM, et al. Behavior and memory evaluation of Wistar rats exposed to 1.8 GHz radiofrequency electromagnetic radiation[J]. Neurol Res, 2014, 36(9): 800-803. DOI:10.1179/1743132813Y.0000000276 |
| [12] |
Zhang LH, Pang LL, Zhu SQ, et al. Intranasal tetrandrine temperature-sensitive in situ hydrogels for the treatment of microwave-induced brain injury[J]. Int J Pharm, 2020, 583: 119384. DOI:10.1016/j.ijpharm.2020.119384 |
| [13] |
Deshmukh PS, Megha K, Nasare N, et al. Effect of low level subchronic microwave radiation on rat brain[J]. Biomed Environ Sci, 2016, 29(12): 858-867. DOI:10.3967/bes2016.115 |
| [14] |
Lee SW, Fried SI. Micro-magnetic stimulation of primary visual cortex induces focal and sustained activation of secondary visual cortex[J]. Philos Trans A Math Phys Eng Sci, 2022, 380(2228): 20210019. DOI:10.1098/rsta.2021.0019 |
| [15] |
Liu L, She L, Chen M, et al. Spatial structure of neuronal receptive field in awake monkey secondary visual cortex (V2)[J]. Proc Natl Acad Sci USA, 2016, 113(7): 1913-1918. DOI:10.1073/pnas.1525505113 |
| [16] |
Sun B, Lv B, Dong Q, et al. Watching moving images specifically promotes development of medial area of secondary visual cortex in rat[J]. Dev Neurobiol, 2009, 69(9): 558-567. DOI:10.1002/dneu.20724 |
| [17] |
Hao Y, Liu W, Liu Y, et al. Effects of nonthermal radiofrequency stimulation on neuronal activity and neural circuit in mice[J]. Adv Sci(Weinh), 2023, 10(11): e2205988. DOI:10.1002/advs.202205988 |
| [18] |
孔晓旭. 粉防己碱对微波辐射脑损伤的治疗作用及其机制研究[D]. 合肥: 安徽医科大学, 2023. Kong XX. Study on the therapeutic effect and mechanism of tetrandrine on microwave radiation brain injury[D]. Hefei: Anhui Medical University, 2023. |
| [19] |
Zhu R, Wang H, Xu X, et al. Effects of 1.5 and 4.3 GHz microwave radiation on cognitive function and hippocampal tissue structure in Wistar rats[J]. Sci Rep, 2021, 11(1): 10061. DOI:10.1038/s41598-021-89348-4 |
| [20] |
胡翠翠, 常晨旭, 孔晓旭, 等. 微波辐射对小鼠联合型学习记忆功能及海马组织结构的影响[J]. 中华放射医学与防护杂志, 2022, 42(7): 481-486. Hu CC, Chang CX, Kong XX, et al. Influence of microwave radiation on associative learning and memory function and hippocampal structure in mice[J]. Chin J Radiol Med Prot, 2022, 42(7): 481-486. DOI:10.3760/cma.j.cn112271-20220324-00120 |
| [21] |
孔晓旭, 冯志华, 王雪佳, 等. 粉防己碱对微波辐射致纹状体损伤的治疗作用及机制探讨[J]. 中华放射医学与防护杂志, 2023, 43(5): 328-334. Kong XX, Feng ZH, Wang XJ, et al. Mechanism of the therapeutic effect of Tetrandrine on striatum injury caused by microwave radiation[J]. Chin J Radiol Med Prot, 2023, 43(5): 328-334. DOI:10.3760/cma.j.cn112271-20230113-00010 |
| [22] |
Zheng R, Zhang X, Gao Y, et al. Biological effects of exposure to 2650 MHz electromagnetic radiation on the behavior, learning, and memory of mice[J]. Brain Behav, 2023, 13(6): e3004. DOI:10.1002/brb3.3004 |
| [23] |
Singh KV, Prakash C, Nirala JP, et al. Acute radiofrequency electromagnetic radiation exposure impairs neurogenesis and causes neuronal DNA damage in the young rat brain[J]. Neurotoxicology, 2023, 94: 46-58. DOI:10.1016/j.neuro.2022.11.001 |
| [24] |
Pilla A, Fitzsimmons R, Muehsam D, et al. Electromagnetic fields as first messenger in biological signaling application to calmodulin-dependent signaling in tissue repair[J]. Biochim Biophys Acta, 2011, 1810(12): 1236-1245. DOI:10.1016/j.bbagen.2011.10.001 |
| [25] |
Narayanan SN, Mohapatra N, John P, et al. Radiofrequency electromagnetic radiation exposure effects on amygdala morphology, place preference behavior and brain caspase-3 activity in rats[J]. Environ Toxicol Pharmacol, 2018, 58: 220-229. DOI:10.1016/j.etap.2018.01.009 |
 2024, Vol. 44
2024, Vol. 44


