先天性心脏病(CHD)是儿童常见的先天性畸形之一[1-2]。CHD的早期诊断及治疗能够提高先天性心脏病患儿的生存质量。经胸超声心动图是CHD首选的影像学检查方法,但受声窗影响,不能很好地显示主动脉弓等心外结构[3-5]。近年来,CT血管成像已成为CHD术前检查的重要工具,但对于年龄小、体重低的患儿,如何在保证图像质量前提下,减低辐射剂量是临床难题。双源CT(DSCT)提供的前瞻性心电门控大螺距扫描模式,可以在一个心动周期内完成数据采集,大大降低辐射剂量,尤其是第三代DSCT,但对婴幼儿的CHD的辐射剂量和图像质量方面报道不多。本研究将评估第三代DSCT前瞻性心电门控大螺距扫描模式在诊断婴幼儿CHD中的价值。
资料与方法1. 病例资料:前瞻性连续收集阜外华中心血管病医院临床确诊为先天性心脏病、拟行手术治疗需要的患儿进行心脏DSCT检查。纳入标准:①患儿体重<10 kg。②临床及手术资料完整。排除标准:①碘对比剂过敏和心肾功能不全患儿。②外周血管条件差不能建立静脉通路者。③已做过手术患儿。④患儿不能配合CT检查者。本研究共纳入243例患者,其中,男120例,女123例,中位年龄为5个月。每例均在CT检查前由其监护人签署患者知情同意书,该研究经医院伦理委员会审查通过[(2019)伦审第(9)号]。
2. 检查设备和分组:采用第二代双源CT扫描仪(Somatom Definition Flash,德国西门子公司)和第三代双源CT扫描仪(Somatom Force,德国西门子公司),采用随机数法分为3组进行CT检查,第一组采用第三代DSCT前瞻性心电门控大螺距扫描(Flash3rd组),第二组采用第二代DSCT前瞻性心电门控大螺距扫描(Flash2nd组),第三组采用第三代DSCT前瞻性心电门控序列扫描(Sequence3rd组),每组81例。
3. 检查方法和扫描参数:患儿仰卧位,胸前粘贴电极,熟睡后自由呼吸状态下头尾方向扫描,范围自胸廓入口至膈下5 cm。3组对比剂使用碘克沙醇(320 mg/ml),1.5 ml/kg,0.1~0.12 ml·s-1· kg-1,设定至少维持12 s的药物注射时间,以同等流率注射等量生理盐水,扫描监测间隔1 s,当四腔心均显影时手动触发延迟3 s扫描。具体扫描参数见表 1。
|
|
表 1 不同CT扫描模式的参数表 Table 1 List of scanning parameters of different scanning mode |
4. 图像后处理及分析:扫描及重建完成后数据传送至德国西门子Syngo.via后处理工作站,进行多平面重建(MPR)、最大密度投影(MIP)和容积再现(VR)等图像后处理。
图像质量的客观评分:包括主动脉及肺动脉的CT值,主动脉及肺动脉的噪声值和主动脉及肺动脉的信噪比(SNR)。测量层厚0.75 mm,感兴趣区(ROI)放置在升主动脉根部及肺动脉主干,ROI面积13 mm2,ROI尽量位于血管中心区,同层面测量5次,取其平均值。SNR =(主动脉或肺动脉CT值)/(主动脉或肺动脉噪声值)。
图像质量的主观评分:由2名具有5年以上诊断经验的诊断医师对图像质量进行独立主观评分:5分,显示清晰,无任何伪影;4分,有轻微伪影,但有高度诊断信心;3分,明显模糊,但有中等度诊断信心;2分,部分结构或关系不能确定,诊断困难;1分,伪影严重,不能诊断。评分≥3分可用于诊断[6]。有效剂量(E)计算:扫描完成后自动生成剂量长度乘积(DLP)和容积CT剂量指数(CTDIvol),E =DLP×k。k为换算因子,年龄<4个月组为0.039,4个月~1岁组为0.026,1~6岁组为0.018 [6]。
5. 患儿心内外结构畸形分析:以手术结果为标准,按照心内外结构畸形分别统计3组患儿不同畸形发生情况,其中心内畸形包括室间隔缺损、房间隔缺损等心内结构的异常,心外畸形包括动脉导管未闭、主动脉弓缩窄、肺静脉异位引流等心外结构的异常。两名诊断医师分别对DSCT显示的所有患儿心内及心外畸形进行盲法判读,若两人意见不一致,则以高年资诊断医师意见为准。记录DSCT对各种畸形的确诊数、漏诊数、误诊数,并与手术结果进行比较。
6. 统计学处理:采用SPSS 22.0软件进行统计学分析。采用Kolmogorov-Smirnov检验评价计量资料的正态性,若符合正态分布,则采用x±s描述数据,若方差齐,则采用方差分析对比3组间差异,两两比较采用LSD-t检验。若不符合正态分布或方差不齐,则采用M(Q1,Q3)描述数据,采用Kruskal-Wallis检验比较3组间差异,采用All pairwise法进行两两比较。2名诊断医师的一致性用Kappa系数表示。采用卡方检验比较3组诊断准确率间的差异。P<0.05为差异有统计学意义。
结果1. 一般资料的比较:Flash3rd组男性患儿39例,女性患儿42例,中位年龄为5个月,中位体重为6.30 kg,中位心率为125次/min。Flash2nd组男性患儿38例、女性患儿43例,中位年龄为4个月,中位体重为5.60 kg,中位心率为129次/min。Sequence3rd组男性患儿43例、女性患儿38例,中位年龄为5个月,中位体重为5.05 kg,中位心率为122次/min。3组间年龄、体重及心率的比较差异无统计学意义(P>0.05)。
2. 3组扫描模式间患儿有效剂量比较:Flash3rd组、Flash2nd组和Sequence3rd组患儿有效剂量E分别为0.24(0.19, 0.27)、0.11(0.10, 0.14) 及0.44(0.39, 0.48)mSv,Flash2nd组明显低于Flash3rd组(H=76.12,P<0.05),Flash3rd组明显低于Sequence3rd组(H=-82.74,P<0.05),差异有统计学意义。
3. 3组扫描模式间图像质量的比较
(1) 客观评价:Flash3rd组和Flash2nd组的主、肺动脉CT值均高于Sequence3rd组,Flash3rd组和Sequence3rd组主、肺动脉SD均低于Flash2nd组(H= -40.27~33.38,P<0.01),Flash3rd组主、肺动脉SNR均高于Flash2nd组和Sequence3rd组(H= -0.90~51.42,P<0.05,表 2)。
|
|
表 2 不同CT扫描模式下图像质量主客观评价的比较[M(Q1, Q3)] Table 2 Comparison of objective and subjective evaluation for image quality at different CT scanning mode[M(Q1, Q3)] |
(2) 主观评价:2名诊断医师分别对Flash3rd组、Flash2nd组和Sequence3rd组图像进行主观评分,Kappa系数分别为0.88、0.80及0.83,一致性好,选择观察者1的主观评分进行分析,结果表明,Flash3rd组、Sequence3rd组主观评分均高于Flash2nd组(H=-93.39~124.05,P<0.05),Flash3rd组和Sequence3rd组差异无统计学意义,见表 2,图 1。
|
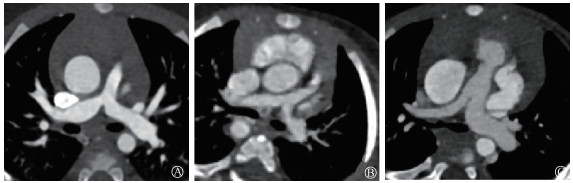
图 1 不同CT扫描模式下图像质量的评价 A. Flash3rd扫描模式;B. Flash2nd扫描模式;C. Sequence3rd扫描模式 Figure 1 Evaluation of imaging quality at different CT scanning mode A. Flash3rdscan; B. Flash2ndscan; C. Sequence3rdscan |
4. 3组扫描模式间患儿心内外结构畸形分析:Flash3rd组患儿手术共发现心内外结构畸形的诊断准确率分别为90.9%、94.8%;Flash2nd组诊断准确率分别为77.7%、88.6%;Sequence3rd组诊断准确率分别为88.9%、92.2%。在诊断心内结构畸形方面,Flash2nd组诊断准确率显著低于Flash3rd组和Sequence3rd组(K=9.36,P<0.05),Flash3rd组和Sequence3rd组差异无统计学意义(P>0.05)。诊断心外结构畸形方面,3组诊断准确率差异无统计学意义(P>0.05,表 3)。
|
|
表 3 不同CT扫描模式对心内外结构畸形的诊断结果 Table 3 Comparison of diagnosis accuracy of intracardiac and extracardiac malformation using different CT scanning mode |
讨论
多层螺旋CT用于婴幼儿先天性心脏病的诊断已有多年的历史,然而,由于儿童的组织器官正在发育和生长,对电离辐射效应更加敏感[7],故辐射暴露仍然是儿科成像中的一个主要问题,如何减少婴幼儿CT扫描剂量是近年来研究的趋势。随着扫描机器更新换代及扫描技术的发展,相关婴幼儿先天性心脏病低剂量扫描的研究也在不断深入[8]。
DSCT应用大螺距模式时,可以在1个心动周期内扫描整个心脏,因此从而获得更低得辐射剂量[9]。本研究的结果证实第三代DSCT前瞻性心电门控触发的大螺距扫描能够兼顾辐射剂量及图像质量,对先天性心脏病诊断具有重要的临床价值,对于体重<10 kg患儿更具优势。在本研究中,Flash3rd组患儿的有效剂量稍高于Flash2nd组,这是由于两组扫描协议的管电压及管电流的策略不同,Flash2nd组采用了设备默认的最低扫描参数(管电压固定为70 kV、管电流固定为80 mAs),且基于过往的技术及临床经验,此传统扫描参数得到的图像质量是可以满足临床最低诊断要求的。但随着临床需求的不断提高,诊断医师对部分图像质量提出质疑,需探讨出更优化的扫描参数,因此在最新的三代双源CT上对参数进行进一步探索。Flash3rd组则采用了CARE kV及CARE DOSE 4D技术[10],此技术能够智能化根据患儿的体重、体型和预设的图像质量参考水平来确定患儿所需的扫描条件,既降低剂量,又保证了图像质量,相较于第二代DSCT在优化低剂量图像质量方面更具优势。因此,Flash3rd组在辐射剂量和图像质量之间达到了平衡,技术方面更为先进,Flash3rd组的客观评分更好,主观评分也显著高于Flash2nd组,给了诊断医师更大的诊断信心。
在诊断效能方面,Flash3rd组和Sequence3rd组心内畸形的诊断准确率显著高于Flash2nd组心内畸形这是由于Flash2nd组选择了设备所能达到的最低的管电压及管电流,造成有效剂量过低,降低了图像质量,会影响诊断医生对心内细微结构的判断。以往也有研究证实,如果DSCT心电门控大螺距扫描模式的辐射剂量过低,其图像质量及诊断CHD合并冠状动脉发育异常准确率低于序列扫描[11]。相较于Sequence3rd组的序列扫描,采用三代DSCT心电门控大螺距扫描模式,使辐射剂量更低,但其对心内外畸形的诊断准确性不劣于序列扫描。综上所述,第三代DSCT前瞻性心电门控触发的大螺距检查能够兼顾辐射剂量及图像质量,对先天性心脏病诊断具有重要的临床价值。
本研究中尚存在一些不足,首先,本研究样本量较小,所得结果可能存在偏差,需提高样本量来进一步研究;其次,需要进一步探讨DSCT针对不同病种的个性化扫描模式的应用。如何在低辐射剂量的条件下得到先天性心脏病患儿的心功能信息也是未来研究的方向之一。
利益冲突 署名作者未接受任何赞助,排名无争议,文章不涉及任何利益
作者贡献声明 孙明华负责病例收集、数据测量及论文撰写;潘玉坤、温茹负责数据的收集、测量、整理及统计学处理;张继良、谢瑞刚、葛英辉负责课题设计与论文指导
| [1] |
葛文, 宋修峰, 邱庆琢, 等. 低辐射剂量宽探测器CT智能心电门控技术对儿童先天性心脏病冠状动脉的可视性评估[J]. 中国医学影像学杂志, 2023, 31(2): 118-123. Ge W, Song XF, Qiu QZ, et al. Feasibility of Auto-ECG-Gating technique with low dose wide-detector coronary CT angiography in display of the coronary artery in pediatric congenital heart disease[J]. J Med Imaging, 2023, 31(2): 118-123. DOI:10.3969/j.issn.1005-5185.2023.02.005 |
| [2] |
吴怡, 程蔚蔚. 先天性心脏病的遗传及环境因素研究进展[J]. 中华围产医学杂志, 2019, 19(6): 472-475. Wu Y, Cheng WW. Advances in the study of genetic and environmental factors in congenital heart disease[J]. Chin J Perinat Med, 2019, 19(6): 472-475. DOI:10.3760/cma.j.issn.1007-9408.2016.06.019 |
| [3] |
Xie WH, Chen LJ, Hu LW, et al. Cardiac computed tomography-derved left atrial strain and volume in pediatric patients with congenital heart disease: a comparative analysis with transthoracic echocardiography[J]. Front Cardiovasc Med, 2022, 9: 870014. DOI:10.3389/fcvm.2022.870014 |
| [4] |
Ali SA, Amin DH, Khattab RT. Intermodality agreement between TTE and low kVp ECG-gated MDCTA in diagnosis of complex CHD in pediatrics[J]. Egypt J Radiol Nucl Med, 2020, 51: 1-11. DOI:10.1186/s43055-020-00217-y |
| [5] |
Malik AA, Ahmad F, Amir S, et al. Agreement between 64-Slice multide- tector CT angiography and transthoracic echocardiography in detection of extracardiac findings of congenital heart disease[J]. J Coll Physicians Surg Pak, 2019, 29(10): 923-927. DOI:10.29271/jcpsp.2019.10.923 |
| [6] |
聂佩, 杨光杰, 徐文坚, 等. 128层双源CT前瞻性心电门控序列扫描与大螺距扫描在小儿先天性心脏病诊断准确率, 图像质量及辐射剂量的对比研究[J]. 中华放射学杂志, 2016, 50(6): 421-426. Nie P, Yang GJ, Xu WJ, et al. Accuracy, image quality and radiation dosecomparison of prospective ECG-gated sequential and high-pitch acquisitionon 128-slice dual-source CT angiography in infants and children with cong-enital heart disease[J]. Chin J Radiol, 2016, 50(6): 421-426. DOI:10.3760/cma.j.issn.1005-1201.2016.06.005 |
| [7] |
Francone M, Gimelli A, Budde RPJ, et al. Radiation safety for cardiovascular computed tomography imaging in paediatric cardiology: a jointexpert consensus document of the EACVI, ESCR, AEPC, and ESPR[J]. Eur Heart J Cardiovasc Imaging, 2022, 23(8): 279-289. DOI:10.1093/ehjci/jeac048 |
| [8] |
Tian L, Wang L, Qin Y, et al. Low-dose computed tomography (CT) for the diagnosis of congenital heart disease in Children: a meta-analysis[J]. Curr Med Imaging, 2020, 16(9): 1085-1094. DOI:10.2174/1573405616666200107110611 |
| [9] |
Schicchi N, Fogante M, Pirani PE, et al. Third generation dual source CT with ultra-high pitch protocol for TAVI planning and coronary tree assess-ment: feasibility, image quality and diagnostic performance[J]. Eur J Radiol, 2020, 122: 108749. DOI:10.1016/j.ejrad.2019.108749 |
| [10] |
Eller A, Wuest W, Scharf M, et al. Attenuation-based automatic kilovolt (kV)-selection in computed tomography of the chest: effects on radiation exposure and image quality[J]. Eur J Radiol, 2013, 82(12): 2386-2391. DOI:10.1016/j.ejrad.2013.08.043 |
| [11] |
Kravchenko D, Hart C, Garbe S, et al. Image quality and radiation dose of dual source high pitch computed tomography in pediatric congenital heart disease[J]. Sci Rep, 2022, 12(1): 9934. DOI:10.1038/s41598-022-13404-w |
 2024, Vol. 44
2024, Vol. 44


