调强放射治疗(intensity modulated radiation therapy,IMRT)和容积旋转调强放射治疗(volumetric modulated arc therapy,VMAT)逆向计划优化过程是一个复杂且耗时的过程[1],系统需要进行不断地迭代运算来实现保护正常组织和覆盖目标靶区之间的均衡[2]。同时,不同机构、不同设计者之间,计划设计方法与经验不尽相同,在计划设计过程中引入的主观性的人为因素干扰,有可能会造成计划质量参差不齐。保证治疗计划质量的标准化、均质化十分必要,以获得独立于设计者经验的高质量放疗计划[3]。
基于先验知识的计划设计方法可以减少计划设计时间,提高效率,同时还能减少计划间的异质性[4]。RapidPlan是瓦里安治疗计划系统中的一个模块[5],利用机器学习建立剂量体积直方图(dose volume histogram,DVH)预测模型,前瞻性地预测危及器官(organ at risk,OAR)的DVH范围,然后利用预测的DVH生成目标线函数进行逆向计划优化[6-7]。当前,RapidPlan已经应用于多个疾病部位,包括头颈部[8]、乳腺[9]、肺[10]、直肠[11]等。
但是,RapidPlan的研究大多基于传统的C形臂加速器,很少有研究涉及使用一种新的环形直线加速器系统Halcyon。Halcyon(Varian Medical System,CA,美国)是瓦里安基于传统C形臂加速器设计的一款全新加速器,具有独特的性能,如无铅门,双层多叶准直器(multileaf collimator,MLC)。该设计使机架及MLC的运动速度更快[12-13],大大减少了治疗时间,降低了患者分次内的移动可能,同时避免了碰撞的风险。同时该设计还可以有效降低射束的穿射与漏射剂量。一些研究已经表明,这些独特的优势会减少危及器官的受照量[14]。
由于上述特点,本研究旨在建立基于Halcyon 2.0环形加速器的宫颈癌术后VMAT放疗RapidPlan模型,并比较人工计划与RapidPlan自动计划在剂量学、计划一致性、计划执行效率之间的差异,进而评估基于Halcyon 2.0系统的RapidPlan模块在宫颈癌术后计划设计的临床可行性与标准化应用方法。
资料与方法1. 病例选择和图像采集:本研究从中国医学科学院北京协和医院放疗中心患者数据库中回顾性选取98例宫颈癌Ⅰ、Ⅱ期术后放疗患者,术后病理为中低分化鳞癌,须接受术后盆腔放疗。所有患者定位方式相同。定位前,保持膀胱充盈,并口服造影剂(泛影葡胺)以增加肠系结构对比度,仰卧位,使用热塑膜固定。模拟定位CT为荷兰飞利浦Brilliance Bigbore大孔径CT(管电压140 kV),采集层厚为0.5 cm。
2. 靶区及危及器官勾画:CT定位图像传输到Varian Eclipse15.6计划系统中,临床医生根据ICRU 52[15]、ICRU 62[16]报告对所有患者进行靶区勾画,临床靶区(clinical target volume,CTV)外放得到计划靶区(planning target volume,PTV)并进行危及器官勾画,危及器官均包括膀胱、直肠、小肠、骨髓、左右股骨头、脊髓。靶区外的小肠和脊髓保留至靶区上下5 cm。
3. 处方剂量和计划设计:所有患者处方剂量均为单次1.8 Gy。计划要求处方剂量至少包绕95%的靶区体积,同时在保证靶区适形度和均匀性的基础上,尽量降低危及器官受照剂量。所有计划设计均基于Halcyon 2.0环形加速器,使用VMAT技术,4个全弧照射,准直器旋转角度分别设置为为45°、45°、315°、315°,等中心点位于整个靶区的几何中心,射线光子能量为6 MV-FFF,剂量率为800 MU/min。所有计划均使用瓦里安Eclipse 15.6.06治疗计划系统设计,剂量算法为AAA剂量体积算法,优化算法为PO算法,计算网格为2.5 mm,所有计划均经过一次中间剂量计算。
4. 模型的建立与评估:将98例由资深物理师设计的人工Halcyon 2.0治疗计划导入Rapidplan模型并进行训练。DVH预测模型训练完成后,需要对模型进行优度检验,以评估该模型的预测能力。检验指标包括:模型决定系数(R2)、平均卡方值(χ2)、均方差(MSE)等,这些指标表征了原始DVH和重建预测DVH之间的差别,可以通过RapidPlan模块中的统计工具进行评价。同时,在模型建立过程中,会产生一些异常值,异常值是对导入模型计划进行统计分析后得出的结果,代表的是与中位数的差别。包括一些强影响点、几何学异常值、剂量学异常值等。例如,一个过度充盈的膀胱或排空的膀胱与大多数适度充盈的膀胱相比,就是一个几何学异常值。定量指标有Cook′s Distance(CD)、Modified Z-score value (mZ)、Studentized residual (SR)等。已有研究表明,多个异常值的存在往往会降低计划质量[17]。因此,在模型建立后,需要尽可能排除多数异常值,以消除对模型质量可能带来的负面影响。
在上述患者数据库中再次选取20例经过临床验证的宫颈癌术后患者病例,作为验证集,用于验证已建立的RapidPlan模型的计划设计能力。验证集与训练集中的所有病例的靶区勾画标准和危及器官勾画标准一致。20例计划处方量均设置为36 Gy/20次,均以处方剂量覆盖95%体积进行归一。使用RapidPlan模型自动生成DVH优化目标和权重,在Halcyon2.0机器上采用与人工计划相同的布野方式进行VMAT计划优化,并比较其与人工计划在剂量学、一致性、执行效率等方面的差异。
5. 计划评估指标:DVH图可以直观地反映靶区和危及器官的剂量分布,将验证集中20例患者的两组计划的DVH图以文本形式输出,导入到Origin 2018软件中绘制出靶区和危及器官的平均DVH图和标准差。
靶区评估指标为:最大剂量Dmax、平均剂量Dmean、最小剂量Dmin,D2%(2%的PTV体积受照剂量),D98%(98%的PTV体积受照剂量)。靶区的适形性指数(conformity index,CI)利用公式(1)计算:
| $ \mathrm{CI}=\frac{V_{\mathrm{TR}}}{V_{\mathrm{T}}} \times \frac{V_{\mathrm{TR}}}{V_{\mathrm{R}}} $ | (1) |
式中,VTR为100%等剂量线包绕的靶区体积;VT为靶区的体积;VR为100%处方等剂量线包绕的体积。CI值的范围在[0, 1]之间,当等于1时,靶区适形性最高,正常组织不接受大于等于处方剂量的照射。靶区的均匀性指数(homogeneity index,HI)利用公式(2)计算:
| $ \mathrm{HI}=\frac{D_{2 \%}-D_{98 \%}}{D_{50 \%}} $ | (2) |
HI表征了靶区内剂量分布是否均匀,HI指数越小,靶区内剂量分布越均匀。靶区的梯度指数(gradient index,GI)利用公式(3)计算:
| $ \mathrm{GI}=\frac{V_{50 \%}}{V_{\mathrm{T}}} $ | (3) |
式中,V50%为50%等剂量线包绕的体积。GI表征了靶区外剂量跌落的速度,其越小,靶区外剂量跌落越快,对正常组织的保护越好。
危及器官评估指标包括膀胱、直肠、小肠、骨髓的:V10、V20、V30、Dmean;小肠的D2cm3;左右股骨头的D5%; 脊髓的D0.1cm3;Body的V5、Dmean。
6. 计划检验及质量保证:验证集中20例人工计划和RapidPlan自动计划均导入到ArcherQA计划评估软件中。ArcherQA使用GPU和并行处理技术,采用快速蒙特卡罗剂量计算方法对剂量再计算,对治疗计划进行二次评估。比较人工计划和自动计划的γ通过率,二者比较选取的评价标准为3%/3 mm、2%/2 mm,阈值10%。
验证集中20例人工计划和RapidPlan自动计划移植到电子射野影像系统(electronic portal imaging device,EPID)进行平面剂量验证。使用γ通过率评估治疗计划系统生成的平面剂量分布与实际测量剂量分布的差异。在Eclipse系统Portal Dosimetry分析中选取的指标为2%/2 mm和1%/1 mm,阈值10%。
比较人工计划和RapidPlan自动计划的机器总跳数(monitor unit,MU)。每个计划的总跳数可以作为衡量计划复杂程度的定量指标[18]。同样的处方量,总跳数越高,计划越复杂,机器的实际执行能力也就越低。同时,由于Halcyon的MLC运行速度快,机架很少变速。因此,计划总跳数越高,往往实际临床治疗所需的时间也就越长,患者的依从性越差。
7. 统计学处理:剂量学指标结果、γ通过率、MU值结果以x±s表示,采用GraphPad Prism 8对验证集中的数据进行配对t检验。P < 0.05为差异有统计学意义。
结果1. 模型建立结果:由于RapidPlan允许在训练模型之后继续对模型进行修改,因此在对导入的98例病例初次建模后,删除了一些具有明显异常值的计划(38例,计划中多个结构CD>10,mZ>3.5,CD代表库克距离,mZ代表修正后的Z值),保留了60例计划(5例50.4 Gy/28次,32例45 Gy/25次,22例36 Gy/20次,1例14.4 Gy/8次),并对修改后的模型进行再次训练,得到最终使用的RapidPlan模型。靶区和危及器官的优化条件由预测模型自动生成,所有计划在计划优化过程中均不再添加人工优化条件。
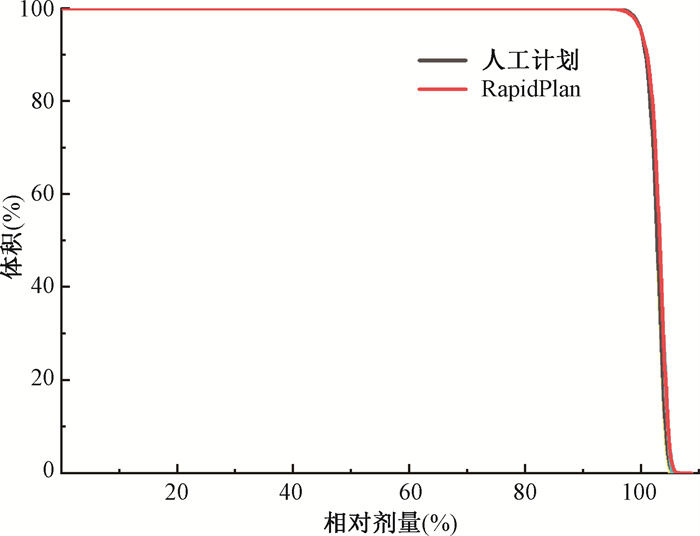
2. 靶区剂量学比较:图 1展示了验证集中20例病例人工计划和自动计划(RapidPlan)的PTV的平均DVH图。可以看到两组计划PTV的平均DVH曲线几乎完全重合(图 1黑色曲线与红色曲线),这说明对于不加任何人工干预的RapidPlan自动计划,靶区仍然可以接受到足够的处方剂量照射,满足临床要求。
|
图 1 人工计划和RapidPlan计划组靶区的PTV平均DVH图 Figure 1 Average DVH of PTV produced by RapidPlan automatic plans and manual plans |
表 1展示了两组计划中靶区的剂量学指标差异。结果表明,RapidPlan计划中靶区整体的平均剂量较人工计划略有升高,靶区内剂量最大值为(38.73±0.22)Gy,高于人工计划的(38.49±0.15)Gy,差异有统计学意义(t=5.16,P<0.05)。这可能是由于自动计划未添加任何人工干预,整体优化时间相对较短,迭代次数少于人工计划所造成。但是,RapidPlan计划的优势体现在剂量学指标标准差较小,表明数据离散程度低,计划质量更加稳定、一致性高,不因为计划设计者的经验而产生较大波动。
|
|
表 1 人工计划和RapidPlan计划靶区剂量学指标比较 Table 1 Comparison of PTV dosimetric parameters between RapidPlan automatic plans and manual plans |
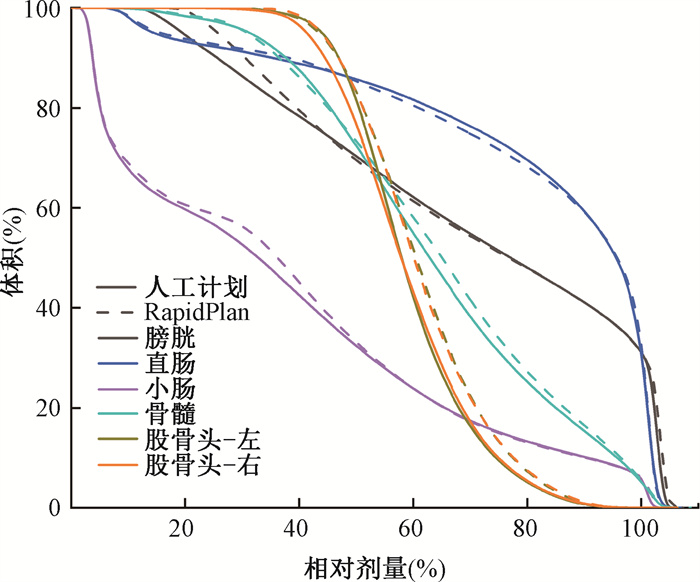
3. 危及器官剂量学比较:验证集中20例病例两组计划危及器官的平均DVH图如图 2所示,其中实线代表人工计划的平均DVH,虚线代表RapidPlan的平均DVH。从图中可以看到,对于膀胱、直肠、小肠、骨髓,两组计划的平均DVH曲线基本一致,股骨头-左、股骨头-右的平均DVH曲线RapidPlan组略高于人工计划组,但是差异有限,即RapidPlan自动计划可以实现与人工计划等同的危及器官剂量分布。
|
图 2 人工计划和RapidPlan计划组危及器官的平均DVH图 Figure 2 Average DVH of OAR produced by RapidPlan automatic plans and manual plans |
两组计划危及器官的剂量学指标见表 2,可以看到RapidPlan计划中,危及器官的某些指标略差于人工计划,但整体差距并不明显,与人工计划仍然是可比的。对于指标的标准差分析发现,RapidPlan组几乎均小于人工计划组,体现了RapidPlan计划在计划一致性方面的优势。
|
|
表 2 人工计划和RapidPlan计划危及器官剂量学指标(x±s) Table 2 OARs dosimetric parameters of RapidPlan automatic plans and manual plans(x±s) |
4. 计划独立核查和验证结果:验证集中20例患者的两组计划均被导入AcherQA软件中进行重新计算、分析。人工计划3 mm/3%、2 mm/2%的γ通过率分别为(99.89±0.11)%、(98.6±0.85)%,RapidPlan计划3 mm/3%、2 mm/2%的γ通过率分别为(99.87±0.07)%、(98.41±0.57)%。两组计划的平均γ通过率均高于98%,差异无统计学意义(P>0.05),但RapidPlan组计划数据离散程度低。
两组计划的Portal Dosimetry面剂量验证结果为人工计划2 mm/2%、1 mm/1%的γ通过率分别为(99.71±0.14)%、(88.22±1.81)%,RapidPlan计划2 mm/2%、1 mm/1%的γ通过率分别为(99.66± 0.26)%、(89.48±1.09)%。
RapidPlan计划组中平均总MU值为(687.46±56.27),明显小于人工计划组的(815.34±96.85),差异具有统计学意义(t=6.09,P < 0.05)。20例人工计划的MU值相较于RapidPlan计划明显波动更大,这是由于人工计划由不同设计者设计,人为因素的引入对计划质量干扰大,导致计划均质性低,RapidPlan可以克服这一缺点。RapidPlan计划MU降低在机器实际执行中效率更高、治疗时间减少,可改善患者的治疗体验。
讨论Halcyon 2.0加速器作为环形加速器由于其独特设计等原因,在计划质量和执行效率方面相较C型臂加速器有优势,因此对于该加速器单独进行RapidPlan建模是有必要的。
本研究表明,基于Halcyon 2.0平台的RapidPlan预测模型产生的自动计划可以实现与人工调试计划媲美的剂量分布,其中一个原因是RapidPlan通过剂量预测区间下限生成线函数,将优化目标从人工设置的点变成线,这是人工计划中无法实现的优化方式。同时,人工计划只能依靠设计者的经验,而RapidPlan模型可以根据先验知识提供每一个OAR可能的DVH范围,这很大程度上避免了人工试错的主观性,使计划的匀质性得到提高。
一般来说,更优质的计划往往伴随着计划复杂程度的增加,而计划复杂性增加可能降低实际治疗时剂量传输的准确性[19]。在人工计划中,为了实现临床计划目标,需要根据患者的靶区和OAR的关系进行反复试错,而此过程中则会产生潜在的优化目标冲突。RapidPlan模型生成的“线优化”条件则根据靶区和危及器官的关系,进行预测并尽量减少了优化目标间的冲突,而目标函数设置之间的潜在冲突会导致优化算法需要更多小的不规则的子野进行调制来满足优化条件,导致MLC叶片到位精度偏差增加。在计划验证中,更复杂的计划往往通过率较低。从以上研究可以看到,RapidPlan自动计划在1mm/1%偏差下,γ通过率更高,且MU值明显减少,说明自动计划在不影响计划质量的情况下可以适当降低计划的复杂程度,这也是下一步需要研究的问题。
在本研究中,为了提高模型的临床可用度,在模型的建立中,导入RapidPlan模型的临床计划均由资深物理师制作,保证每一个计划的质量。在模型初步建立之后,在保证训练库计划数量足够的基础上,对其中存在多个结构参数超出阈值的计划进行删减或修改,进一步优化模型。
在模型的使用过程中,也有一些需要调试的地方。在计划优化过程中,为了排除人为因素的干扰,使用了自动收敛模式,保证了一定的迭代次数,不添加任何人工调参,整体计划优化时间减少,计划间的一致性提高。
综上,基于Halcyon 2.0系统的RapidPlan模块能够实现临床可用的宫颈癌VMAT计划,而且使计划设计更加标准化、均质化,降低了优化耗时,提高了临床效率。
| [1] |
Arsene-Henry A, Fourquet A, Kirova YM. Evolution of radiation techniques in the treatment of breast cancer (BC) patients: From 3D conformal radiotherapy (3D CRT) to intensity-modulated RT (IMRT) using helical tomotherapy (HT)[J]. Radiother Oncol, 2017, 124(2): 333-334. DOI:10.1016/j.radonc.2017.07.002 |
| [2] |
Nakamura K, Okuhata K, Tamura M, et al. An updating approach for knowledge-based planning models to improve plan quality and variability in volumetric-modulated arc therapy for prostate cancer[J]. J Appl Clin Med Phys, 2021, 22(9): 113-122. DOI:10.1002/acm2.13353 |
| [3] |
Marrazzo L, Meattini I, Arilli C, et al. Auto-planning for VMAT accelerated partial breast irradiation[J]. Radiother Oncol, 2019, 132: 85-92. DOI:10.1016/j.radonc.2018.11.006 |
| [4] |
Ge Y, Wu QJ. Knowledge-based planning for intensity-modulated radiation therapy: a review of data-driven approaches[J]. Med Phys, 2019, 46: 2760-2775. DOI:10.1002/mp.13526 |
| [5] |
Hirashima H, Nakamura M, Mukumoto N, et al. Reducing variability among treatment machines using knowledge-based planning for head and neck, pancreatic, and rectal cancer[J]. J Appl Clin Med Phys, 2021, 22(7): 245-254. DOI:10.1002/acm2.13316 |
| [6] |
Masi K, Archer P, Jackson W, et al. Knowledge-based treatment planning and its potential role in the transition between treatment planning systems[J]. Med Dosim, 2018, 43(3): 251-257. DOI:10.1016/j.meddos.2017.10.001 |
| [7] |
Tol J, Dahele M, Delaney A, et al. Can knowledge-based DVH predictions be used for automated, individualized quality assurance of radiotherapy treatment plans?[J]. Radiother Oncol, 2015, 10: 234. DOI:10.1186/s13014-015-0542-1 |
| [8] |
Fogliata A, Reggiori G, Stravato A, et al. RapidPlan head and neck model: the objectives and possible clinical benefit[J]. Radiat Oncol, 2017, 12(1): 73. DOI:10.1186/s13014-017-0808-x |
| [9] |
Fogliata A, Nicolini G, Bourgier C, et al. Performance of a knowledge-based model for optimization of volumetric modulated arc therapy plans for single and bilateral breast irradiation[J]. PLoS One, 2015, 10(12): e0145137. DOI:10.1371/journal.pone.0145137 |
| [10] |
Visak J, McGarry RC, Randall ME, et al. Development and clinical validation of a robust knowledge-based planning model for stereotactic body radiotherapy treatment of centrally located lung tumors[J]. J Appl Clin Med Phys, 2021, 22(1): 146-155. DOI:10.1002/acm2.13120 |
| [11] |
Huang Y, Li S, Yue H, et al. Impact of nominal photon energies on normal tissue sparing in knowledge-based radiotherapy treatment planning for rectal cancer patients[J]. PLoS One, 2019, 14(3): e0213271. DOI:10.1371/journal.pone.0213271 |
| [12] |
Cozzi L, Fogliata A, Thompson S, et al. Critical appraisal of the treatment planning performance of volumetric modulated arc therapy by means of a dual layer stacked multileaf collimator for head and neck, breast, and prostate[J]. Technol Cancer Res Treat, 2018, 17: 1533033818803882. DOI:10.1177/1533033818803882 |
| [13] |
杨波, 汪之群, 李文博, 等. 新型"环形"机架加速器在宫颈癌术后盆腔放疗的临床应用研究[J]. 中国医疗设备, 2021, 36(4): 24-29. DOI:10.3969/j.issn.1674-1633.2021.04.007 |
| [14] |
Subramaniam S, Thirumalaiswamy S, Srinivas C, et al. Chest wall radiotherapy with volumetric modulated arcs and the potential role of flattening filter free photon beams[J]. Strahlenther Onkol, 2012, 188(6): 484-490. DOI:10.1007/s00066-012-0075-6 |
| [15] |
International Commission on Radiation Units and Measurements. Prescribing, recording, and reporting photon beam therapy[R]. ICRU Report No. 50. Bethesda: ICRU, 1993. DOI: 10.1093/jicru/os26.1.report50.
|
| [16] |
International Commission on Radiation Units and Measurements. Prescribing, recording, and reporting photon beam therapy[R]. ICRU Report No. 62. Bethesda: ICRU, 1999. DOI: 10.1259/bjr.74.879.740294.
|
| [17] |
Delaney A, Tol J, Dahele M, et al. Effect of dosimetric outliers on the performance of a commercial knowledge-based planning solution[J]. Int J Radiat Oncol Biol Phys, 2016, 94: 469-477. DOI:10.1016/j.ijrobp.2015.11.011 |
| [18] |
Wall PDH, Fontenot JD. Evaluation of complexity and deliverability of prostate cancer treatment plans designed with a knowledge-based VMAT planning technique[J]. J Appl Clin Med Phys, 2020, 21(1): 69-77. DOI:10.1002/acm2.12790 |
| [19] |
Craft D, Suss P, Bortfeld T. The tradeoff between treatment plan quality and required number of monitor units in intensity‐modulated radiotherapy[J]. Int J Radiat Oncol Biol Phys, 2007, 67(5): 1596-1605. DOI:10.1016/j.ijrobp.2006.11.034 |
 2022, Vol. 42
2022, Vol. 42


