2. 瓦里安医疗系统公司, 北京 100176
2. Varian Medical Systems, Beijing 100176, China
立体定向放疗是大剂量,少分次的放射治疗,对非小细胞肺癌等效果良好[1-2],但在执行过程中由于器官运动导致的剂量偏差,成为最大的挑战。美国医学物理师协会(AAPM)TG101报告[3]和TG76报告[4]报道了立体定向放疗中肿瘤随呼吸运动的管理方法,包括基于4DCT扫描得到患者运动靶区(ITV),基于患者某个呼吸时相或振幅的门控放疗,以及基于屏气的放疗等。美国瓦里安公司实时位置监测系统(RPM)是利用放置在体外的红外反射模块来间接监测患者的呼吸状态,此装置可以与瓦里安加速器联动,发出触发信号来控制加速器束流开始或停止;同时,RPM配套软件还具备呼吸预测功能,来评价患者的呼吸状态改变是否超出了设定阈值,从而保证患者治疗与模拟定位时呼吸状态的相对一致性[5]。由于患者在治疗过程中,存在因紧张、治疗时间太长或其他因素导致的分次治疗间或分次治疗内出现呼吸状态的改变,进而增加束流剂量的不确定性风险。但国内分析呼吸状态改变对RPM自由呼吸门控下立体定向放疗影响的相关研究少见报道,本研究尝试应用自行研制简单运动模体研究和评价此影响,进而为临床治疗提供参考。
材料与方法1. 简单运动模体的研制:利用可一维前后方向周期性运动、振幅为0~1 cm的瓦里安公司培训演示装置,加装带刻度手动垂直升降平台,直流电机调速器和一个定时器。使装置具备前后方向±2 cm垂直运动和运动周期(10~20次/min)连续可调功能,从而模拟患者基线漂移,呼吸频率改变。通过定时器预设的中断时间停止给运动模体供电,使模体停留在中断前状态来模拟呼气末和吸气末延时。通过随机模体运动起始位置、中断位置和中断时间来模拟患者的无规律呼吸。用PP塑料加工带防水套0.6 cm3电离室测量孔的模体,模体物理厚度2 cm。模体主要元素为C、H、O,满足电子平衡,CT值10次重复测量结果为(-126.20±3.55)HU。将测量模体,RPM红外反射模块和ISO Cube模体(美国Varian公司)加载到运动装置当中保持位置固定并随装置同步运动。至此构建了模拟肿瘤前后一维位移与RPM振幅正相关的简单运动模体。
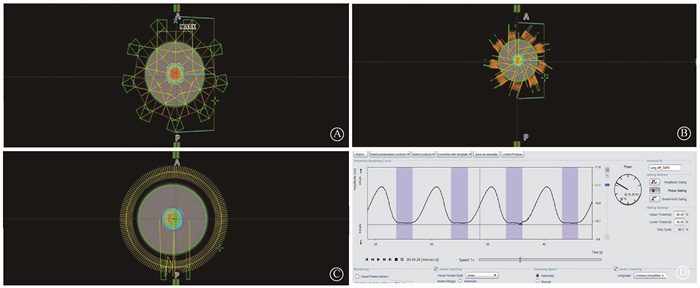
2. 4DCT扫描、计划设计和测量原理:将运动模体运动位置调整至呼气末最低振幅位置,放至美国GE公司16排CT床面,用水平尺调整水平,激光灯摆位,插入0.6 cm3 Farmer电离室(德国PTW公司),静止状态采集位置验证和剂量刻度用图像CT1。打开运动装置电源和定时器,运动模体以成人正常平静呼吸13次/min频率,标准正弦曲线垂直上下运动。RPM获取呼吸曲线,4DCT模式回顾式薄层扫描,10个呼吸时相CT重建后传输至美国瓦里安公司Eclipse15.5放疗计划系统(TPS)。在TPS中选择最稳定的呼气末(Phase 30%~60%)时相作为门控治疗窗,并在选定的每个呼吸时相图像中勾画电离室空腔,合并生成大体肿瘤体积(GTV)。GTV均匀外扩5 mm生成计划靶区(PTV),体积为7.2 cm3。在30%~60%呼吸时相生成的平均图像上根据立体定向放疗(SBRT)计划剂量学要求设计3种计划[3, 6]:9野均分三维适形计划(A);9野均分固定野动态调强计划(B);单弧旋转调强计划(C)。所有计划处方剂量为95% PTV体积达到10 Gy,采用非均整(FFF)模式,跳数1 400 MU/min,单次执行。图 1为3组计划射野设计和剂量分布情况,3组计划在TPS计算得出的GTV平均剂量分别为1 135.1、1 172.3、1 178.9 cGy。3组计划都基于30%~60%呼吸时相门控在VitalBeam加速器(美国Varian公司)上执行治疗,RPM Breathing Predictive Filter值为默认的20%。因为ISO Cube模体是随运动装置同步前后方向运动,且有唯一中心小球,所以用90°kV门控触发拍片准确测量ISO Cube模体中心小球与等中心前后方向垂直距离(L),间接评价门控触发治疗时,GTV与加速器等中心相对位置的正确性,门控计划中L值为4.75 cm。
|
图 1 3组计划射野设计、剂量分布和门控时项设置情况 A.三维适形;B.固定野动态调强;C.单弧旋转调强;D.计划和执行时门控时项设置 Figure 1 Field arrangement, dose distribution, and phase-based gating settings of three plans A. Three dimensional conformal radiotherapy; B. Intensity modulated radiotherapy; C. Volumetric modulated arc therapy; D. Phase-based gating settings used in plan and therapy |
3. 剂量刻度和摆位验证: 加速器质量保证和绝对剂量标定校准后,参考文献[7]方法对模体进行剂量刻度。首先在CT1中勾画电离室空腔体积(GTV1),并生成锥形束CT(CBCT)配准和剂量刻度用计划Plan1(90°和270°两个方向三维适形对穿静态射野,射野大小10 cm × 10 cm,FFF模式,1 400 MU/min,200 MU),TPS计算得出GTV1平均剂量为192.4 cGy。其次将运动模体运动位置调整至呼气末最低振幅位置,放置加速器床面,静止状态采集CBCT,重复6次测量摆位误差,并进行位置修正。最后执行6次Plan1计划,记录温度气压校准后电离室读数为(197.90±0.11)cGy,计算得出校准系数等于0.972(TPS计算GTV1平均剂量/电离室6次测量剂量均值)。将Plan1计划中射野大小分别更改为5 cm × 5 cm、4 cm × 4 cm、2 cm × 4 cm、3 cm × 3 cm、2 cm × 3 cm、2 cm × 2 cm,验证TPS计算与测量剂量的一致性,重复测量5次。
4. 正常呼吸曲线下重复测量评价实验装置正确性和稳定性: 运动模体静止状态摆位,CBCT位置校正后。打开运动装置电源和定时器,使模体运行4DCT时一致的运动频率和振幅。分别载入设计的3组计划, 计划执行前90°拍摄门控kV数字摄影图像,记录L值;计划执行,记录校正系数校正后电离室读数;重复执行5次。均值差异反映测量值与TPS计算值的系统误差大小,标准差大小反映3种计划下模体整体不稳定性。
5. 呼吸状态改变模拟与测量: 运动模体静止状态摆位,CBCT位置校正后。模体先运行与4DCT时一致的运动频率和振幅,标准正弦曲线前后运动。RPM学习完成后,分别调节基线偏移1、2、5、6、8、10和15 mm;改变呼吸频率为20、15、11和10次/min;设置呼气末延时1、2、3 s;吸气末延时1、2、3 s;以及不规则呼吸。测量各模拟状态下3组计划电离室受照剂量值(Dose)和L值。分析各情况与Dose和L的相关性,以及是否超出摆位误差阈值(5 mm)对受照剂量的影响。
6. 统计学处理:应用SPSS 16.0统计软件进行分析,计量资料符合正态分布,用x±s表示,两变量间的相关性采用Bivariate Correlation过程的Spearman分析,两相关样本的比较应用Wilcoxon符号秩检验,应用Kruskal-Wallis H检验的多个独立样本的秩和检验。P < 0.05为差异有统计学意义。
结果1. 验证模体摆位重复性和TPS与测量剂量一致性:运动模体6次摆位,CBCT配准后误差前后平移(0.01±0.19)cm,头脚平移(-0.01±0.03)cm,左右平移(-0.02±0.03)cm,床旋转(-0.10±0.30)°,进出倾斜(-0.07±0.23)°,左右转动(-0.17±0.08)°,6维摆位误差较小,满足测试要求。5 cm × 5 cm、4 cm × 4 cm、2 cm × 4 cm、3 cm × 3 cm、2 cm × 3 cm、2 cm × 2 cm射野下5次重复测量,TPS计算与测量剂量均值差异分别为0.15%、0.35%、0.55%、0.13%、0.16%、-1.59%,除2 cm × 2 cm射野外,其他误差均 < 1%。
2. 正常呼吸曲线下重复测量评价装置正确性和稳定性:5次重复测量3组计划结果见表 1。3组计划电离室测量均值与TPS误差在2%内, 3组计划重复测量标准差为0,3组计划执行的稳定性良好。
|
|
表 1 正常呼吸曲线下3组计划重复测量结果(cGy, x±s) Table 1 Repeated measurement results of three plans under normal respiratory curves (cGy, x±s) |
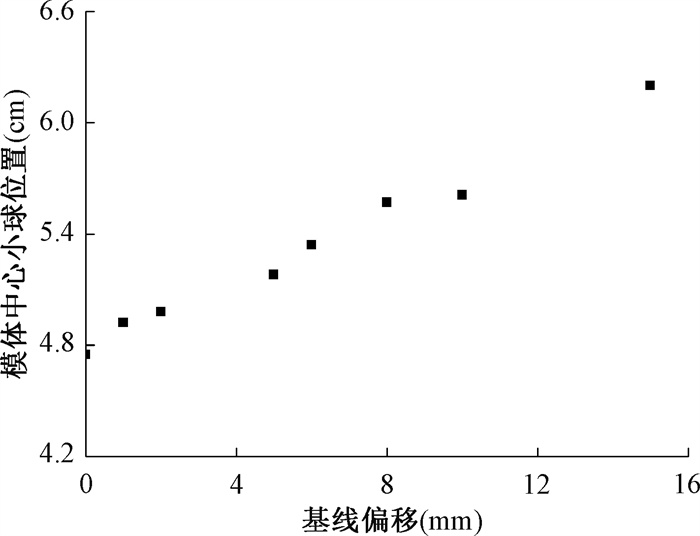
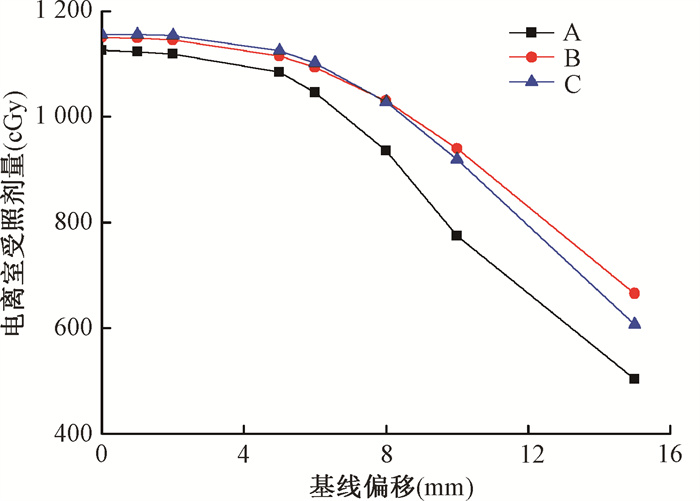
3. 基线偏移与模体中心小球和受照剂量的相关性:基线发生偏移,3组计划都能继续执行。从图 2可以看出L与基线偏移呈现正相关(r=0.99, P < 0.01)。图 3为各基线偏移下运动模体执行3组计划电离室测量结果, 从结果可以看出偏移在5 mm摆位误差范围内时3组计划Dose变化在4%以内,相对较小;超出5 mm后随着偏移增大,Dose快速下降呈现负相关(r=-0.95, P < 0.01);误差超出5 mm阈值与否对Dose差异有统计学意义(Z=-3.059, P < 0.01)。3组计划受基线偏移的影响率差异无统计学意义(P>0.05)。
|
图 2 基线不同偏移量模体中心小球位置测量值 Figure 2 Measured position of the ball at the phantom center under different baseline shifts |
|
注:A. 三维适形计划;B.固定野动态调强计划;C.单弧旋转调强计划 图 3 3组计划随基线不同偏移量电离室剂量测量值 Figure 3 Measured dose in the ionization chamber of the three plans varying with baseline shift |
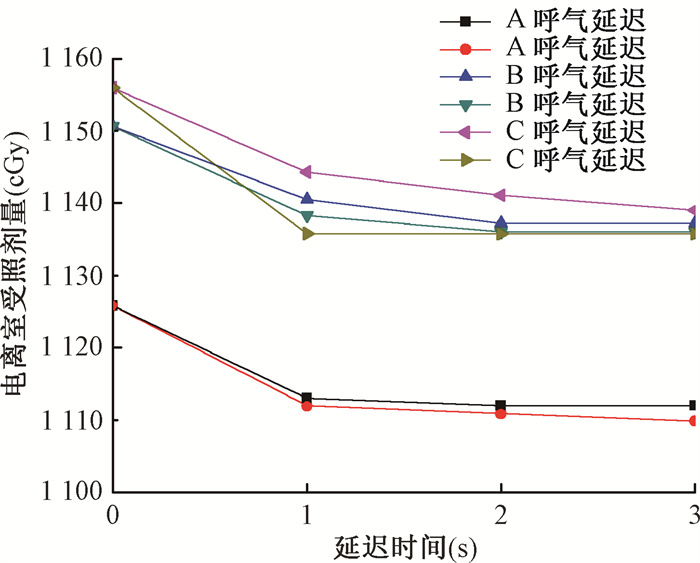
4. 呼吸频率、波形改变与受照剂量的相关性:频率改变对受照剂量的影响最大误差只有0.78%,影响较小,3组计划剂量受频率影响率差异无统计学意义(P>0.05)。波形改变导致3组计划Dose不同程度下降如图 4所示,最大误差达到-1.74%;并且吸气末延迟相对呼气末延迟影响更大(Z=-2.678, P < 0.01);不同延迟时间对受照剂量的影响没有发现明显的相关性(P>0.05)。3组计划受波形改变的影响率差异无统计学意义(P>0.05)。
|
注:A. 三维适形计划;B.固定野动态调强计划;C.单弧旋转调强计划 图 4 3种计划呼气、吸气延迟电离室剂量测量值 Figure 4 Measured dose in the ionization chamber of the three plans under end-expiratory and end-inspiratory delay |
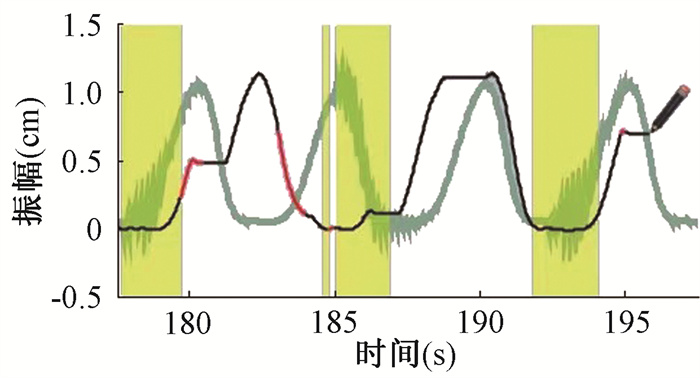
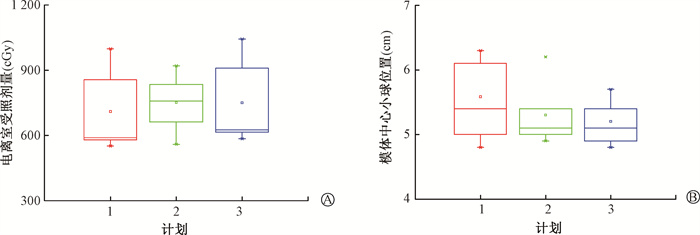
5. 不规则呼吸对模体中心小球位置和受照剂量影响:图 5为模体产生不规则波形后的照射过程,加速器还能继续出束治疗,但可以看出出束窗并不一直在模体运动的最低点呼气末位置。图 6为3组计划重复测量6次L和剂量统计箱图,3D-CRT、IMRT、VMAT在不规则呼吸下电离室受照剂量分别为(709.68±180.00)、(751.40±127.16)和(750.00±185.60)cGy,从中可以看出Dose均小于处方剂量,并且一致性欠佳。
|
注:黑色曲线为不规则呼吸曲线;绿色曲线为标准呼吸曲线;黄色部分为加速器出束的时间窗 图 5 不规则呼吸照射过程 Figure 5 Irradiation under irregular breathing |
|
注:1. 三维适形计划;2.固定野动态调强计划;3.单弧旋转调强计划 图 6 3组计划6次重复测量不规则呼吸下电离室受照剂量(A)和模体中心小球位置(B)情况 Figure 6 The dose in the ionization chamber(A) and the position of the ball at the phantom center(B) of the three plans under irregular breathing from six repeated measurements |
讨论
本研究建立了一个可以模拟各种呼吸状态改变的简单运动测量模体,摆位重复性和测量稳定性都能满足临床要求。测量模体利用Farmer电离室空腔模拟肿瘤,体积较小,如果测量模拟肿瘤内空间某点的绝对剂量属于小野剂量范畴,可能导致测量的不确定性增加[8]。但本研究中并非研究肿瘤体积内一点的绝对剂量,而只是分析各呼吸状态改变与标准呼吸状态下GTV受照平均剂量的一致性差异,并且此设计可以敏感测量呼吸门控触发变化导致的剂量差异。因此认为应用构建的测量模体来比较呼吸状态改变后的受照剂量一致性差异是可行的。
经过剂量刻度后,正常呼吸曲线下重复测量与TPS计算剂量偏差在2%以内。3组计划测量标准差都为0,说明此运动模体在各种治疗方式中整体稳定性良好,并未观察到运动靶区移动和多叶准直器运动间的相互影响效应和1 400 cGy/min高剂量率等对测量稳定性整体造成影响[9-11]。因为科室没有胶片剂量分析设备,导致此模体只测量和验证了各呼吸状态改变下GTV的平均剂量和门控触发位置的一致性变化,并没有运用胶片对研究结果和平面剂量进行测量和分析,此模体只能模拟单因素影响下的改变,没能模拟混合多因素或患者实际呼吸曲线情况,同时多篇文献曾报道RPM触发信号与kV拍片和MV出束间都存在延迟误差,本实验中忽略了此延迟误差的影响[12-14]。
本研究实验结果可以得出当患者治疗过程中RPM基线偏移值超出计划设计摆位误差值时会导致受照剂量显著下降,这时应该停止治疗,查找偏移原因。Tachibana等[15]报道baseline偏移的原因可能有患者体位改变和呼吸改变两种情况,单纯生物反馈无法分辨偏移的真实原因可能导致错误深呼吸,同时不建议重新学习呼吸曲线,这将掩盖这一基线偏移现象。
3组计划除标准呼吸频率剂量偏小,其他频率剂量一致性较好,这可能是因为测量正常呼吸频率和改变呼吸频率时间不一致,加速器束流微小偏差导致的。呼吸波形的改变会导致受照剂量下降,吸气末时间延迟导致的误差较呼气末延迟增大,这提示呼吸波形变异越大对剂量的影响越大,与Cai等[16]报道的一致。有文献报道通过视频和音频训练可以减小患者治疗时的振幅频率改变和不规则呼吸从而减小内肿瘤靶区(ITV)[17-19],因此治疗前训练患者有规律周期性呼吸还是十分必要的。
综上所述,患者呼吸状态改变会导致剂量下降。基线偏移超出摆位误差阈值或者波形变异较大,且出现不规则呼吸时更甚,且与放疗技术不相关。治疗技师在治疗过程中应该打开患者参考呼吸曲线,当患者出现基线偏移超摆位误差外扩值或无规律不规则呼吸时需要中止治疗,直到患者回归到规则呼吸,并通过kV门控触发摄片确认靶区在PTV范围内再继续治疗。
利益冲突 无
作者贡献声明 郭海亮负责数据整理分析和论文撰写; 李珊、唐春波负责模型设计; 王兴柳、张震负责实验数据采集; 袁军负责整体规划和行政支持
| [1] |
Chang JY, Senan S, Paul MA, et al. Stereotactic ablative radiotherapy versus lobectomy for operable stage I non-small-cell lung cancer: a pooled analysis of two randomised trials[J]. Lancet Oncol, 2015, 16(6): 630-637. DOI:10.1016/S1470-2045(15)70168-3 |
| [2] |
Kann BH, Verma V, Stahl JM, et al. Multi-institutional analysis of stereotactic body radiation therapy for operable early-stage non-small cell lung carcinoma[J]. Radiother Oncol, 2019, 134: 44-49. DOI:10.1016/j.radonc.2019.01.027 |
| [3] |
Benedict SH, Yenice KM, Followill D, et al. Stereotactic body radiation therapy: The report of AAPM Task Group 101[J]. Med Phys, 2010, 37(8): 4078-4101. DOI:10.1118/1.3438081 |
| [4] |
Kissick MW, Mackie TR. Task Group 76 Report on 'The management of respiratory motion in radiation oncology'[Med Phys, 33, 3874-3900(2006)][J]. Med Phys, 2009, 36(12): 5721-5722. DOI:10.1118/1.3260838 |
| [5] |
Varian Medical Systems, Inc. RPM respiratory fating system reference guide[R]. Calfornia: Varian Medical Systems, 2012.
|
| [6] |
Bezhak A, Bradley J, Gaspar L, et al. Radiation Therapy Oncology Group 0813. Seamless phase I/II study of stereotactic lung radiotherapy (SBRT) for early stage, centrally located, non-small cell lung cancer (NSCLC) in medically inoperable patients [R]. Philadelphia: Radiation Therapy Oncology Group, 2015.
|
| [7] |
Hill NL. Dosimetric verification of respiratory-gated radiation therapy using a dynamic phantom for commissioning the varian real-time position management system[D]. Toledo: University of Toledo Health Science Campus, 2013.
|
| [8] |
Palmans H, Andreo P, Huq MS, et al. Dosimetry of small static fields used in external photon beam radiotherapy: Summary of TRS-483, the IAEA-AAPM international code of practice for reference and relative dose determination[J]. Med Phys, 2018, 45(11): e1123-e1145. DOI:10.1002/mp.13208 |
| [9] |
Ong CL, Dahele M, Slotman BJ, et al. Dosimetric impact of the interplay effect during stereotactic lung radiation therapy delivery using flattening filter-free beams and volumetric modulated arc therapy[J]. Int J Radiat Oncol Biol Phys, 2013, 86(4): 743-748. DOI:10.1016/j.ijrobp.2013.03.038 |
| [10] |
Riley C, Yang Y, Li T, et al. Dosimetric evaluation of the interplay effect in respiratory-gated RapidArc radiation therapy[J]. Med Phys, 2014, 41(1): 011715. DOI:10.1118/1.4855956 |
| [11] |
Fernandez DJ, Sick JT, Fontenot JD. Interplay effects in highly modulated stereotactic body radiation therapy lung cases treated with volumetric modulated arc therapy[J]. J Appl Clin Med Phys, 2020, 21(11): 58-69. DOI:10.1002/acm2.13028 |
| [12] |
King RB, Agnew CE, O'Connell BF, et al. Time-resolved dosimetric verification of respiratory-gated radiotherapy exposures using a high-resolution 2D ionisation chamber array[J]. Phys Med Biol, 2016, 61(15): 5529-5546. DOI:10.1088/0031-9155/61/15/5529 |
| [13] |
Chugh BP, Quirk S, Conroy L, et al. Measurement of time delays in gated radiotherapy for realistic respiratory motions[J]. Med Phys, 2014, 41(9): 091702. DOI:10.1118/1.4890604 |
| [14] |
Smith WL, Becker N. Time delays and margins in gated radiotherapy[J]. J Appl Clin Med Phys, 2009, 10(3): 140-154. DOI:10.1120/jacmp.v10i3.2896 |
| [15] |
Tachibana H, Kitamura N, Ito Y, et al. Management of the baseline shift using a new and simple method for respiratory-gated radiation therapy: detectability and effectiveness of a flexible monitoring system[J]. Med Phys, 2011, 38(7): 3971-3980. DOI:10.1118/1.3598434 |
| [16] |
Cai J, McLawhorn R, Read PW, et al. Effects of breathing variation on gating window internal target volume in respiratory gated radiation therapy[J]. Med Phys, 2010, 37(8): 3927-3934. DOI:10.1118/1.3457329 |
| [17] |
Neicu T, Berbeco R, Wolfgang J, et al. Synchronized moving aperture radiation therapy (SMART): improvement of breathing pattern reproducibility using respiratory coaching[J]. Phys Med Biol, 2006, 51(3): 617-636. DOI:10.1088/0031-9155/51/3/010 |
| [18] |
Kini VR, Vedam SS, Keall PJ, et al. Patient training in respiratory-gated radiotherapy[J]. Med Dosim, 2003, 28(1): 7-11. DOI:10.1016/S0958-3947(2)00136-X |
| [19] |
George R, Chung TD, Vedam SS, et al. Audio-visual biofeedback for respiratory-gated radiotherapy: impact of audio instruction and audio-visual biofeedback on respiratory-gated radiotherapy[J]. Int J Radiat Oncol Biol Phys, 2006, 65(3): 924-933. DOI:10.1016/j.ijrobp.2006.02.035 |
 2022, Vol. 42
2022, Vol. 42


