颞骨放射性骨坏死(osteoradionecrosis, ORN)是头颈部恶性肿瘤放疗后最严重的耳部并发症,以外耳道甚至乳突/鼓室骨质暴露、感染及坏死为主要特征。颞骨ORN分为局限型(仅累及外耳道)与广泛型(累及乳突、中耳及内耳),以前者占绝大多数[1-2]。目前,临床上多采用保守的治疗方案处理局限型颞骨ORN,包括耳内镜下定期清理坏死骨组织及分泌物、局部或全身使用抗生素/激素、高压氧等,然而仍然有超过20%的患者对于上述治疗无反应甚至持续进展,最终接受颞骨切除的手术治疗[3-4]。
PENTOCLO方案是指联合使用己酮可可碱(pentoxifylline)、维生素E(tocopherol)、氯膦酸盐(clodronate)3种药物,发挥抗氧化、抗纤维化及抑制炎症的药理作用。临床试验已证实PENTOCLO方案可明显改善下颌骨ORN患者的症状,促进骨质和皮肤愈合[5]。近年来,散在的病例报告提示PENTOCLO方案对颞骨ORN也具有显著的疗效[6-7]。本研究观察单个中心应用PENTOCLO方案治疗局限型颞骨ORN的疗效,为该方案的广泛应用提供临床数据。
资料与方法1. 研究对象:回顾性分析2020年11月至2021年4月期间在中山大学孙逸仙纪念医院诊断为颞骨ORN并接受PENTOCLO方案治疗的患者资料。入选标准:头颈部恶性肿瘤接受过放疗的患者;耳内镜下见外耳道有明显的骨质裸露,但乳突气房未暴露,鼓膜完整;患耳反复疼痛、流脓;接受过全身或局部抗生素应用、耳内镜处理和(或)高压氧治疗6个月以上症状无明显改善;年龄>18岁。排除标准:原发肿瘤复发患者;广泛型颞骨ORN;严重肝脏或肾脏功能不全;对PENTOCLO方案中单种或多种药物有过敏史。本研究通过中山大学孙逸仙纪念医院伦理委员会审核(审批号:SYSKY-2022-285-01)。
2. 治疗方案:患者首先接受2周抑菌、抗渗出治疗。口服药物方案:阿莫西林/克拉维酸钾400 mg/57 mg,2次/d;左氧氟沙星500 mg,1次/d;氟康唑50 mg,1次/d;波尼松20 mg,1次/d。随后患者接受至少1年的PENTOCLO方案治疗:己酮可可碱400 mg,2次/d,周一至周五;维生素E,100 mg,2次/d,周一至周五;氯膦酸二钠,800 mg,2次/d,周一至周五。剩余2 d继续使用左氧氟沙星500 mg,1次/d;波尼松20 mg,1次/d [6]。患者不定期到门诊复查耳内镜。若患耳外耳道暴露骨质明显高于周围组织,则在耳内镜下刮除凸起骨质。所有患者均在首次就诊时取外耳道分泌物进行细菌培养。
3. 疗效评价:耳痛及耳流脓改善程度由患者主观评价:痊愈(完全消失);好转(较用药前明显减轻);无效(较用药前无改善或恶化)。骨坏死改善程度根据耳内镜结果由同一位耳科医生进行评价:痊愈(皮肤完全覆盖);好转(骨质裸露范围明显减小);稳定(骨质裸露范围无明显改变);进展(骨质裸露范围明显扩大)。最后一次随访时(2022年6月)的症状及体征作为疗效的评价依据。
4. 统计学处理:采用SPSS 19.0软件进行统计学分析,定量数据经正态性检验符合正态分布,以x±s表示,组间比较采用独立样本t检验;定性数据以例数和百分比表示,组间比较采用χ2检验。P < 0.05为差异有统计学意义。
结果本研究总共纳入21名局限型颞骨ORN患者(23侧患耳),其中男13例,女8例;平均年龄(57±11)岁,临床特征见表 1。
|
|
表 1 21例颞骨放射性骨坏死患者的临床资料 Table 1 Characteristics of 21 patients with temporal bone osteoradionecrosis |
本研究中大部分患者对PENTOCLO方案耐受良好,仅有2例出现一过性的头晕、腹泻症状,但均未中断方案。PENTOCLO方案的平均使用时间为(506±48)d。16/23侧患耳(73.9%)在接受治疗1周内耳痛及耳流脓症状明显缓解。在最后一次随访时,19/23侧患耳(82.6%)的耳痛、耳流脓症状完全消失,获得痊愈;2/23侧患耳(8.7%)的症状好转;2/23侧患耳(8.7%)的症状无明显改善。9/23侧患耳(39.1%)的外耳道裸露骨质已完全被皮肤覆盖,获得痊愈;11/23侧患耳(47.8%)骨质裸露范围明显减小;3/23侧患耳(13.0%)骨坏死程度稳定;无患耳病变进展。典型病例治疗前后的耳内镜表现见图 1。性别、患耳侧别、既往治疗方式对PENTOCLO方案的疗效无明显影响(P>0.05)。
|
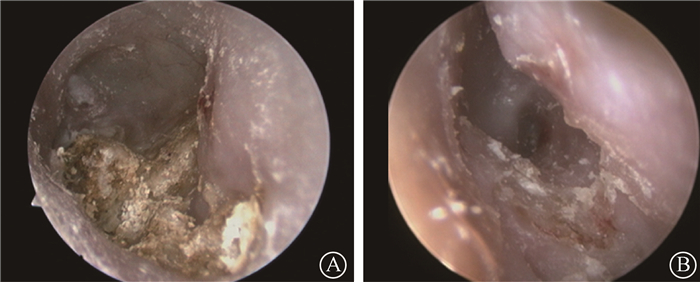
图 1 1例局限型颞骨ORN患者在接受PENTOCLO方案治疗前后的耳内镜图片 A. 治疗前;B. 治疗后14个月 Figure 1 Endoscopic images of the external auditory canal of a patient with localized temporal bone osteoradionecrosis before and after the treatment with PENTOCLO protocol A. Before the treatment; B. 14 months after the treatment |
讨论
目前认为ORN的发生是由于放疗对组织的直接损伤致使辐射组织内出现低氧、低血供及大量自由基的产生,进而造成骨组织纤维化及功能障碍,最终导致骨坏死并多继发感染[8-10]。颞骨ORN多在放疗后8~10年后逐渐出现,发生率约8.5%,临床表现为反复发作的耳流脓、耳痛及听力下降,严重影响患者的生活质量[11-12]。国际上尚无公认的颞骨ORN标准治疗方案。尽管药物(抗生素、激素、止痛药)、耳内镜下局部清理及高压氧等保守治疗方式可以治愈大部分局限型颞骨ORN,但仍有部分病例对保守治疗无反应并持续进展[3]。一旦坏死骨范围扩展至乳突、鼓室、颞下颌关节,颞骨外侧切除将成为唯一有可能治愈ORN的方法,然而,患者需要入院接受全麻手术、切除坏死骨后遗留的巨大创面需要局部皮瓣修复、术后听力丧失等[12-15]。
鉴于ORN的主要病理特征之一是骨组织的纤维化,近年来抗纤维化成为ORN治疗的新靶点。国外学者在2002年首次报道应用己酮可可碱和维生素E治愈乳腺癌放疗后胸骨ORN的个案[16]。己酮可可碱能通过抑制TNF-α减轻炎症反应并提供胶原酶的活性,维生素E可清除氧自由基,两种药物协同具有显著的抗纤维化作用。此外,氯磷酸能减轻炎症反应,抑制破骨细胞活性,抑制成纤维细胞增殖[17]。前瞻性临床研究证实,联合使用己酮可可碱、维生素E和氯膦酸可以有效治愈下颌骨ORN[5, 18]。目前,PENTOCLO方案已成为早期下颌骨ORN的首选治疗方案[19]。ORN多继发感染,常见感染细菌为铜绿假单胞菌及金黄色葡萄球菌,有时也可伴发真菌感染。因此,在实施PENTOCLO方案前及过程中均需联用抗生素清除致病菌。
2015年首次报道应用PENTOCLO方案成功治愈1例局限型颞骨ORN患者[6]。随后,2020年报道联合使用己酮可可碱及维生素E治疗5例局限型颞骨ORN患者的经验,结果显示,4例患者的骨质暴露范围明显缩小,3例患者的症状明显减轻,1例患者进展至广泛型ORN[7],平均用药时间为300 d。本研究是国内首次报道PENTOCLO方案治疗局限型颞骨ORN的疗效,样本量也明显多于既往研究[6-7]。本研究中,绝大部分局限型颞骨ORN患者能够从PENTOCLO方案中明显获益,体现在超过80%的患耳症状完全消失,接近40%的患耳裸露骨质完全被皮肤覆盖,接近50%的患耳裸露骨质范围明显减小,治疗效果优于文献报道的常规保守治疗方案[3]。此外,PENTOCLO方案长期应用的安全性也在本研究中得到证实[19]。
本研究存在一定的局限性。首先,本项目是回顾性研究,部分临床信息缺失,比如放疗的剂量与分布不详;骨坏死的面积未进行量化;疼痛及耳流脓程度未进行数字评分量化。其次,患者不定期的随访使得无法对药物开始起效的时间以及过程进行详细评价。最后,本研究未包含常规治疗的对照组。但值得注意的是,本研究纳入的患者均经过至少6个月以上的普通药物(抗生素、激素)及高压氧治疗,因此患者的前期治疗效果可做为自身对照,从而在一定程度上可以对比PENTOCLO方案的疗效。未来的大样本、随机对照、多中心的临床试验将最终确认PENTOCLO方案治疗颞骨ORN的有效性。
综上所述,PENTOCLO方案治疗局限型颞骨ORN的效果显著,不良反应轻微,可以作为局限型颞骨ORN常规保守治疗无效的替代方案。
利益冲突 所有作者均声明不存在利益冲突
作者贡献声明 苏悦嘉、吴敏健、陈文负责研究设计、临床数据收集及分析;熊浩负责研究设计及文章撰写
| [1] |
Ramsden RT, Bulman CH, Lorigan BP. Osteoradionecrosis of the temporal bone[J]. J Laryngol Otol, 1975, 89(9): 941-955. DOI:10.1017/s0022215100081226 |
| [2] |
Lee EW, Jyung RW. Osteoradionecrosis of the temporal bone[J]. Ear Nose Throat J, 2015, 94(1): 18-19. DOI:10.1097/MAO.0000000000001925 |
| [3] |
Lovin BD, Hernandez M, Elms H, et al. Temporal bone osteoradionecrosis: an 18-year, single-institution experience[J]. Laryngoscope, 2021, 131(11): 2578-2585. DOI:10.1002/lary.29758 |
| [4] |
Kammeijer Q, van Spronsen E, Mirck PG, et al. Treatment outcomes of temporal bone osteoradionecrosis[J]. Otolaryngol Head Neck Surg, 2015, 152(4): 718-723. DOI:10.1177/0194599814564536 |
| [5] |
Delanian S, Chatel C, Porcher R, et al. Complete restoration of refractory mandibular osteoradionecrosis by prolonged treatment with a pentoxifylline-tocopherol-clodronate combination (PENTOCLO): a phase Ⅱ trial[J]. Int J Radiat Oncol Biol Phys, 2011, 80(3): 832-839. DOI:10.1016/j.ijrobp.2010.03.029 |
| [6] |
Glicksman JT, Khalili S, Fung K, et al. Pentoxifylline-tocopherol-clodronate combination: a novel treatment for osteoradionecrosis of the temporal bone[J]. Head Neck, 2015, 37(12): E191-193. DOI:10.1002/hed.24057 |
| [7] |
Lovin BD, Choi JS, Lindquist NR, et al. Pentoxifylline and tocopherol in the management of temporal bone osteoradionecrosis: a case series[J]. Otol Neuro, 2020, 41(10): 1438-1446. DOI:10.1097/MAO.0000000000002781 |
| [8] |
Marx RE. Osteoradionecrosis: a new concept of its pathophysiology[J]. J Oral Maxillofac Surg, 1983, 41(5): 283-288. DOI:10.1016/0278-2391(83)90294-x |
| [9] |
Meyer I. Infectious diseases of the jaws[J]. J Oral Surg, 1970, 28(1): 17-26. |
| [10] |
Delanian S, Lefaix JL. The radiation-induced fibroatrophic process: therapeutic perspective via the antioxidant pathway[J]. Radiother Oncol, 2004, 73(2): 119-131. DOI:10.1016/j.radonc.2004.08.021 |
| [11] |
Morrissey D, Grigg R. Incidence of osteoradionecrosis of the temporal bone[J]. ANZ J Surg, 2011, 81(12): 876-879. DOI:10.1111/j.1445-2197.2010.05641.x |
| [12] |
Yuhan BT, Nguyen BK, Svider PF, et al. Osteoradionecrosis of the temporal bone: an evidence-based approach[J]. Otol Neurotol, 2018, 39(9): 1172-1183. DOI:10.1097/MAO.0000000000001925 |
| [13] |
Kadakia S, Badhey A, Inman J, et al. Surgical management of temporal bone osteoradionecrosis: single surgeon experience of 47 cases[J]. Am J Otolaryngol, 2017, 38(6): 688-691. DOI:10.1016/j.amjoto.2017.07.005 |
| [14] |
Chen J, Lin F, Liu Z, et al. Pedicled temporalis muscle flap stuffing after a lateral temporal bone resection for treating mastoid osteoradionecrosis[J]. Otolaryngol Head Neck Surg, 2017, 156(4): 622-626. DOI:10.1177/0194599817690102 |
| [15] |
区永康, 许耀东, 郑亿庆, 等. 鼻咽癌放疗后颞骨骨坏死的手术治疗[J]. 中华医学杂志, 2007, 87(2): 121-123. Ou YK, Xu YD, Zheng YQ, et al. Surgical treatment of diffused osteoradionecrosis of temporal bone in cases with nasopharyngeal carcinoma after radiotherapy[J]. Nat Med J Chin, 2007, 87(2): 121-123. DOI:10.3760/j.issn.0376-2491.2007.02.013 |
| [16] |
Delanian S, Lefaix JL. Complete healing of severe osteoradionecrosis with treatment combining pentoxifylline, tocopherol and clodronate[J]. Br J Radiol, 2002, 75(893): 467-469. DOI:10.1259/bjr.75.893.750467 |
| [17] |
Diel IJ, Solomayer EF, Costa SD, et al. Reduction in new metastases in breast cancer with adjuvant clodronate treatment[J]. N Engl J Med, 1998, 339(6): 357-363. DOI:10.1056/NEJM199808063390601 |
| [18] |
Delanian S, Depondt J, Lefaix JL. Major healing of refractory mandible osteoradionecrosis after treatment combining pentoxifylline and tocopherol: a phase Ⅱ trial[J]. Head Neck, 2005, 27(2): 114-123. DOI:10.1002/hed.20121 |
| [19] |
Martos-Fernandez M, Saez-Barba M, Lopez-Lopez J, et al. Pentoxifylline, tocopherol, and clodronate for the treatment of mandibular osteoradionecrosis: a systematic review[J]. Oral Surg Oral Med Oral Pathol Oral Radiol Endod, 2018, 125(5): 431-439. DOI:10.1016/j.oooo.2018.02.004 |
 2022, Vol. 42
2022, Vol. 42


