2. 苏州大学附属第一医院放疗科, 苏州 215006
2. Department of Radiotherapy Oncology, First Affiliated Hospital of Soochow University, Suzhou 215006, China
光学体表成像(optical surface imaging,OSI)通过结构光测量或散斑投影等原理获取传感器和被测物体间的距离,以重现患者体表轮廓,因其具有耗时少、无辐射和非侵入等优势而成为放疗摆位研究中的热点[1-5]。然而,胸部肿瘤的运动与体表轮廓的运动并非完全一致[6],且在乳腺癌根治术后放疗(post-mastectomy radiation therapy,PMRT)中常在患者体表覆盖组织补偿膜以增大皮肤剂量[7],这可能会对OSI的体表检测造成困扰。因此,本研究以锥形束CT(cone beam CT,CBCT)为参考,验证OSI辅助PMRT放疗摆位的性能并探索基于3D打印的硅胶补偿膜对OSI的影响,为临床使用策略提供参考。
资料与方法1. 患者资料:回顾性选择2021年1月至2021年4月于四川大学华西医院行左侧PMRT的女性患者16例,年龄39~65岁,平均年龄52岁,均采用Synergy(瑞典医科达公司)医用直线加速器开展容积旋转调强放疗,且患者在全程放疗中使用OSI技术,上肢上举和外展功能良好,不阻挡OSI正常成像。患者体位固定均采用仰卧位真空垫,双手置于头顶并紧扣真空垫,患侧胸部覆盖补偿膜。研究共纳入389个有效放疗分次,其中6例患者(共143分次)使用3D打印硅胶补偿膜。
2. CBCT图像获取:采用120 kV,160 mAs的CT扫描参数,机架行逆时针扫描,角度范围为135°~310°,旋转速度3.33°/s,过滤板S 20,400帧。
3. OSI图像获取:使用Catalyst(瑞典C-RAD公司)获取OSI图像,图像配准的感兴趣区(region of interest,ROI)范围不包含腋窝、下颌和手臂。Catalyst等中心与加速器相同,扫描参数平均图像采集时长、单次曝光和图像增益分别设为8 s、5 ms和500%。
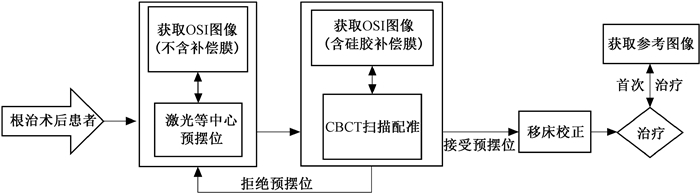
4. 图像数据采集流程:CBCT及OSI图像数据采集流程如图 1,在患者通过3点激光线进行预摆位后,获取无补偿膜时OSI检测的摆位误差(OSIno-bolus,以下简称OSIn),随后利用CBCT获取解剖信息,并使用自动灰度配准联合治疗师手动配准来获取CBCT摆位误差,若误差在临床可接受范围内,则在移床校正误差后开始治疗,若误差过大(平移>5 mm[8]或旋转>3°)则重新执行预摆位。其中,对使用基于3D打印技术的硅胶补偿膜的患者,同时获取含补偿膜的OSI图像,并通过后期离线配准得到相应的OSI摆位误差(OSIbolus,以下简称OSIb)。在本研究中,OSI检测所得摆位误差不作为临床摆位参考,且所有患者均于首次治疗中获取OSI参考图像,这比通过计划系统重建获得的参考图像更为可靠[9]。
|
图 1 图像采集流程 Figure 1 Image acquisition process |
5. OSI摆位误差分析:在OSI与CBCT获取的摆位误差中,平移方向(T)的左右、头脚和升降分别以x、y和z表示,绕其轴旋转的方向(R)分别以Rx、Ry和Rz表示。以CBCT检测的摆位误差为金标准,分析了所有患者中OSIn与CBCT的相关性,利用观测者操作特性(receiver operating characteristics,ROC)曲线评估OSI检测患者摆位的诊断效能。对于使用硅胶补偿膜的患者,将CBCT摆位误差减去OSI摆位误差定义为OSI的检测精度,比较OSIn及OSIb的检测精度。
6. 统计学处理:使用IBM SPSS 26.0进行统计分析,利用GraphPad Prism 8绘制图表。由于数据呈现非正态分布,故使用Spearman秩相关进行相关性分析,以CBCT为分类标准绘制受试者工作特征曲线(ROC)。对OSIn和OSIb平移方向的检测精度做Wilcoxon符号秩检验并计算其系统误差和随机误差,系统误差是组内各患者精度平均值的标准差,随机误差是每个患者精度的标准差的均方根[10]。P<0.05为差异有统计学意义。
结果1. OSIn与CBCT摆位误差的相关性分析:相关结果如表 1,在16例患者中,OSIn与CBCT的摆位误差在x、y和z方向呈高度相关(r=0.87、0.82、0.80),在Rx、Ry和Rz方向呈弱相关或无相关(r<0.40)。
|
|
表 1 乳腺癌根治术后患者OSIn与CBCT的摆位误差和相关系数 (x±s) Table 1 Setup errors and correlation coefficients of OSIn and CBCT in postmastectomy patients (x±s) |
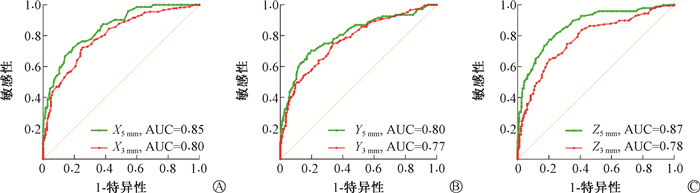
2. ROC曲线分析:对16例患者的389个治疗分次,以CBCT为金标准,分别基于3和5 mm诊断阈值绘制OSIn的ROC曲线(图 2),使用曲线下面积(area under curve,AUC)衡量OSI的诊断效能。其中AUC5 mm和AUC3 mm在x方向分别为0.85和0.80,y方向为0.80和0.77,z方向为0.87和0.78。
|
注:AUC. 曲线下面积 图 2 基于3和5 mm诊断阈值的ROC曲线 A. x平移方向;B. y平移方向;C. z平移方向 Figure 2 ROC curves based on 3 and 5 mm diagnostic thresholds A. x direction; B. y direction; C. z direction |
3. 硅胶补偿膜对OSI检测精度的影响分析:在基于硅胶补偿膜的治疗分次中,比较了OSIn与OSIb平移方向上的检测精度,见表 2。OSIn与OSIb检测精度在x、z方向上差异无统计学意义(P>0.05),在y方向上差异有统计学意义(Z=-2.56,P=0.01),与OSIn相比,OSIb检测精度的系统误差与随机误差在x方向均增加约1 mm,在y方向上,OSIb系统误差增加约3.1 mm,随机误差增加1.9 mm,且x、y方向上的95%置信区间有所增大。
|
|
表 2 OSIn和OSIb平移方向的检测精度 (mm) Table 2 Precision in the translational detection in the case of OSIn and OSIb(mm) |
讨论
相较于放射性成像技术,OSI通过光学扫描获取体表轮廓,并提供非刚性算法来计算软组织表面的形变与位移,光学体表成像已被证实优于三维激光摆位[3, 11],将其应用于临床能提高摆位精度。尽管OSI具有无额外辐射的显著优势,但使用OSI替代CBCT尚待进一步研究[12-13]。
本研究中,在患者体表未覆盖补偿膜时,OSI与CBCT在平移方向上的相关性均高于旋转方向,且OSI在x方向上检测摆位具有较高的精度(r=0.87)。Cravo Sá 等[14]发现在常规摆位流程中引入OSI可显著降低x方向的摆位误差。此外,Wei等[15]报道了OSI与CBCT的相关性,其平移相关性更低(0.7<r<0.8),而旋转相关性更高(0.5<r<0.75),与本研究结果稍有差异。
OSIn与CBCT检测的摆位误差在旋转方向的相关性较差,可能是由于OSI监测旋转和变形的性能容易受到ROI范围的影响。Carl等[16]强调了Catalyst系统对高质量图像的依赖性,例如,Elekta Synergy加速器对OSI双侧摄像头有间断性遮挡,同时中央摄像头无法持续捕获到患者胸骨柄区域的体表图像[11]。考虑到本研究纳入的患者均采用自由呼吸,通常剑突下的体表呼吸运动幅度更大,这可能不利于OSI在y及z方向上的配准,因此,相较于单侧ROI,研究使用的双侧ROI可在一定限度上改善患者的图像缺损;此外,由于腋窝和手臂等结构的分次间变化可能导致胸部外侧变形,且在健侧乳腺中更为明显,而未固定的下颌可对OSI在y方向的配准产生较大影响[17]。Bert等[18]提出应当使用较大的ROI,在摆位中让患者的腋窝、手臂及下颌保持一致有助于矫正患者姿势,但本研究中OSI不参与引导摆位,故ROI也未纳入腋窝、手臂和下颌等结构。最后,有研究采用仅包含胸壁的ROI可以在平移方向获得较好的精度和较高的刷新率[19],但是将ROI限制在胸壁区域可能会导致难以区分旋转方向的随机误差。Sauer等[20]的研究对ROI做了更为细致的划分,并建议使用仅包含患侧乳房、胸骨及两侧乳房下缘环带的ROI,但该研究并未考虑补偿膜的介入。
在乳腺癌放疗中,通过日常的影像引导放疗(IGRT)辅助,平移方向的摆位误差可控制在5 mm以内[21]。ROC分析表明,OSI在y方向上的诊断效能最低。当使用5 mm诊断阈值时,OSI诊断效能尚可(AUC5 mm≥0.8),更严苛的阈值使OSI的诊断效能略有降低(0.8≥AUC3 mm>0.75)。Alderliesten等[19]的一项研究使用了仅包含左侧胸壁的ROI以获得更好的结果(AUCleft=0.92,AUCboth=0.84),并建议使用4到8 mm的阈值,与本研究基本一致。
传统3D打印补偿膜的材料以聚乳酸、ABS塑料等为主,利用此类材料制作的等效补偿膜硬度较大、柔韧性较差,在患者呼吸时较难实现与皮肤的完全贴合,并且存在轻微的不均匀性[22]。为规避此类问题,可以选择在患者弹力紧身衣的内侧放置软硬适度、厚度适度的硅胶膜,不使用3D打印技术的同时仍可改善OSI对体表呼吸运动信息的获取。
本研究采用的补偿膜是含氢硅油和乙烯基聚合物混合而成的硅胶材质,并基于3D打印技术制作。首先在定位CT图像中确定与受累皮肤对应的补偿膜尺寸,并利用定位CT重建的患者解剖信息生成补偿膜和相应模具的数字模型,其次通过3D打印机打印补偿膜模具,最后将加成型的液体硅胶注入模具,保温后得到定形的硅胶补偿膜。此类补偿膜无微气泡,与3D打印的PLA、ABS材质相比,生物相容性和适形性更稳定,并且在研究中观察到补偿膜良好的平坦度和反光性有助于改善成像质量,提高OSI配准时的可靠性。孙梦帆等[23]的研究有类似结论。此外,虽然患者存在呼吸运动,并且硅胶补偿膜具有5 mm左右的厚度,但尚不能认为补偿膜对OSI在x及z方向上的摆位检测有显著影响,这在一定程度上得益于软性补偿膜材质提供的良好贴合性;而在y方向上,补偿膜引入的不确定性尚不能忽略,相比于OSIn,OSIb检测精度的系统误差增大3.11 mm,随机误差增大1.9 mm。这种差异可能是由于不同患者使用不同定制规格的补偿膜,且在同一患者的不同分次间,补偿膜的摆放还受到不同操作者的影响,这都可能导致各个OSI图像间出现不同的补偿膜反光边界,进一步在特定方向上影响图像配准。
光学体表成像在患者摆位、分次内监测及呼吸门控等方面均有一定的临床应用价值[24],并可作为传统成像方式的补充提高摆位精度和减少摆位时间[25-26]。同时,OSI是胸部呼吸门控中实用的监测工具[27],将OSI应用于乳腺DIBH治疗,可实现较好的心脏位置准确性[28],且等中心误差可降低至2 mm[29]。然而,难以避免的物理遮挡会降低OSI检测摆位的可信度,因此,操作者在确定ROI时应更加慎重,覆盖于体表的不同尺寸和材质的补偿膜则引入了额外的不确定性,下一阶段的研究将进一步探索ROI大小与3D打印硅胶补偿膜反光边界对OSI的综合影响。
综上所述,在乳腺癌放疗摆位中OSI尚无法替代CBCT,但检测误差在临床可接受范围内,通过良好的操作训练减轻成像路径上补偿膜等因素的干扰,OSI辅助摆位的性能有望进一步提高。
利益冲突 无
作者贡献声明 罗大双负责实验方案设计、数据采集、分析和论文撰写;李治斌拟定写作思路和分析数据;张翔宇和贺海萍负责数据采集和分析;李光俊提供研究思路、指导实验设计和修改论文;柏森负责论文审校
| [1] |
张光伟, 吴何苟, 刘剑锋, 等. 光学表面监测系统自动摆位功能对乳腺癌放疗患者治疗精度及摆位时间的影响[J]. 中国医学物理学杂志, 2021, 38(4): 411-415. Zhang GW, Wu HG, Liu JF, et al. Effects of automatic setup function of optical surface monitoring system on treatment accuracy and setup time of breast cancer patients undergoing radiotherapy[J]. Chin J Med Phys, 2021, 38(4): 411-415. DOI:10.3969/j.issn.1005-202X.2021.04.003 |
| [2] |
Bright M, Foster RD, Hampton CJ, et al. Failure modes and effects analysis for surface-guided DIBH breast radiotherapy[J]. J Appl Clin Med Phys, 2022, 23(4): e13541. DOI:10.1002/acm2.13541 |
| [3] |
Stanley DN, McConnell KA, Kirby N, et al. Comparison of initial patient setup accuracy between surface imaging and three point localization: a retrospective analysis[J]. J Appl Clin Med Phys, 2017, 18(6): 58-61. DOI:10.1002/acm2.12183 |
| [4] |
Kojima H, Takemura A, Kurokawa S, et al. Evaluation of technical performance of optical surface imaging system using conventional and novel stereotactic radiosurgery algorithms[J]. J Appl Clin Med Phys, 2021, 22(2): 58-68. DOI:10.1002/acm2.13152 |
| [5] |
高艳, 梁晓敏, 张定, 等. 光学表面监测系统对头部无框架立体定向放疗运动监控的研究[J]. 中华放射医学与防护杂志, 2022, 42(4): 283-290. Gao Y, Liang XM, Zhang D, et al. Application of optical surface monitoring system in intra-fraction motion monitoring in frameless cranial stereotactic radiotherapy[J]. Chin J Radiol Med Prot, 2022, 42(4): 283-290. DOI:10.3760/cma.j.cn112271-20211210-00479 |
| [6] |
Pallotta S, Vanzi E, Simontacchi G, et al. Surface imaging, portal imaging, and skin marker set-up vs. CBCT for radiotherapy of the thorax and pelvis[J]. Strahlenther Onkol, 2015, 191(9): 726-733. DOI:10.1007/s00066-015-0861-z |
| [7] |
Farhood B, Bahreyni Toossi MT, Ghatei N, et al. A comparison between skin dose of breast cancer patients at the breast region, measured by thermoluminescent dosimeter in the presence and absence of bolus[J]. J Cancer Res Ther, 2018, 14(6): 1214-1219. DOI:10.4103/0973-1482.188429 |
| [8] |
Batumalai V, Holloway L, Delaney GP. A review of setup error in supine breast radiotherapy using cone-beam computed tomography[J]. Med Dosim, 2016, 41(3): 225-229. DOI:10.1016/j.meddos.2016.05.001 |
| [9] |
Moser T, Habl G, Uhl M, et al. Clinical evaluation of a laser surface scanning system in 120 patients for improving daily setup accuracy in fractionated radiation therapy[J]. Int J Radiat Oncol Biol Phys, 2013, 85(3): 846-853. DOI:10.1016/j.ijrobp.2012.05.026 |
| [10] |
van Herk M. Errors and margins in radiotherapy[J]. Semin Radiat Oncol, 2004, 14(1): 52-64. DOI:10.1053/j.semradonc.2003.10.003 |
| [11] |
Kügele M, Mannerberg A, Nørring Bekke S, et al. Surface guided radiotherapy (SGRT) improves breast cancer patient setup accuracy[J]. J Appl Clin Med Phys, 2019, 20(9): 61-68. DOI:10.1002/acm2.12700 |
| [12] |
Li Z, Xiao Q, Li G, et al. Performance assessment of surface-guided radiation therapy and patient setup in head-and-neck and breast cancer patients based on statistical process control[J]. Phys Med, 2021, 89(9): 243-249. DOI:10.1016/j.ejmp.2021.08.007 |
| [13] |
Hoisak JDP, Pawlicki T. The role of optical surface imaging systems in radiation therapy[J]. Semin Radiat Oncol, 2018, 28(3): 185-193. DOI:10.1016/j.semradonc.2018.02.003 |
| [14] |
Cravo Sá A, Fermento A, Neves D, et al. Radiotherapy setup displacements in breast cancer patients: 3D surface imaging experience[J]. Rep Pract Oncol Radiother, 2018, 23(1): 61-67. DOI:10.1016/j.rpor.2017.12.007 |
| [15] |
Wei X, Liu M, Ding Y, et al. Setup errors and effectiveness of optical laser 3D surface imaging system (sentinel) in postoperative radiotherapy of breast cancer[J]. Sci Rep, 2018, 8(1): 7270. DOI:10.1038/s41598-018-25644-w |
| [16] |
Carl G, Reitz D, Schonecker S, et al. Optical surface scanning for patient positioning in radiation therapy: a prospective analysis of 1902 fractions[J]. Technol Cancer Res Treat, 2018, 17(1): 1-9. DOI:10.1177/1533033818806002 |
| [17] |
Padilla L, Kang H, Washington M, et al. Assessment of interfractional variation of the breast surface following conventional patient positioning for whole-breast radiotherapy[J]. J Appl Clin Med Phys, 2014, 15(5): 177-189. DOI:10.1120/jacmp.v15i5.4921 |
| [18] |
Bert C, Metheany KG, Doppke KP, et al. Clinical experience with a 3D surface patient setup system for alignment of partial-breast irradiation patients[J]. Int J Radiat Oncol Biol Phys, 2006, 64(4): 1265-1274. DOI:10.1016/j.ijrobp.2005.11.008 |
| [19] |
Alderliesten T, Sonke JJ, Betgen A, et al. Accuracy evaluation of a 3-dimensional surface imaging system for guidance in deep-inspiration breath-hold radiation therapy[J]. Int J Radiat Oncol Biol Phys, 2013, 85(2): 536-542. DOI:10.1016/j.ijrobp.2012.04.004 |
| [20] |
Sauer TO, Ott OJ, Lahmer G, et al. Region of interest optimization for radiation therapy of breast cancer[J]. J Appl Clin Med Phys, 2021, 22(10): 152-160. DOI:10.1002/acm2.13410 |
| [21] |
Hamming VC, Visser C, Batin E, et al. Evaluation of a 3D surface imaging system for deep inspiration breath-hold patient positioning and intra-fraction monitoring[J]. Radiat Oncol, 2019, 14(1): 125. DOI:10.1186/s13014-019-1329-6 |
| [22] |
Zou W, Fisher T, Zhang M, et al. Potential of 3D printing technologies for fabrication of electron bolus and proton compensators[J]. J Appl Clin Med Phys, 2015, 16(3): 90-98. DOI:10.1120/jacmp.v16i3.4959 |
| [23] |
孙梦帆, 彭海燕, 何阳, 等. 反光补偿膜对Catalyst监测乳腺癌术后放疗摆位的影响[J]. 重庆医学, 2022, 51(02): 313-319. Sun MF, Peng HY, He Y, et al. Effect of reflective compensating film on postoperative radiotherapeutic positioning by Catalyst monitor[J]. Chongqing Med, 2022, 51(2): 313-319. DOI:10.3969/j.issn.1671-8348.2022.02.028 |
| [24] |
Padilla L, Havnen-Smith A, Cerviño L, et al. A survey of surface imaging use in radiation oncology in the United States[J]. J Appl Clin Med Phys, 2019, 20(12): 70-77. DOI:10.1002/acm2.12762 |
| [25] |
Walter F, Freislederer P, Belka C, et al. Evaluation of daily patient positioning for radiotherapy with a commercial 3D surface-imaging system (CatalystTM)[J]. Radiat Oncol, 2016, 11(1): 154. DOI:10.1186/s13014-016-0728-1 |
| [26] |
李谭谭, 张江鹄, 宋永文, 等. 光学表面监测系统与CBCT确定左侧乳腺癌深吸气屏气放疗误差的比较[J]. 中华放射肿瘤学杂志, 2020, 29(4): 278-282. Li TT, Zhang JH, Song YW, et al. Comparison of the performance of two methods to determine set-up errors for DIBH patients with left sided breast cancer in radiotherapy[J]. Chin J Radiat Oncol, 2020, 29(4): 278-282. DOI:10.3760/cma.j.cn113030-20190423-00006 |
| [27] |
Schönecker S, Walter F, Freislederer P, et al. Treatment planning and evaluation of gated radiotherapy in left-sided breast cancer patients using the Catalyst(TM)/Sentinel(TM) system for deep inspiration breath-hold (DIBH)[J]. Radiat Oncol, 2016, 11(1): 143. DOI:10.1186/s13014-016-0716-5 |
| [28] |
张光伟, 钟鹤立, 吴何苟, 等. 光学表面监测系统引导实现左侧乳腺癌深吸气屏气治疗临床应用及评估[J]. 中国医学物理学杂志, 2021, 38(7): 793-797. Zhang GW, Zhong HL, Wu HG, et al. Application and evaluation of OSMS guided DIBH radiotherapy for left-sided breast cancer[J]. Chin J Med Phys, 2021, 38(7): 793-797. DOI:10.3969/j.issn.1005-202X.2021.07.001 |
| [29] |
Laaksomaa M, Sarudis S, Rossi M, et al. AlignRT(R) and Catalyst in whole-breast radiotherapy with DIBH: Is IGRT still needed?[J]. J Appl Clin Med Phys, 2019, 20(3): 97-104. DOI:10.1002/acm2.12553 |
 2022, Vol. 42
2022, Vol. 42


