2. 复旦大学放射医学研究所,上海 200032
2. Institute of Radiation Medicine, Fudan University, Shanghai 310000, China
大量流行病学研究证实,在工作场所和家庭中接触氡会增加患肺癌的风险。在公众中, 暴露于居室内氡被确定为肺癌的第二大原因,仅次于吸烟[1-2]。氡致肺癌的风险估计提供了衡量肺癌在人群中归因份额的方法。国外很多研究已经估算了居室内氡致肺癌的病因学贡献[3-4];国内关于不同地区氡浓度水平的报道较多。有学者调查显示我国居室内氡浓度呈现逐年上升的趋势[5-7],并据此估计了公众现在所受天然辐射剂量平均年有效剂量为3.1 mSv,远高于世界均值。国内既往有两项涉及居室氡与肺癌关系研究,一项在沈阳,一项在甘肃平凉、庆阳地区,经合并分析,共包括1 050肺癌病例和1 996名对照,根据线性模型,在95%置信区间情况下,每100 Bq/m3的比值比(OR)为1.33(95%CI 1.01~1.36)[8]。1999年,美国电离辐射生物效应委员会(BEIR)报告VI通过对11项氡暴露矿工队列研究(包括我国个旧锡矿矿工队列研究从1976—1987年共随访17 143名矿工)的联合分析,开发了两种首选的风险模型,分别为照射-年龄-时段模型和照射-年龄-浓度模型[9]。历经10余年的改进和完善,美国环境保护署(EPA)于2003年评估了居室内氡的风险,并得出了两个BEIR-VI模型(后称为EPA/BEIR-VI风险模型)的合理平均值[10]。同时,我国也有学者对氡与肺癌的危险度关系及模型进行了深入研究[11-13]。但目前国内暂无居室内氡导致肺癌风险估计结果的相关报道。本文拟使用目前较为权威且适用的EPA/BEIR-VI风险模型,基于我国的人口学和肺癌死亡数据、吸烟分布、氡浓度水平等因素,计算我国氡诱发肺癌的例数,评估我国居室内氡浓度水平致肺癌死亡的风险,旨在让公众对于居室内氡的危害有更为直观且科学的认识,同时也为今后开展居室内氡浓度水平的控制和科学配置卫生资源提供更进一步的科学数据。
资料与方法1.氡致肺癌风险模型的计算:根据EPA/BEIR-VI风险模型[10],计算超额相对危险(ERR)公式(1)如下:
| $ e(\alpha ) = \beta \left( {{W_{5 - 14}} + 0.78{W_{15 - 24}} + 0.51{W_{25 + }}} \right){\varphi _{{age}}} $ | (1) |
式中,a为年龄,岁;β为单位暴露增加的风险,表示每个工作水平月(WLM)的ERR值。对吸烟者,β=0.057;非吸烟者,β=0.127。对于特定氡浓度,累积暴露W(以WLM表示)可以通过3个暴露后的时间段加权计算,即W5-15是年龄a之前的5~14年的暴露量,WLM;W15-24是年龄a之前的15~24年之间的暴露量;W25+是在年龄a之前的25年及以上的暴露量,WLM。该模型认为罹患肺癌前5年以内的氡暴露不会增加肺癌的风险。在风险计算中EPA给出了ϕage(a)的连续函数。1 Bq/m3氡浓度的连续照射导致在居室内年暴露量为4.4×10-3 WLM(假设居室内居留时间占70%,氡及其子体平衡因子为0.4)。
肺癌终生风险的计算公式(2)在BEIR VI报告中给出,肺癌的终生风险是由每年的肺癌死亡风险相加得到的:
| $ \begin{array}{*{20}{c}} {{R_e} = \sum\nolimits_{i = 1}^{110} {\frac{{{h_i}\left( {1 + {e_i}} \right)}}{{h_i^* + {h_i}{e_i}}}} \prod\nolimits_{k = 1}^{i - 1} {\exp } \left( { - \left( {h_i^* + {h_k}{e_k}} \right)} \right)}\\ {\left[ {1 - \exp \left( { - \left( {h_i^* + {h_i}{e_i}} \right)} \right)} \right]} \end{array} $ | (2) |
式中,Re为特定暴露下的肺癌终生风险;hi和hi*分别为在年龄i时肺癌死亡率和全死因死亡率;ei为对于年龄i由氡及其子体暴露所致ERR值(由式1给出)。
终生相对危险(LRR)定义为LRR=Re/R0,式中R0是基线风险,即暴露于本底氡水平的终生肺癌风险。LRR描述了室内氡暴露造成的肺癌风险比暴露于室外本底水平增加的比例。
关于吸烟因素的调整,BEIR-VI报告认为,吸烟和氡联合暴露对导致肺癌而言在相对风险尺度上是亚相乘的。BEIR-VI报告认为,吸烟和氡的联合作用对导致肺癌而言为次乘效应。
关于我国不同性别吸烟率的调查来自文献调研,2003年我国吸烟年龄平均从15岁开始,男性吸烟率为67%,女性吸烟率为4%[16]。假设吸烟诱发肺癌有10年的潜伏期,与从不吸烟人群相比,一直吸烟人群的相对危险度本研究引用EPA/BEIR-VI模型中的数据,男性为14,女性为12。按照EPA/BEIR-VI模型中通过吸烟致肺癌的相对危险度(RR),对吸烟与不吸烟人群的肺癌死亡率进行调整。
2.我国居室内氡浓度的选取:2006—2010年开展的覆盖我国部分地区的居室氡浓度调查[17],共涉及1个省和7个城市,测量房间数共计2 029个,涉及省市人口约占全国总人口的12%。氡浓度范围为5.3~183.0 Bq/m3,按样本量加权算数均值为(32.6± 5.2) Bq/m3,按人口加权均值为(30.7± 4.3) Bq/m3。同样,2008—2010年开展的涉及我国9个城市的居室氡浓度调查显示,室内氡浓度平均水平为(34.9± 25.3) Bq/m3[18]。在本文中,假设居民一直暴露的居室内氡浓度水平为30 Bq/m3。同时还结合相关报道[5],分别计算终生暴露在居室内氡浓度水平为40 Bq/m3和70 Bq/m3时的风险。
结果1.不同年龄吸烟与不吸烟男性的ERR分布:根据式(1),假设氡浓度为30 Bq·m-3,20~80岁吸烟与不吸烟男性居室内氡致肺癌ERR的分布见图 1。从图 1可看出,ERR值随着年龄的增长,有先上升后下降的趋势,这可能是因为EPA/BEIR-VI模型对于50岁以上人群ERR风险进行了修正。随着到达年龄的增长,肺癌死亡基线风险会增加。不吸烟与吸烟男性的ERR在50岁时达到最大值,分别为0.511、0.230,前者是后者的2.2倍。不吸烟男性人群居室内氡致肺癌死亡ERR高于吸烟男性人群,是因为吸烟人群比不吸烟人群的肺癌发病基线要高很多,吸烟人群的肺癌超额绝对风险要高于不吸烟人群。
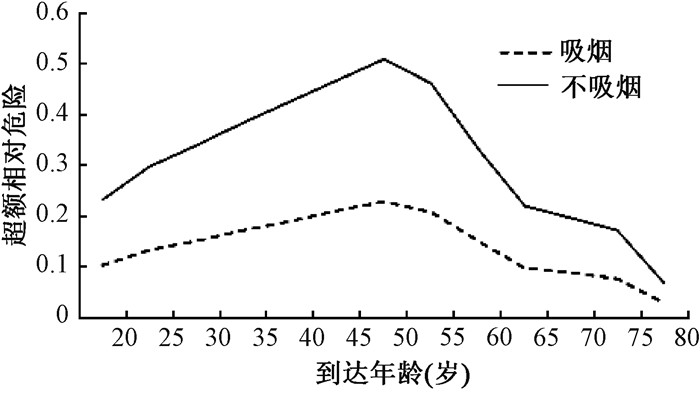
|
(假设氡浓度为30 Bq/m3) 图 1 吸烟与不吸烟男性不同到达年龄的ERR分布 (radon concentration assumed to be 30 Bq/m3) Figure 1 ERR distribution of smoking and non-smoking men with different attained age |
2.不同性别吸烟与非吸烟人群的LRR分布:利用BEIR-VI模型估算出不同性别、不同氡浓度的LRR,见表 1。根据国内肺癌发病率数据,估算男性基线肺癌风险(R0)吸烟人群和不吸烟人群分别为0.117和0.008;女性基线肺癌风险(R0)吸烟人群与不吸烟人群分别为0.369和0.031。从表 1可以看出,相同氡浓度下,男性与女性不吸烟人群的肺癌死亡LRR要高于同性别吸烟人群,浓度越高其LRR也越高;当氡浓度为1 000 Bq/m3时,不吸烟人群男性、女性的LRR分别可达6.714和5.672。与吸烟人群相比,不吸烟人群的LRR要高得多,这主要是因为不吸烟人群的基线肺癌风险远低于(小于十分之一)长期吸烟人群。
|
|
表 1 不同性别和不同氡浓度的吸烟与不吸烟的LRR分布 Table 1 LRR distribution of smoking and non-smoking by gender and radon concentration |
3.我国居室内氡致肺癌风险的预测:根据文献[7]假设我国氡浓度平均值为30 Bq/m3,< 15岁的人群氡致肺癌死亡风险约为2人,而15岁及以上的人群按照吸烟率进行调整,计算不同年龄段、不同性别的氡致肺癌死亡人数见表 2。从表 2可以看出,吸烟男性氡致肺癌人数要高于不吸烟的人群,而不吸烟的女性人群氡致肺癌死亡人数要高于吸烟人群。产生这个差异的一个主要原因是女性吸烟率远低于男性,但吸烟和氡致女性人群肺癌死亡的风险比例仍值得进一步研究。据估算,我国2015年由氡所致肺癌死亡人数约为55 512人,其中吸烟男性为28 774人,不吸烟男性为2 363人;吸烟女性为4 048人,不吸烟女性为20 325人。我国约6.62%的肺癌死亡是由居室内氡暴露造成的(2015年我国肺癌死亡人数为838 793人),但如果假设我国居室内氡浓度水平分别为40 Bq/m3和70 Bq/m3,2015年居室内氡暴露致肺癌死亡人数分别为73 941人和129 008人,约8.82%和15.38%的肺癌死亡可归因于居室内氡暴露。
|
|
表 2 我国2015年死于氡致肺癌人数(氡浓度为30 Bq/m3) Table 2 Number of lung cancer deaths caused by radon in China in 2015 (radon concentration is 30 Bq/m3) |
讨论
本研究利用EPA/BEIR-VI风险模型结合我国的肺癌死亡率等人口学数据,估算了不同居室氡浓度下致肺癌死亡的风险,显示我国居室内氡浓度水平在30 Bq/m3时,预测致2015年肺癌死亡为55 512人,我国约有6.62%的肺癌死亡由居室内氡暴露造成。
既往关于我国居室内氡浓度水平的调查文献较多,本文选择的氡浓度为30 Bq/m3,但近些年,许多研究发现由于建筑类型和建筑材料的变化等原因,居室内氡浓度水平呈上升趋势。尚兵等[5]报道1999—2003年我国26个城市和地区室内平均氡浓度值为(43.8±37.3)Bq/m3;刘焱等[6]报道2018—2019年深圳市居室内平均氡浓度值为(63±10)Bq/m3;武云云等[7]2020年对5个城市的25户住宅密闭门窗24 h,测量居室内氡浓度均值为122 Bq/m3。一般认为随着我国住宅从80年代以黏土砖平房为主,到目前以工业废渣砌块楼房的变化,居室内氡浓度水平是上升的。若假设我国氡浓度水平为40 Bq/m3,氡致肺癌死亡人数为73 941人,约有8.82%的肺癌死亡可归因于居室内氡暴露。据中国疾病预防控制中心辐射防护与核安全医学所近年来组织开展的氡浓度监测数据初步结果,我国居室内氡浓度水平接近70 Bq/m3,据此水平估计约15.38%的肺癌死亡是由居室内氡暴露导致的。必须说明的是,为了简化计算,假定终生氡暴露水平是不变的,而实际上在整个暴露过程中氡浓度很可能是变化的,因此,本研究的初步估算结果仍存在有不确定度。
基于EPA/BEIR-VI风险模型的研究结果,显示我国氡浓度水平导致肺癌死亡的归因占比与其他国家相比相对较低。加拿大既往调查显示,10%的肺癌死亡是由于居室内氡暴露造成的,但在2009年4月启动的第二次全国住宅氡调查,观测到的氡浓度几何均值为41.9 Bq/m3,标准差为2.8,理论估计加拿大人16%的肺癌死亡可归因于居室内氡暴露[19]。Catelinois等[4]量化了氡致肺癌风险系数和暴露相关的不确定性,根据所考虑的模型计算,法国1999年居室内平均氡浓度约为89 Bq/m3,有2.2% (90% UI,0.3~4.4)到12.4% (90% UI,11.9~12.8)的肺癌死亡可归因于居室内氡暴露,并建议吸烟者不仅可以通过降低居室内氡浓度,还可以通过戒烟来降低风险。美国1995年平均氡浓度水平约为46 Bq/m3,估计13.5%的肺癌与居室内氡暴露有关[10]。
本文使用BEIR模型进行风险预测,而文献中也有应用其他模型,例如欧洲矿工氡风险模型[20]、北美住宅氡合并分析风险模型[21]以及我国居室内氡合并分析模型[8]等。使用不同的风险模型所预测的风险有差异(约相差2倍)[3],其中,BEIR模型预测的风险接近于几种模型的均值。对许多人来说,模型预测的风险往往被视为理论或假设的风险,这可能不是真实的,但风险是真实存在的,在一些环境参数未知或不为人所知的不同环境中,预测值与观察到的结果存在差异是完全可以理解的。模型的不确定性主要来源于样本变异性、个体暴露估计、吸烟资料不完整等。为了提高风险估计/预测的准确性,需要进行更多的研究,要细化风险评估的技术细节。其中,模型中引用吸烟男性的肺癌风险的相对危险度为14,女性为12,但有研究表明东方人吸烟致肺癌的相对危险度要低于西方人群[22],此外,如若使用不同性别年龄别吸烟率数据更能符合实际平滑预测数据。最为关键的还是需要了解我国居室内氡浓度水平的分布情况,对不同氡浓度水平进行加权计算其风险,才能更为准确地评估我国居室内氡的健康风险,为今后能够更好地指导居室内氡水平的控制提供理论基础,同时也有助于公众对居室内氡的危害有更为科学且直观的认识。
利益冲突 无
志谢 感谢国家癌症中心/中国医学科学院肿瘤医院流行病学研究室李霓主任提供癌症统计相关数据
作者贡献声明 苗晓翔负责设计研究方案、实施研究过程、数据计算、撰写论文;苏垠平负责设计论文框架、数据计算分析、修改论文要素;卓维海、孙全富负责提出研究方向、组织协调和指导修改论文
| [1] |
The World Health Organization. Handbook on indoor radon[R]. Geneva: WHO, 2009.
|
| [2] |
Hoffman FO. Lung cancer risk from radon and progeny and statement on radon. ICRP publication 115, Ann. ICRP 40(1)[J]. Radiat Prot Dosim, 2012, 151(1): 199-201. DOI:10.1093/rpd/ncs093 |
| [3] |
Chen J. Lifetime lung cancer risks associated with indoor radon exposure based on various radon risk models for Canadian population[J]. Radiat Prot Dosim, 2017, 173(1-3): 252-258. DOI:10.1093/rpd/ncw297 |
| [4] |
Catelinois O, Rogel A, Laurier D, et al. Lung cancer attributable to indoor radon exposure in France: impact of the risk models and uncertainty analysis[J]. Environ Health Perspect, 2006, 114(9): 1361-1366. DOI:10.1289/ehp.9070 |
| [5] |
尚兵, 张林, 陈斌. 中国典型地区室内氡水平的研究[J]. 工程兵勘探设计, 2007, 55(5): 4-11. Shang B, Zhang L, Chen B. Study on indoor radon level in typical areas of China[J]. Engin Recon Design, 2007, 55(5): 4-11. |
| [6] |
刘焱, 郭键锋, 时劲松, 等. 深圳市室内氡浓度水平调查与研究[J]. 能源与保护, 2020, 42(7): 74-77. Liu Y, Guo JF, Shi JS, et al. Investigation and study on indoor radon concentration level in Shenzhen City[J]. China Energ Environment Prot, 2020, 42(7): 74-77. DOI:10.19389/j.cnki.1003-0506.2020.07.016 |
| [7] |
武云云, 张庆召, 宋延超, 等. 建筑节能设计对严寒和寒冷地区居室氡浓度和换气率的影响[J]. 中华放射医学与防护杂志, 2020, 40(12): 945-950. Wu YY, Zhang QZ, Song YC, et al. Impact of energy-saving design of residential buildings on both indoor radon concentration and air exchange rate in severe-cold areas and cold areas[J]. Chin J Radiol Med Prot, 2020, 40(12): 945-950. DOI:10.3760/cma.j.issn.0254-5098.2020.12.009 |
| [8] |
Lubin JH, Wang ZY, Boice JD Jr, et al. Risk of lung cancer and residential radon in China: pooled results of two studies[J]. Int J Cancer, 2004, 109(1): 132-137. DOI:10.1002/ijc.11683 |
| [9] |
National Research Council. BEIR VI. Health effects of exposure to Radon[R]. Washington, DC: The National Academies Press, 1999.
|
| [10] |
United States Environmental Protection Agency. EPA assessment of risks from radon in homes[R]. Washington, DC: USEPA, 2003.
|
| [11] |
童建. 氡致肺癌的危险度评价模型[J]. 中华劳动卫生职业病杂志, 2007, 25(6): 372-374. Tong J. Model for evaluation of hazards of radon induced lung cancer[J]. Chin J Ind Hyg Occup Dis, 2007, 25(6): 372-374. DOI:10.3760/cma.j.issn.1001-9391.2007.06.017 |
| [12] |
孙世荃. 氡子体照射诱发肺癌的危险估计模型[J]. 中国辐射卫生, 1996, 5(3): 132-135. Sun SQ. Risk estimation model of lung cancer induced by radon daughter irradiation[J]. Chin J Radiol Health, 1996, 5(3): 132-135. DOI:10.13491/j.issn.1004-714x.1996.03.003 |
| [13] |
王作元, 曹吉生, 崔宏星. 氡致肺癌的相对危险度[J]. 中华放射医学与防护杂志, 2001, 21(5): 395-396. Wang ZY, Cao JS, Cui HX. Relative risk of lung cancer caused by radon[J]. Chin J Radiol Med Prot, 2001, 21(5): 395-396. DOI:10.3760/cma.j.issn.0254-5098.2001.05.031.issn.0254-5098.2001.05.031 |
| [14] |
Chen WQ, Zheng RS, He J. Cancer statistics in China, 2015[J]. CA Cancer J Clin, 2016, 66(2): 115-132. DOI:10.3322/caac.21338 |
| [15] |
中国统计局. 中国统计年鉴[M]. 北京: 中国统计出版社, 2016. National Bureau of Statistics. Chinese statistical yearbook[M]. Beijing: China Statistics Press, 2016. |
| [16] |
Zhang H, Cai B. The impact of tobacco on lung health in China[J]. Respirology, 2003, 8(1): 17-21. DOI:10.1046/j.1440-1843.2003.00433.x |
| [17] |
王春红, 潘自强, 刘森林, 等. 我国部分地区居室氡浓度水平调查研究[J]. 辐射防护, 2014, 34(2): 65-73. Wang CH, Pan ZQ, Liu SL, et al. Investigation on indoor radon concentration in some areas of China[J]. Radiat Prot, 2014, 34(2): 65-73. DOI:10.3969/j.issn.1000-8187.2014.02.001 |
| [18] |
卓维海, 王喜元, 金元. 我国9个城市室内的氡浓度水平[Z]. 包头: 第三次全国天然辐射照射与控制研讨会论文汇编, 2010. Zhuo WH, Wang XY, Jin Y. Indoor radon concentration in 9 cities of China[Z]. Baotou: Compilation of papers of the Third National Symposium on Natural Radiation Exposure and Control, 2010. |
| [19] |
Chen J, Moir D, Whyte J. Canadian population risk of radon induced lung cancer: a re-assessment based on the recent cross-Canada radon survey[J]. Radiat Prot Dosim, 2012, 152(1-3): 9-13. DOI:10.1093/rpd/ncs147 |
| [20] |
Darby S, Hill D, Auvinen A, et al. Radon in homes and risk of lung cancer: collaborative analysis of individual data from 13 European case-control studies[J]. BMJ, 2005, 330(7485): 223. DOI:10.1136/bmj.38308.477650.63 |
| [21] |
Krewski D, Lubin JH, Zielinski JM, et al. A combined analysis of North American case-control studies of residential radon and lung cancer[J]. J Toxicol Environ Health A, 2006, 69(7): 533-597. DOI:10.1093/rpd/ncs147 |
| [22] |
Stellman SD, Takezaki T, Wang L, et al. Smoking and lung cancer risk in American and Japanese men: an international case-control study[J]. Cancer Epidemiol Biomarkers Prev, 2001, 10(11): 1193-1199. DOI:10.1016/S0040-6090(98)00943-2 |
| [23] |
Jung KJ, Jeon C, Jee SH. The effect of smoking on lung cancer: ethnic differences and the smoking paradox[J]. Epidemiol Health, 2016, 38. DOI:10.4178/epih.e2016060 |
 2022, Vol. 42
2022, Vol. 42


