立体定向放射治疗(SBRT)或立体定向放射外科(SRS)技术具有剂量分布适形度高、剂量跌落快[1]和周围正常组织损伤小的优势[2]。但由于该技术射野小,剂量难以准确测量[3-4],可能存在大量非共面射野角度,导致相关质量控制工作难度增加。临床常用的小野测量探测器需要多种修正,大量的校准因子[5]使测量复杂且影响剂量的准确性。国际原子能机构(IAEA)发布的TRS-483号报告指出:塑料闪烁体探测器是目前唯一射线质校准因子为1.0的探测器,建议在测量小野时使用塑料闪烁体探测器[1, 6-7]。
W2剂量计(美国Standard Imaging公司)是目前唯一商业量产的塑料闪烁体探测器[8-11],由于W2的光信号由光纤传输,而光纤在高能射线照射下会发生切伦科夫辐射,对剂量信号产生污染[12]。同时切伦科夫辐射对射线与光线夹角敏感,本研究旨在非共面射野临床应用前,探究该探测器对电子束和光子束切伦科夫辐射的修正以及角度响应的修正,为后续SBRT/SRS的临床应用提供理论依据。
材料与方法1. 仪器设备:本研究采用瓦里安Ⅸ-5459型号直线加速器(美国瓦里安医疗系统公司),提供6、10 MV光子束和6、9、12、15 MeV电子束进行测量。
2. Exradin的W2塑料闪烁体:W2塑料闪烁纤维的探测器,包括W2-1×1和W2-1×3两种型号。本研究所使用的型号为W2-1×1,其直径1 mm,长度为1 mm(有效灵敏体积为8×10-4 cm3)。而型号W2-1×3的直径也为1 mm,长度为3 mm(有效灵敏体积为24×10-4 cm3),当探测信号受到限制需提高信噪比时,可以使用W2-1×3型号。探测器使用时需连接专用的静电计(MAX SD,美国Standard Imaging公司)。W2闪烁体由两个主要组件组成:塑料闪烁纤维(由聚苯乙烯组成探测器的敏感部分)和光纤,光纤将闪烁器中产生的光传输到光电探测单元进行信号处理。塑料闪烁体受照发光的光谱在450 nm左右具有一个特征峰,而切伦科夫辐射的光谱较为平坦,覆盖整个可见光谱。在医用加速器产生的电离辐射粒子能量范围内,切伦科夫辐射光谱不随受照光纤长度与角度变化,闪烁体信号由蓝色和绿色两通道线性组合构成[13]。因此,可以根据双通道信号确定剂量,公式如下:
| $ D = {k_{{\rm{gain}}}}\left( {{S_{{\rm{Blue}}}} - CLR \cdot {S_{{\rm{Green}}}}} \right) $ | (1) |
式中,D为绝对剂量,Gy;kgain为信号剂量转换系数;SBlue为蓝色通道信号;SGreen为绿色通道信号;CLR为切伦科夫校准因子。
3. MAX SD静电计控制单元:是一种专用的光电探测和信号处理单元,用于提取闪烁体的辐射信号。其中光电探测单元将收集的光信号通过分光光度计分成“蓝色”和“绿色”信号通道, 由两个光电二极管收集可见光信号。切伦科夫辐射具有与闪烁光谱重叠的宽光谱,因此来自蓝光通道的信号是由闪烁体发光和切伦科夫辐射共同产生的,而绿光通道的信号源主要是由切伦科夫辐射产生的。各通道光电二极管分别收集电流,根据以下公式进行计算两通道信号比例,以剥离蓝光通道中切伦科夫辐射贡献:
| $ {\rm{CLR}} = \frac{{{\rm{Blu}}{{\rm{e}}_{{\rm{MAX}}}} - {\rm{Blu}}{{\rm{e}}_{{\rm{MIN}}}}}}{{{\rm{Gree}}{{\rm{n}}_{{\rm{MAX}}}} - {\rm{Gree}}{{\rm{n}}_{{\rm{MIN}}}}}} $ | (2) |
式中,Blue和Green为蓝色和绿色通道信号;MAX和MIN为被照射的最大和最小光纤长度, cm。
此外,MAX SD可以将校正后的光信号转换为模拟信号,由外部单通道静电计读取,最后基于电信号进行绝对剂量标定。
4.光子和电子的剂量和剂量率线性
(1) 光子剂量和剂量率线性:将W2探测器放置于固体水校准模体中,垂直于射束,照射能量为6 MV,射野为5 cm×5 cm,剂量线性以400 MU/min恒定剂量率,对探测器照射100、200、300、400、500和600 MU,每个剂量重复测量3次。剂量率线性以100 MU恒定剂量,对100~600 MU/min进行线性验证,重复测量3次。
(2) 电子剂量和剂量率线性:将W2探测器放置于固体水校准模体中,垂直于射束,照射能量为6 MeV,射野为6 cm×6 cm限光筒,剂量线性以400 MU/min恒定剂量率,对探测器照射100、200、300、400、500和600 MU,每个剂量重复测量3次。剂量率线性以100 MU恒定剂量,对100~600 MU/min和1 000 MU/min进行线性验证,重复测量3次。
5. 光子和电子的角度响应测量
(1) W2的角度响应(CLR)校准:利用与剂量计配套的固体水模体进行校准,该校准模体可以将光纤固定在直通道(光纤受照长度最小)或弯通道(光纤受照长度最大)中,由于射野中光纤受照长度的区别,所测得的切伦科夫辐射强度不同。在光纤长度受照分别最大和最小的两种情况中,应注意确保光纤的尖端紧靠通道的末端,即保持探测器敏感体积在射野中同一位置。固定好的W2闪烁体应与射束中心轴垂直,光子束校准条件为照射能量6和10 MV,照射野30 cm×30 cm,100 MU恒定剂量,源到探测器的距离(SDD)为100 cm,直到读数稳定,重复测量3次;电子束校准条件为照射能量6、9、12和15 MeV,照射野25 cm×25 cm限光筒,100 MU恒定剂量,SDD=100 cm,直到读数稳定,重复测量3次。MAX SD静电计可根据公式(2)计算并在内置数据库中记录CLR值。
(2) 闪烁体有效灵敏体积定位:由于W2闪烁体水等效,很难通过透视片观察其有效灵敏体积的位置。因此,使用带有定位功能的虚拟探头, (图 1 A的红色圆圈为W2有效灵敏体积,其有效测量点处为一个直径1 mm的不锈钢球)进行kV影像板定位,用以确定W2闪烁体的有效灵敏体积,图 1B为后面W2实验提供准确的测量位置。

|
注:红色圆圈为W2有效灵敏体积 图 1 W2闪烁体有效灵敏体积定位图像 A.虚拟探测器;B.W2探测器 Figure 1 Effective sensitive volume position image of W2 scintillator A.Dummy detector; B. W2 detector |
(3) 角度响应:以射束中心轴为基准,旋转中心与光纤轴线分别成0°、15°、30°、45°、60°、75°和90°(0°与射束垂直,90°与射束平行)进行照射。光子束照射能量为6和10 MV,100 MU恒定剂量,分别在1 cm × 1 cm、2 cm × 2 cm、3 cm × 3 cm、4 cm × 4 cm、5 cm × 5 cm、7 cm × 7 cm和10 cm × 10 cm的照射野下测量,研究辐照角度方向对CLR测量的影响。电子束照射能量为6、9、12和15 MeV,100 MU恒定剂量,分别在6 cm × 6 cm、10 cm × 10 cm和15 cm × 15 cm限光筒下测量,研究辐照角度对CLR测量的影响。测量时均需将W2闪烁体的有效灵敏体积放置于射束等中心的位置。
(4) 绝对剂量归一:根据公式(1)重新整理公式:
| $ \frac{{{S_{{\rm{Blue}}}}}}{D} = {\rm{CLR}} \cdot \frac{{{S_{{\rm{Green}}}}}}{D} + \frac{1}{{{k_{{\rm{gain}}}}}} $ | (3) |
按照公式(3)将MAX SD测量的信号通道除以对应射野剂量,是将蓝、绿色通道信号按照剂量进行归一。根据公式(3)可知CLR为蓝、绿色通道的信号比的斜率,将不同射野测得的数据整合为一个数据集进行线性回归。本实验在进行剂量归一时,所有角度均按W2光纤为0°时测量的剂量归一。本中心放疗计划系统光子束和电子束建模的算法分别为AXB和eMC,由于采用eMC计算剂量计对应沉积剂量的精度鲜有报道,因此本研究确定光子束与电子束的剂量方法不同,做分类描述。①光子束绝对剂量:使用Eclipse治疗计划系统AXB算法版本15.5(Varian Medical Systems,Palo Alto,CA, 美国瓦里安公司)计算网格1 mm计算得到模体等中心的剂量,对应闪烁体在相应射野中受照剂量。采用45 cm×45 cm×40 cm固体水模体,相同机器,机架角度0°,小机头角度0°,剂量100 MU,照射能量为6和10 MV,射野分别为1 cm × 1 cm、2 cm × 2 cm、3 cm × 3 cm、4 cm × 4 cm、5 cm × 5 cm、7 cm × 7 cm和10 cm × 10 cm等中心垂照,测量不同射野下模体等中心的剂量。②电子束绝对剂量:将Roos电离室(德国PTW公司)放置在二维水箱中治疗射束等中心位置,机架角度0°,小机头角度0°,剂量100 MU,照射能量为6、9、12和15 MeV,在6 cm × 6 cm、10 cm × 10 cm和15 cm × 15 cm限光筒下测量等中心的剂量。
6. 统计学处理:本研究采用SPSS 25.0版软件对数据进行自抽样(bootstrapping)检验。由于不同照射条件下测量的校准系数(CLR,kgain)显现一定的差异分布,应用自抽样法将校准系数数据生成多个校准情况,获得校准系数误差,该误差可评估实际临床应用中校准系数的潜在误差。同时将该误差传递到测得的剂量上,可评估实际测量中剂量测量的不确定度。本研究采用SigmaPlot10.0版软件进行绘图。静电计读数的稳定性采用x±s表示,P < 0.05为差异有统计学意义。
结果1.剂量和剂量率线性:结果显示,照射能量分别为6 MV和6 MeV,探测信号与剂量的线性回归决定系数相同(y=0.01x×0.000 2,y=0.01x×0.007 0; R2=1.0),探测信号强度随剂量率的变化情况,光子束和电子束蓝、绿通道读数相对稳定,两通道均以100 MU/min为基准,蓝通道最大偏差分别为0.61%和0.49%, 绿通道最大偏差分别为0.37%和0.42%。W2测得的蓝光和绿光信号强度比较差异无统计学意义(P>0.05),说明两通道信号强度与剂量率无关。
2. MAX SD静电计读数稳定性:结果如表 1所示,重复测量3次,在光子束和电子束校准条件下,最大长度光纤中蓝色和绿色通道读数平均值的标准偏差为0.03~0.21,最小长度光纤中蓝色和绿色通道读数平均值的标准偏差为0.03~0.47,表明静电计读数具有很好的重复性。
|
|
表 1 不同能量最大和最小长度光纤得到的蓝、绿色通道读数(x±s) Table 1 Blue and green channel signal in the max and min fibers withdifferentenergy(x±s) |
3. W2光信号与能量、射野及角度的关系
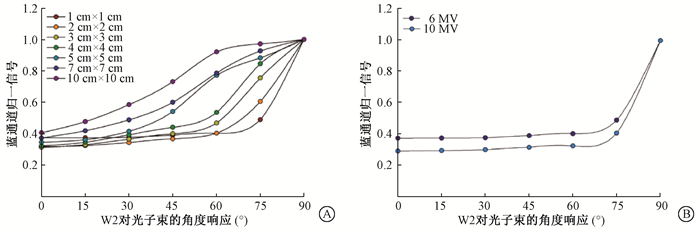
(1) 光子束光信号的角度响应与能量、射野的关系:图 2显示,对于不同能量和不同射野大小的光子束,随着入射角度的增加,光输出信号逐渐增加,并在90°时出现最大值。
|
图 2 能量和射野不同时W2对光子束的角度响应 A.相同能量(6 MV)不同射野;B.相同射野(1 cm×1 cm)不同能量 Figure 2 Angular response of W2 to the photon beam with different energy and field size A. One energy(6 MV)with different field size; B. One field size(1 cm×1 cm)with different X-ray energy |
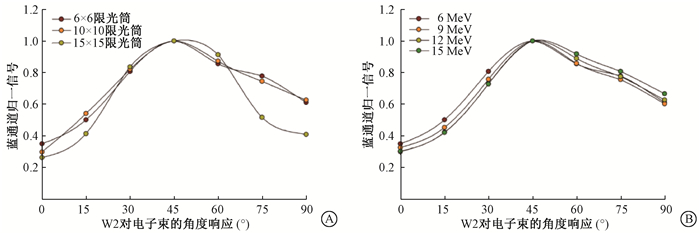
(2) 电子束光信号的角度响应与能量、射野的关系:图 3显示在不同能量与不同射野大小的电子束照射下蓝光通道信号沿射束与光纤所成角度分布关系。当入射角度从零增加时,光电二极管的光输出信号(蓝色通道信号)增加,在大约45°处增加至最大值,然后下降。在6 cm×6 cm、10 cm × 10 cm和15 cm × 15 cm限光筒的相同角度出现峰值,在6、9、12和15 MeV的相同角度出现峰值。
|
图 3 不同能量和不同限光筒条件下W2的角度响应 A.不同限光筒; B.不同能量 Figure 3 Angular response for W2 with different energy and applicator A. Different applicator; B. Different energy |
4.角度响应
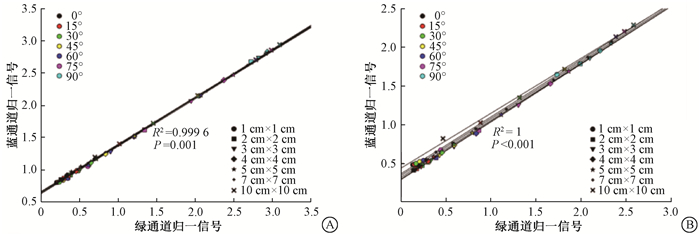
(1) W2闪烁体在光子束中的角度响应(CLR):图 4显示蓝色和绿色通道信号的函数关系,将不同射野尺寸和不同角度的CLR拟合成一个总CLR,其中6 MV的总CLR=0.741,10 MV的总CLR=0.746。结果显示根据不同射野大小单独拟合CLR,与总CLR相比,1 cm×1 cm到10 cm×10 cm射野范围内,6 MV的偏差分别为-0.68%、0.54%、0.41%、0.14%、-1.35%、-1.08%和-1.08%。10 MV的偏差分别为-1.47%、0%、0%、-0.13%、-1.21%、-1.47%和-1.74%。
|
图 4 不同射野和不同角度下,蓝色和绿色通道信号比值(CLR) A.6 MV;B.10 MV Figure 4 The ratio of signal(CLR)between the blue and green channel for different field size and incident angle A. 6 MV; B. 10 MV |
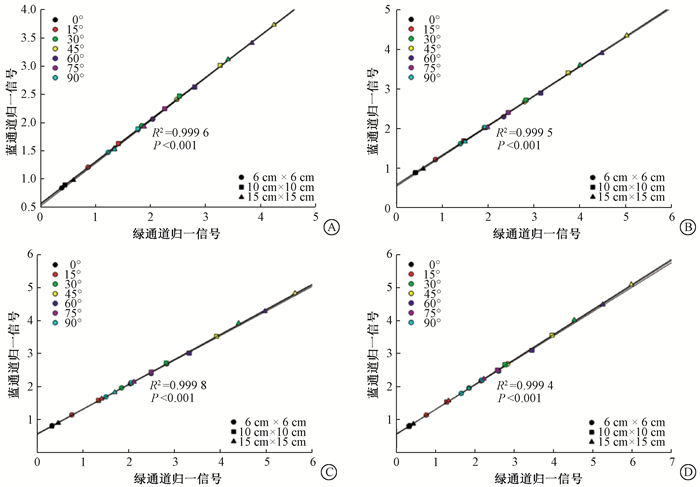
(2) W2闪烁体在电子束中的CLR:图 5显示蓝色和绿色通道信号的函数关系,将不同限光筒和不同角度的CLR拟合成一个总CLR,其中6 MeV的总CLR=0.750,9 MeV的总CLR=0.753,12 MeV的总CLR=0.757,15 MeV的总CLR=0.757。结果显示根据不同限光筒大小单独拟合CLR,与总CLR相比,在6 cm×6 cm、10 cm×10 cm和15 cm×15 cm限光筒,6 MeV的偏差分别为-0.80%,0.13%和1.2%,9 MeV的偏差分别为-1.20%,-0.27%和0.8%,12 MeV的偏差分别为-1.72%,-0.79%和0.26%,15 MeV的偏差分别为-1.72%,-0.79%和0.26%。
|
图 5 不同限光筒和不同角度下,蓝色和绿色通道信号比值(CLR) A.6 MeV;B.9 MeV;C.12 MeV;D.15 MeV Figure 5 The ratio of signal(CLR)between the blue and green channel for different applicator, energy and incident angle A. 6 MeV; B. 9 MeV; C. 12 MeV; D. 15 MeV |
5.CLR、kgain和剂量的不确定度
(1) CLR和kgain的不确定度:采用bootstrapping统计学方法重复抽样,6、9、12、15 MeV、6 MV和10 MV的CLR和kgain,差异均有统计学意义(tCLR=66.472、60.807、59.079、54.178、165.826、37.948,tkgain=204.782、211.429、221.640、212.818、309.633、109.466,P < 0.05)。由于不同照射条件下测量的校准系数(CLR,kgain)在应用自抽样法时会生成多个校准情况,存在校准系数的误差(不确定度)。结果显示,照射能量为6、9、12和15 MeV的CLR不确定度分别为0.65%、0.7%、0.8%和0.75%,kgain不确定度分别为1.5%、1.4%、1.4%和1.6%。照射能量为6和10 MV的CLR不确定度分别为0.4%和0.9%,kgain不确定度分别为0.8%和1.25%。
(2) 剂量的不确定度:根据公式(1)可知,CLR和kgain影响剂量的不确定度,在拟合情况下进行误差传递分析,CLR和kgain对剂量不确定度的影响,照射能量为6、9、12和15 MeV剂量的不确定度分别为2.96%、2.76%、2.76%和3.15%,照射能量为6和10 MV剂量的不确定度分别为1.59%和2.46%。
讨论非共面放疗在现代癌症治疗中仍占有重要地位,特别是在颅内肿瘤和肿瘤再次复发的情况下,大量研究为非共面放疗提供并优化了很多新颖的方法[14]。为了确保患者治疗安全,对非共面射野进行剂量验证尤为重要。常规验证非共面的剂量方法包括胶片法、电离室法等[15-16],但应用探测器时并未考虑探测器的角度响应问题。已有研究表明W2塑料闪烁体探测器对光子的切伦科夫辐射的修正有效[17-18],但并未提及电子束。由于光子束中产生的次级电子方向比较分散,而电子束的电子运动方向较为集中,因此电子束射野内的光纤长度和角度对产生的切伦科夫辐射影响比光子束更明显。本研究结果显示在射线出束方向较为一致的电子线照射下,经修正W2测得的信号不随角度变化而变化,光子束角度响应的线性均良好。因而W2在非共面放疗中可减少由于角度响应带来的剂量不确定性,测量剂量更加准确。
本研究剂量和剂量率线性结果与Galavis等[18]研究的一致,同时与使用其他闪烁体测量的结果相一致[19-20],W2剂量率读数的标准偏差在1%以内。在不同能量的光子线照射下,光信号沿光纤与射线夹角变化规律不同于电子线照射下所得结果。光子线中可能的切伦科夫贡献来源有两处:①在均整器和整个准直系统中产生的次级电子。②光子在光纤与闪烁体中产生的散射电子。由于存在这两种次级电子的原因,光子线中的电子角度散布较电子线更为发散,因此更容易出现当前观测的现象:在夹角超过某个临界值之后,W2中的光信号随夹角增大而增大,最终趋近于饱和数值。随着射野变大,入射电子的方向分布更为发散,因此临界夹角值随着射野增大而变小。进一步定量分析切伦科夫辐射对有效信号的影响需要结合蒙特卡罗仿真分离上述两种次级电子来源的贡献、以及量化不同射野对电子能量与方向分布的影响。
在不同能量和不同射野大小的电子线照射下,原始的光输出信号与不同角度的变化,W2的光信号均在相同的角度45°出现峰值,这与Beddar等[21]研究的电子束角度响应结果一致。由于在本实验中所用的夹角分辨率较低,因此未能观测到光信号达到峰值的角度随入射能量变化的现象。
在光子束和电子束不同能量和射野的照射条件下,SBlue和SGreen成一定比例,均保持线性,且一致性较好,本研究结果与文献[2]的角度依赖性结果一致,说明目前W2探测器所使用的双通道修正办法对消除电子束照射下的切伦科夫辐射信号同样有效。切伦科夫辐射在蓝光通道中的贡献比例几乎与能量无关,但与光纤/射束角度之间的夹角密切相关。切伦科夫辐射的光谱分布很广,覆盖了整个可见光范围。在塑料闪烁体发光的蓝色区域(400~480 nm)处较强。其可以进行光学过滤,限制闪烁体内与剂量率无关的光通过[20]。
综上,经双通道信号测量修正得到的信号不随角度变化而变化,即使是在高能电子束流下也成立。证实切伦科夫校准因子线性良好,该探测器可应用于立体定向放射治疗中的非共面射野剂量学测量。
利益冲突 所有研究者未接受任何不正当的职务或财务利益,对研究的独立性和科学性予以保证。
志谢 本研究接受中央高校基本科研业务费/北京大学临床医学+X青年专项(PKU2020LCXQ019)。
作者贡献声明 王美娇负责数据采集整理、结果分析、论文撰写;姚凯宁负责数据采集、整理和实验设计;李莎、刘卓伦负责前期数据采集工作;岳海振、蒋璠、吴昊指导实验进行和论文修改;王若曦负责实验设计和指导论文修改。
| [1] |
Qin Y, Gardner S, Huang Y, et al. SU-G-TeP2-08:evaluation of plastic scintillator detector for small field stereotactic patient-specific quality assurance[J]. Med Phys, 2016, 43(6): 3664-3664. DOI:10.1118/1.4957043 |
| [2] |
Galvin JM, Ezzell G, Eisbrauch A, et al. Implementing IMRT in clinical practice: a joint document of the American Society for Therapeutic Radiology and Oncology and the American Association of Physicists in Medicine[J]. Int J Radiat Oncol Biol Phys, 2004, 58(5): 1616-1634. DOI:10.1016/j.ijrobp.2003.12.008 |
| [3] |
Laub WU, Wong T. The volume effect of detectors in the dosimetry of small fields used in IMRT[J]. Med Phys, 2003, 30(3): 341-347. DOI:10.1118/1.1544678 |
| [4] |
Vahc YW, Chung WK, Park KR, et al. The properties of the ultramicrocylindrical ionization chamber for small field used in stereotactic radiosurgery[J]. Med Phys, 2001, 28(3): 303-309. DOI:10.1118/1.1350437 |
| [5] |
Palmans H, Andreo P, Huq MS, et al. Dosimetry of small static fields used in external photon beam radiotherapy: summary of TRS-483, the IAEA-AAPM international code of practice for reference and relative dose determination[J]. Med Phys, 2018, 45(11): e1123-e1145. DOI:10.1002/mp.13208 |
| [6] |
Mancosu P, Pasquino M, Reggiori G, et al. Dosimetric characterization of small fields using a plastic scintillator detector: a large multicenter study[J]. Phys Med, 2017, 41: 33-38. DOI:10.1016/j.ejmp.2017.03.024 |
| [7] |
Qin Y, Zhong H, Wen N, et al. Deriving detector-specific correction factors for rectangular small fields using a scintillator detector[J]. J Appl Clin Med Phys, 2016, 17(6): 379-391. DOI:10.1120/jacmp.v17i6.6433 |
| [8] |
Lacroix F, Archambault L, Gingras L, et al. WE-E-AUD-06:clinical prototype of a plastic water-equivalent scintillating fiber dosimeter matrix for IMRT QA applications[J]. Med Phys, 2007, 34(6): 2610-2611. DOI:10.1118/1.2761598 |
| [9] |
Archambault L, Beddar AS, Gingras L, et al. Water-equivalent dosimeter array for small-field external beam radiotherapy[J]. Med Phys, 2007, 34(5): 1583-1592. DOI:10.1118/1.2719363 |
| [10] |
Archambault L, Arsenault J, Gingras L, et al. Plastic scintillation dosimetry: optimal selection of scintillating fibers and scintillators[J]. Med Phys, 2005, 32(7): 2271-2278. DOI:10.1118/1.1943807 |
| [11] |
Beddar AS, Kinsella KJ, Ikhlef A, et al. A miniature "Scintillator-Fiberoptic-PMT" detector system for the dosimetry of small fields in stereotactic radiosurgery[J]. Ieee T Nucl Sci, 2001, 48(3): 924-928. DOI:10.1109/23.940133 |
| [12] |
Beddar AS, Mackie TR, Attix FH. Water-equivalent plastic scintillation detectors for high-energy beam dosimetry: Ⅰ. Physical characteristics and theoretical consideration[J]. Phys Med Biol, 1992, 37(10): 1883-1900. DOI:10.1088/0031-9155/37/10/006 |
| [13] |
Frelin AM, Fontbonne JM, Ban G, et al. Spectral discrimination of Cerenkov radiation in scintillating dosimeters[J]. Med Phys, 2005, 32(9): 3000-3006. DOI:10.1118/1.2008487 |
| [14] |
Smyth G, Evans PM, Bamber JC, et al. Recent developments in non-coplanar radiotherapy[J]. Br J Radiol, 2019, 92(1097): 20180908. DOI:10.1259/bjr.20180908 |
| [15] |
Smyth G, Evans PM, Bamber JC, et al. Dosimetric accuracy of dynamic couch rotation during volumetric modulated arc therapy (DCR-VMAT) for primary brain tumours[J]. Phys Med Biol, 2019, 64(8): 08N. DOI:10.1088/1361-6560/ab0a8e |
| [16] |
Wilson B, Otto K, Gete E. A simple and robust trajectory-based stereotactic radiosurgery treatment[J]. Med Phys, 2017, 44(1): 240-248. DOI:10.1002/mp.12036 |
| [17] |
Snyder JD, Sullivan RJ, Wu X, et al. Use of a plastic scintillator detector for patient-specific quality assurance of VMAT SRS[J]. J Appl Clin Med Phys, 2019, 20(9): 143-148. DOI:10.1002/acm2.12705 |
| [18] |
Galavis PE, Hu L, Holmes S, et al. Characterization of the plastic scintillation detector Exradin W2 for small field dosimetry[J]. Med Phys, 2019, 46(5): 2468-2476. DOI:10.1002/mp.13501 |
| [19] |
Carrasco P, Jornet N, Jordi O, et al. Characterization of the Exradin W1 scintillator for use in radiotherapy[J]. Med Phys, 2015, 42(1): 297-304. DOI:10.1118/1.4903757 |
| [20] |
Beddar AS, Mackie TR, Attix FH. Water-equivalent plastic scintillation detectors for high-energy beam dosimetry: Ⅱ. properties and measurements[J]. Phys Med Biol, 1992, 37(10): 1901-1913. DOI:10.1088/0031-9155/37/10/007 |
| [21] |
Beddar AS, Mackie TR, Attix FH. Cerenkov light generated in optical fibres and other light pipes irradiated by electron beams[J]. Phys Med Biol, 1992, 37(4): 925-935. DOI:10.1088/0031-9155/37/4/007 |
| [22] |
Wang LL, Klein D, Beddar AS. Monte Carlo study of the energy and angular dependence of the response of plastic scintillation detectors in photon beams[J]. Med Phys, 2010, 37(10): 5279-5286. DOI:10.1118/1.3488904 |
 2021, Vol. 41
2021, Vol. 41


