2. 山东第一医科大学(山东省医学科学院)预防医学科学学院(放射医学研究所), 济南 250012
2. College of Preventive Medicine, Shandong First Medical University(Shandong Academy of Medical Sciences), Jinan 250012, China
131I以碘化钠溶液口服的形式被用于治疗良性甲状腺疾病和分化型甲状腺癌,这种治疗方式已有60多年的历史[1-2]。131I为极易挥发的人工放射性核素,物理半衰期为8.025 d,衰变方式为β衰变,产生多能量γ射线,其中分支比最大的为81.5%,能量为364.5 keV[3]。131I在给药的操作过程易释放到工作场所中,患者留院期间对工作场所产生131I污染[4]。131I在人体内的生物半排期为12 d,131I以气态碘的形式被医务人员吸收,从而产生内照射。131I污染一直是倍受关注的辐射危害因素[5-7]。
国际原子能机构(IAEA)提出,长时间从事核医学治疗的医务人员或偶尔在核医学科工作但可能接受到显著职业照射的医务人员,在条件允许的情况下,须进行内照射个人监测[8]。其中内照射的个人监测方法主要包括体外直接测量、生物样品(尿液)分析以及空气采样分析[9]。目前,国内学者利用空气采样分析方法对接触131I治疗的医务人员进行内照射监测的研究还很少。本课题选取空气采样方法,收集了山东省6家医院核医学碘治疗工作场所中的131I气溶胶,通过现场询问接触碘治疗的医务人员在各场所的工作时长,拟定出每年(50周)各医院碘治疗医务人员在各工作场所的不同停留时间。监测出各场所131I气溶胶的活度浓度值、估算医务人员内照射剂量,对各医院具体情况,如场所布局、管理、医务人员的职业素养等内容进行调查并结合监测情况进行分析,为医院辐射防护管理提供参考依据。
材料与方法1. 研究对象:选取山东省内开展核医学131I治疗的三级甲等医院5家和三级乙等医院1家。碘治疗工作场所分为控制区和监督区两部分,收集各医院核医学科控制区的(最大服药量患者的)病房、患者通道、分装室(有/无自动分装仪)和远程操作给药室,以及监督区的办公室(医生和护士工作站)、医护通道等场所的131I气溶胶。
2. 主要仪器与材料:CF-1001-DIG型便携式大容量空气采样器(美国HI-Q公司)、tc-12碘盒(美国HI-Q公司)、GMX40P4-76型HPGe-γ能谱仪(美国ORTEC公司)。
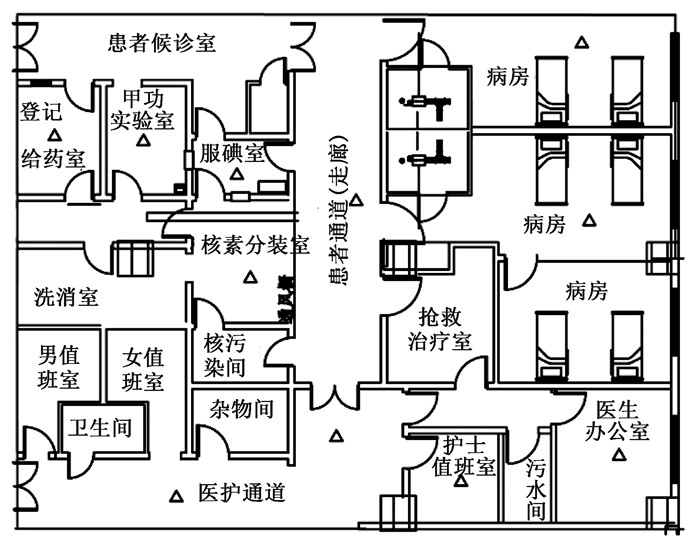
3. 样品采集:本次研究对6家医院进行编号A、B、C、D、E、F,采样时间分别为2、3、5、6、7月份。在药品分装完成30 min后进行采样,按顺序依次对分装间、远程操作给药室、患者通道、病房、护士工作站、医护通道、医生办公室进行采样,每次采集时间平均为60 min。因监测条件有限,仅收集到给药后12 h内的空气样品。采样点的选择主要考虑各医院放射工作人员居留区和场所主要污染区;采样点位于房间或走廊的中部,空气采样器通过固定支架放置在距离地面1.5 m处,采样器流量设置为(100 L/min)。测量点位见图 1。
|
注:△为监测点位 图 1 某医院核医学科131I空气采样点分布图 Figure 1 Distribution map of 131I air sampling points in the nuclear medicine department of a hospital |
4. 仪器校准与刻度
(1) 流量校准:CF-1001-DIG型便携式大容量空气采样器由北京市计量检测科学研究院提供校准,校准证书标号:EB21Z-EC100752。
(2) 131I效率刻度:由中国计量科学研究院电离辐射计量科学研究所生产提供的活性炭测碘效率校准源,校准源标号为2NHX210301。
5. 测量与计算:用无污染的保鲜膜将采样后的碘盒包装密封后带回实验室,校准源和待测样品均放置在距离HPGe-γ能谱仪探头中心5 cm的位置处,可忽略校准源133Ba γ射线符合相加对效率的影响(由供源单位提供)。131I的γ能谱的特征峰能量364.489 keV与校准源133Ba的γ能谱的特征峰能量356.013 keV很接近,把133Ba的356.013 keV效率作为131I的效率[7]进行样品活度浓度计算。根据WS/T 184中的计算公式[10],对样品中131I的活度浓度进行计算。
133Ba效率计算公式:
| $ \mathit{\varepsilon } = \frac{{{N_Y}/{t_Y} - {N_b}/{t_b}}}{{A \times P}} $ | (1) |
| $ A = {A_0} \times \mathit{e}\frac{{ - {\rm{ln}}2 \times t}}{{{{\rm{T}}_{1/2}}}} $ | (2) |
式中,ε为校准源某特征γ射线全能峰的探测效率;NY为校准源某特征γ射线全能峰计数;tY为校准源测量活时间,s;Nb为某特征γ射线全能峰对应的本底计数;tb为本底测量活时间,s;A为校准源某核素测量时的活度,Bq;P为相应能量γ射线发射概率。其中,在监测样品测量前测量本底,发现本底为0,未受污染,继续测量当天同批监测样品,测量结束后继续测量本底,发现未受污染。本次研究所用样品均按此方法进行测量,本底均未受到污染。131I活度浓度计算公式:
| $ {C_t} = \frac{{{N_{\rm{s}}}/{t_{\rm{s}}} - {N_{\rm{b}}}/{t_{\rm{b}}}}}{{\mathit{\varepsilon } \times P \times V \times F}} $ | (3) |
式中,Ct为样品中131I测量时的活度浓度,Bq/m3;NS为考核样品某特征γ射线全能峰计数;tS为考核样品测量活时间,s;Nb为某特征γ射线全能峰相应的本底计数;tb为本底测量活时间,s;V为考核样品的体积,m3;F为可能的测量修正系数:K1、K2。
衰变校正系数:若样品采样时间、放置待测时间和测量时间均大于待测核素的半衰期,要对核素在各时间段的衰变进行校正,从样品采集开始到样品测量开始之间的校正见式(4),样品在测量阶段的校正见式(5)。
| $ {K_1} = {{\rm{e}}^{ - \frac{{{\rm{ln}}(2) \times t}}{{{T_{1/2}}}}}} $ | (4) |
式中,K1为样品采集时到样品测量时的衰变校正因子;t为样品采集时到样品测量时的时间差,s;T1/2为核素半衰期,s。
| $ {K_2} = \frac{{{T_{1/2}}}}{{{\rm{ln}}(2) \times {t_{\rm{r}}}}} \times (1 - {{\rm{e}}^{ - \frac{{{\rm{ln}}(2) \times {t_{\rm{r}}}}}{{{T_{1/2}}}}}}) $ | (5) |
式中,K2为样品测量过程中的衰变校正因子;tr为样品测量的实时间,s。
内照射剂量估算公式[9]:
| $ {\mathit{I}_j} = {C_j}BT $ | (6) |
式中,Ij为放射性核素的年摄入量,Bq;Cj为固定空气采样器监测的131I的活度浓度,Bq/m3;B为呼吸率,m3/h,选取1.2 m3/h,以考虑医务人员较高的体力活动;T为监测周期内工作场所停留的总有效时间,h,年工作时间假设为50周。
| $ E(\mathit{\tau }) \approx {A_0}e(\mathit{\tau }) $ | (7) |
式中,E(τ) 为待积有效剂量,Sv;A0为放射性核素131I的摄入量;e(τ)为放射性核素单位摄入量的待积有效剂量,Sv/Bq;当131I的空气动力学活动中值(AMAD)为5 μm时,e(τ)为1.1×10-8 Sv/Bq。
6. 6家医院碘治疗工作场所的基本情况:6家医院(分别标记为A、B、C、D、E、F)均有独立通风系统,且通风情况良好。A~E医院的放射性药物为自动分装,F为手动分装。6家医院的病房数量依次为9、4、11、10、13、1,调查期间收治的甲状腺癌患者依次为9、5、16、11、2、2人,其中C、E两家医院还收治了甲亢患者8、20人。除F院外,其余5家医院监督区和控制区在同一楼层。
结果1. 碘治疗控制区131I活度浓度结果:结果见表 1。分装间131I活度浓度范围为1.1×102~1.81×103 Bq/m3,平均为6.06×102 Bq/m3,E院最高;远程操作给药室131I活度浓度范围为0.33×102~1.28×103 Bq/m3,平均为6.63×102 Bq/m3,E院最高;患者通道的131I活度浓度范围为1.80×102~2.94×103 Bq/m3,平均为1.08×103 Bq/m3,C院最高;甲状腺癌病房的131I活度浓度范围为8.31×102~2.08×103 Bq/m3,平均为1.60×103 Bq/m3,C院最高。C医院患者通道给药当天空气中131I的活度浓度比病房高,考虑是两家医院的患者中午和傍晚会在走廊散步所致。
|
|
表 1 6家医院碘治疗控制区不同采样地点空气中131I的活度浓度(Bq/m3) Table 1 Activity concentration of 131I in air in iodine treatment controlled area of 6 hospitals(Bq/m3) |
2. 碘治疗监督区131I的活度浓度结果:结果见表 2。护士工作站131I活度浓度范围为3.64~82 Bq/m3,平均浓度为39.44 Bq/m3,D院最高;(医生办公室门前)医护通道131I活度浓度范围为9.82~ 2.62×102 Bq/m3,平均浓度为192.97 Bq/m3,C院最高;医生办公室的131I活度浓度范围为5.44~1.87×102 Bq/m3,平均浓度为44.71 Bq/m3,E院最高。F院医生办公室空气中131I浓度比在同一楼层的其他5家医院的平均浓度低。C院与病房入口最接近的医护通道空气中131I的活度浓度是6家医院最高为262 Bq/m3。D院护士工作站与控制区相通(一门之隔,经常开门方便工作),其护士工作站空气中131I的活度浓度是6家医院最高。
|
|
表 2 6家医院碘治疗监督区不同采样地点空气中131I的活度浓度(Bq/m3) Table 2 Activity concentration of 131I in air in iodine treatment and supervised areas of 6 hospitals (Bq/m3) |
3. 医务人员内照射剂量估算结果:6家医院的给药量范围为7.4~70.1 GBq(表 3),其中A院与E院具有相似的给药量,E院分装间给药当天空气中131I的活度浓度比A医院的浓度高16倍。假设医务人员在核医学工作场所停留时空气中131I的活度浓度全年保持不变,采取保守计算的方式,选取表 1,2的测量数据,计算年摄入量和待积有效剂量。6家医院医务人员的待积有效剂量范围为0.07~5.68 mSv,其中医生的平均待积有效剂量为1.25 mSv,护士的平均待积有效剂量为1.26 mSv,均未超过国家标准所规定的剂量限值20 mSv[11]。A、E、F 3家医院的分装碘罐和电脑操作给药均由医生进行,在分装间和给药室停留的时间较长(表 3),医生的待积有效剂量分别为:0.21、5.68和0.84 mSv;B、C、D 3家医院的分装和电脑操作给药以及病房更换被服均由护士进行,护士的待积有效剂量分别为:0.63、1.24和2.50 mSv,均大于所在医院的医生剂量,其中D医院护士待积有效剂量是医生的35倍;E医院医生待积有效剂量比本院的护士高4倍。
|
|
表 3 各医院核医学科医务人员年摄入量和待积有效剂量估算 Table 3 Estimates of annual intake and committed effective dose to medical staff of nuclear medicine department of hospitals |
讨论
患者住院期间,病房和患者通道空气中131I浓度最大,其中B、C医院的甲状腺癌病房空气中131I活度浓度均比严源等[12]测量的7.15×102Bq/m3高一个量级,主要原因是B、C两家医院比其所测医院的给药量高1个量级,由此也能证明,病房空气中131I浓度的大小与给药量大小有一定关系。6家医院分装间给药当天131I的平均活度浓度大于张震等[13]对4家医院测量的最大值320 Bq/m3,同样大于王红波[14]所测的最大值244 Bq/m3。其主要原因是本研究所测医院与张震等[13]、王红波[14]所测医院的131I药量、给药时间、通风强度的不同导致的;另外,E院分装间131I浓度比其他5家医院高出1个量级,怀疑是由于医务人员的操作不当导致的源项污染(医生不重视,经常分装、给药过程中不佩戴口罩和防污手术服)。Brudecki等[15]测得分装间在给药当天空气中131I的活度浓度为(492±4)Bq/m3。Carneiro等[16]在分装间打开通风柜作业时,距离1 m处测得空气中131I平均浓度为7.4 Bq/m3,最高为416.67 Bq/m3,两者均低于本次测量的平均值,主要原因在于给药量的不同以及本省医务人员存在为简化流程而忽略使用通风柜的情况。另外,张震等[13]报道,利用自动分装给药,空气中131I的活度浓度要远小于手动分装,本次实验只有F院属于手动分装,测量数值偏低的主要原因为给药量是6家医院最少的,仅有200 mCi(1 Ci=3.7×1010 Bq),只有1间病房,2名患者,并未体现出上述结论。
关于监督区各工作场所空气中131I的活度浓度的报道不多。本次监测各医院监督区3个工作场所的平均浓度均与王红波[14]利用个体采样器测得的结果相似,其医护通道空气中131I的活度浓度163.55 Bq/m3,护士站64.58 Bq/m3,医生办公室55.80 Bq/m3。其中,个别医院污染程度高主要与场所布局、医务人员的习惯相关。如C院的护士总会在中午和傍晚为患者通道开门通风,E院的护士总会从医生办公室进出患者通道,除了B院和F院外,其他医院的医生办公室和控制区在同一楼层并且距离较近等。Brudecki等[15]发现波兰某医院护士站空气中131I的平均活度浓度为(174±25)Bq/m3,因为其护士站在病房走廊,可能代表病房和患者通道的空气中131I的活度浓度平均值,与D院护士工作站(与控制区患者通道只有一门之隔)的情况大抵相同,虽不在走廊中,浓度也高于其余4家医院。
本次调查估算出的待积有效剂量仅代表没有穿戴任何防护性口罩的医务人员在各工作场所停留时,因吸入131I的气溶胶所产生的内照射剂量;且为了保守计算,医务人员的内照射剂量估算是依照工作内容完成度最高的医生和护士进行的,故代表的是碘治疗场所可能接受剂量最高的职业,而不是医务人员的个体水平。王红波[14]对核医学工作人员估算的待积有效剂量范围为0.01~3.06 mSv,平均值为0.86 mSv,本研究结果与之相似。张震等[13]估算的待积有效剂量最大值与平均值分别为0.44和0.18 mSv。Brudecki等[17]对波兰核医学医务人员进行监测发现,医生的待积有效剂量范围为0.02至0.8 mSv,均小于本研究测量的结果。原因主要是医务人员的工作负荷不同且在控制区以及有污染的监督区进行较长时间停留,而张震等[13]和Brudecki等[17]并未将监督区的131I气溶胶污染计算在内。Brudecki等[15]得出医生进行分装操作,相比护士,待积有效剂量要高2倍(医生平均1.2 mSv,护士0.56 mSv),而E医院医生比护士高4倍,可能与E医院分装间和给药室受到污染和工作耗时较久有关。
在准备患者出院时,应有相应的标准来判断患者体内的放射性活度是否满足出院条件。IAEA给出的出院标准为患者体内的131I活度不得超过1.11 GBq, 或者距离病患1 m时外照射的剂量率 < 30 μSv/h[18]。经调查发现,B、D、E 3家医院每天监控患者体内碘活度,在 < 25 μSv/h时办理出院,A、C、F 3家医院仅凭经验判断,这些细节反映了各医院在甲状腺癌患者入院治疗和准许出院的相关制度和措施上仍存在问题。
综上,各医院核医学科碘治疗的工作负荷大,工作场所仍存在不可忽视的131I气溶胶污染现象,医务人员亟需普及辐射知识并加强防护。例如在131I治疗的封闭场所内,工作人员须穿戴放射性污染防护服,气溶胶防护口罩,而无需使用铅防护用品[19];碘治疗场所需拥有良好的通风换气环境,保证控制区的负压通风环境并减少其与监督区的空气流通;尽量避免在控制区附近办公等。应面向全国各地区核医学科开展内照射监测,探索更加合理的防护标准和方法。
利益冲突 无
作者贡献声明 孙伟航负责现场调查与测量、数据分析与论文撰写;张琳、牛菲负责项目的协调与论文写作的指导,参与现场调查与测量;李甜甜、闵楠、杨淑慧、刘芳参与现场调查与测量;许家昂负责测量方法的指导;朱建国负责测量方法的指导,项目的协调与论文写作的指导
| [1] |
Bento J, Teles P, Neves M, et al. Study of nuclear medicine practices in Portugal from an internal dosimetry perspective[J]. Radiat Prot Dosim, 2012, 149(4): 438-443. DOI:10.1093/rpd/ncr319 |
| [2] |
Paquet F, Bailey MR, Leggett RW, et al. ICRP Publication 137. Occupational intakes of radionuclides: Part 3[J]. Ann ICRP, 2017, 46(3-4): 1-486. DOI:10.1177/0146645317734963 |
| [3] |
Matsuo K, Machida H, Takiuchi T, et al. Role of hysterectomy and lymphadenectomy in the management of early-stage borderline ovarian tumors[J]. Gynecol Oncol, 2017, 144(3): 496-502. DOI:10.1016/j.ygyno.2017.01.019 |
| [4] |
Thies ED, Tanase K, Maeder U, et al. The number of 131I therapy courses needed to achieve complete remission is an indicator of prognosis in patients with differentiated thyroid carcinoma[J]. Eur J Nucl Med Mol Imaging, 2014, 41(12): 2281-2290. DOI:10.1007/s00259-014-2851-2 |
| [5] |
Mróz T, Brudecki K, Mietelski JW, et al. Medical activated charcoal tablets as a cheap tool for passive monitoring of gaseous 131I activity in air of nuclear medicine departments[J]. J Radioanal Nucl Chem, 2018, 318(1): 723-726. DOI:10.1007/s10967-018-6107-7 |
| [6] |
刘明, 耿建华, 梁颖. 核医学治疗分化型甲状腺癌场所空气中131I浓度的研究进展[J]. 中国辐射卫生, 2019, 28(6): 734-736. Liu M, Geng JH, Liang Y. Research progress of 131I concentration in air in nuclear medicine for differentiated thyroid carcinoma[J]. Chin J Radiat Health, 2019, 28(6): 734-736. DOI:10.13491/j.issn.1004-714x.2019.06.036 |
| [7] |
王所富, 於国兵, 顾先宝, 等. 某医院核医学科不同区域不同形态131I的分布研究[J]. 标记免疫分析与临床, 2019, 26(6): 1011-1015. Wang SF, Yu GB, Gu XB, et al. Distribution of different forms of 131I in different areas of nuclear medicine in a hospital[J]. Labeled Immunoassays Clin Med, 2019, 26(6): 1011-1015. DOI:10.11748/Bjmy.issn.1006-1703.2019.06.028 |
| [8] |
International Atomic Energy Agency. Safety Series No. 115: International basic safety standards for protection against ionizing radiation and for the safety of radiation sources[R]. Vienna: IAEA, 1996.
|
| [9] |
国家卫生健康委员会. GBZ 129-2016职业性内照射个人监测规范[S]. 北京: 中国标准出版社, 2016. National Health Commission of the People's Republic of China. GBZ 129-2016 Personal Monitoring specification for occupational internal exposure[S]. Beijing: Standards Press of China, 2016. |
| [10] |
中华人民共和国卫生部. WS/T 184-2017空气中放射性核素的γ能谱分析方法[S]. 北京: 中国标准出版社, 2017. Ministry of Health of the People's Republic of China. WS/T 184-2017 γ-spectral analysis of radionuclides in air according to the Health industry standard[S]. Beijing: Standards Press of China, 2017. |
| [11] |
国家质量监督检验检疫总局. GB 18871-2002电离辐射防护与辐射源安全基本标准[S]. 北京: 中国标准出版社, 2003. General Administration of Quality Supervision, Inspection and Quarantine of the People's Republic of China. GB 18871-2002 Basic standards for protection against ionizing radiation and for the safety of radiation sources[S]. Beijing: Standards Press of China, 2003. |
| [12] |
严源, 金潇, 邵明刚. I-131治疗场所放射性废气排放源项调查与评价[J]. 同位素, 2019, 32(6): 388-394. Yan Y, Jin X, Shao MG. I-131 radioactive emissions source term investigation and evaluation of treatment places[J]. J Isot, 2019, 32(6): 388-394. DOI:10.7538/tws.2018.youxian.068.Youxian.068 |
| [13] |
张震, 张奇, 拓飞, 等. 4家核医学工作场所空气中131I活度浓度的监测[J]. 工业卫生与职业病, 2013, 39(3): 185-187. Zhang Z, Zhang Q, Tuo F, et al. Monitoring of 131I activity concentration in the air of four nuclear medicine workplaces[J]. Ind Health Occup Dis, 2013, 39(3): 185-187. |
| [14] |
王红波. 核医学科工作人员职业性内照射研究[D]. 北京: 中国疾病预防控制中心, 2017. Wang HB. Study on occupational internal exposure of nuclear medicine staff[D]. Beijing: Chinese Center for Disease Control and Prevention, 2017. |
| [15] |
Brudecki K, Szczodry A, Mróz T, et al. Measurement of 131I activity in air indoor Polish nuclear medical hospital as a tool for an internal dose assessment[J]. Radiat Environ Biophys, 2018, 57(1): 77-82. DOI:10.1007/s00411-017-0724-3 |
| [16] |
Carneiro LG, de Lucena EA, Sampaio Cda S, et al. Internal dosimetry of nuclear medicine workers through the analysis of (131)I in aerosols[J]. Appl Radiat Isot, 2015, 100: 70-74. DOI:10.1016/j.apradiso.2014.11.021 |
| [17] |
Brudecki K, Kowalska A, Zagrodzki P, et al. Measurement of 131I activity in thyroid of nuclear medical staff and internal dose assessment in a Polish nuclear medical hospital[J]. Radiat Environ Biophys, 2017, 56(1): 19-26. DOI:10.1007/s00411-016-0674-1 |
| [18] |
International Atomic Energy Agency. Safety standards series No. GSR Part 3: Radiation protection and safety of radiation sources: international basic safety standards for protection against ionizing radiation[R]. Vienna: IAEA, 2014.
|
| [19] |
国家卫生健康委员会. GBZ 120-2020核医学放射防护要求[S]. 北京: 中国标准出版社, 2020. National Health Commission of the People's Republic of China. GBZ 120-2020 Requirements for radiation protection in nuclear medicine[S]. Beijing: Standards Press of China, 2020. |
 2021, Vol. 41
2021, Vol. 41


