心脏冠状动脉CT血管成像(coronary CT angiography, CCTA),可无创性的实现对心脏冠状动脉的三维立体评估,是临床中冠状动脉相关疾病筛查诊断的首选方案[1]。但随着CCTA在临床上使用率的快速增长,其电离辐射相关危险也成为临床关注问题,辐射危险的评估需要使用受检者的器官剂量和个体有效剂量[2],对这些患者个体化辐射相关计量指标快速估算将有助于临床决策及患者辐射危险管理。体型特异性剂量估算值(size specific dose estimation,SSDE)自2011年美国物理师协会204工作组报告(AAPM work group 204)中提出后[3],目前已成为被广泛认可的用于体部CT扫描中辐射剂量评估的计量指标[4]。近年来多项研究都报道了SSDE与受检者器官剂量的相关性,提示SSDE可能用于估算个体器官剂量[5-7]。本研究旨在探讨将SSDE用于冠状动脉CTA中估算患者器官剂量和个体有效剂量的可行性。
资料与方法 1、临床资料回顾性分析华中科技大学同济医学院附属协和医院2021年1月10日至2月10日间CCTA病例421例。平均年龄(58.5±12.8)岁,范围为18~89岁;其中男性244例,(56.5±13.3)岁,女性177例,(61.3±11.5)岁。病例排除标准:冠状动脉搭桥术后,起搏器植入,以及由于金属伪影可能造成辐射剂量估算不准的病例。
2、设备与方法所有病例均使用德国西门子第3代双源SOMATOM Force CT进行扫描,探测器准直器为0.6 mm ×192。扫描方案为前瞻性心电门控触发轴扫模式, 管电压使用CARE kV根据患者定位图自动选择,范围为70~120 kV;管电流使用Care-Dose 4D智能实时调制。扫描触发方式为团注追踪法(bolus-tracking)。高压注射器使用三腔式高压注射器(CT MOTION, Ulrich medical)。对比剂使用碘迈伦(400 mg/ml),注射流速为2.5~4.5 ml/s。对比剂注射量=(扫描时间+经验值7 s)×注射流速,随后同速注射生理盐水30 ml。
3、SSDE使用患者水等效直径(WED)作为患者体型参数,通过WED计算SSDE[8],公式如下:
| $ {\rm{SSDE}} = {\rm{CTD}}{{\rm{I}}_{{\rm{vol}}}} \times f\left( {{\rm{WED}}} \right) $ | (1) |
式中,CTDIvol为容积CT剂量指数(冠状动脉CTA扫描协议采用32 cm体模);f(WED)为美国医学物理师协会(AAPM)220工作组[8]报告中给出的WED所对应的转换因子。WED通过Radimetrics(Radimetrics Inc, Bayer)平台利用患者定位图计算[9]。
4、器官剂量与个体有效剂量采用Monte Carlo模拟法计算的器官剂量和个体有效剂量作为参考标准值。器官剂量计算方法为:通过Radimetrics模型库中的标准化模拟人体数学模型,基于性别和定位图,将患者映射到对应体型的数字体模,使用Monte Carlo模拟器进行估算;其中器官剂量为冠状动脉扫描中主要曝光器官,包括心脏、肺脏、肝脏及女性患者的乳腺。
个体有效剂量使用患者器官剂量和国际放射防护委员会(ICRP)103号报告[10]中的组织敏感权重系数,按如下公式计算:
| $ 个体有效剂量 = {\sum _{{\rm{organs}}}}器官剂量 \times 组织权重因子 $ | (2) |
通过线性拟合推算转换系数a和b,以通过SSDE估算器官剂量和个体有效剂量,公式如下:
| $ 估算值 = a \times SSDE - b $ | (3) |
以Monte Carlo模拟法计算的辐射剂量值为参考值,计算SSDE估算的剂量值与参考值的相对误差:
| $ 相对误差 = \frac{{估算值-参考值}}{{参考值}} \times 100\% $ | (4) |
数据统计分析使用R语言开源软件。计量资料符合正态分布,以x±s表示。使用线性回归分析SSDE与器官剂量和个体有效剂量的关系,P < 0.05为差异有统计学意义。基于相对误差计算平均误差以评估准确性。
结果 1、一般结果本研究共纳入421例研究对象。患者体型参数WED平均值为(24.5±2.2) cm,CTDIvol平均值为(16.8±8.7) mGy,DLP平均值为(195.5±104.2) mGy·cm,SSDE平均值为(20.8±8.8) mGy。
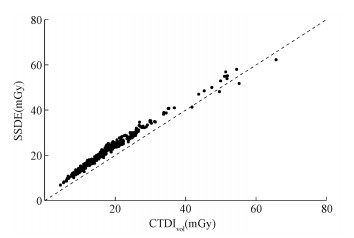
2、对比SSDE与CTDIvol图 1中,大部分数据都分布在虚线左上方,表示大部分患者的SSDE值大于CTDIvol。
|
注:图中虚线为Y=X参考线 图 1 对比SSDE与CTDIvol Figure 1 Comparison of SSDE and CTDIvol |
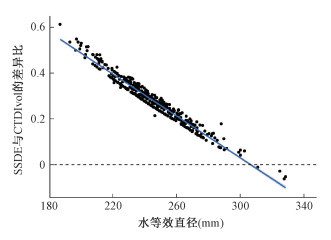
图 2中可见,SSDE与CTDIvol之间的差异比与WED有强相关性(R2=0.96);患者体型越小,SSDE与CTDIvol之间的差异越大。同时对于体型较大患者(WED>300),SSDE与CTDIvol之间的差异值<0,表示CTDIvol值大于SSDE。
|
注:图中蓝线为回归线,虚线为SSDE与CTDIvol无差异的参考线 图 2 SSDE~CTDIvol之间的差异比与水等效直径的关系 Figure 2 The relationship between the difference of SSDE-CTDIvol and water equivalent diameter |
3、器官剂量
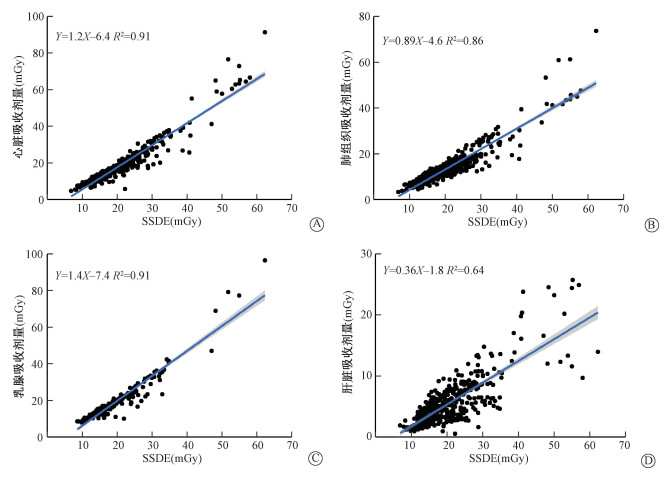
各器官剂量平均值为心脏(18.7± 11.1) mSv、肺脏(14.0±8.4) mSv、肝脏(5.7±3.9) mSv、乳腺(20.1±12.2) mSv。SSDE与各器官剂量的线性相关分析结果见图 3,有统计学意义(R2=0.91、0.86、0.91、0.64,P<0.05)。
|
注:图中公式为通过SSDE估算器官剂量的线性拟合公式:器官剂量=a×SSDE-b;图中蓝线均为线性拟合回归线 图 3 器官剂量与SSDE的线性相关性 A. 心脏剂量与SSDE; B. 肺脏剂量与SSDE; C. 乳腺剂量与SSDE; D. 肝脏剂量与SSDE Figure 3 The linear relationship between organ doses and SSDE A. Heart dose and SSDE; B. Lung dose and SSDE; C. Breast dose and SSDE; D. Liver dose and SSDE |
4、个体有效剂量
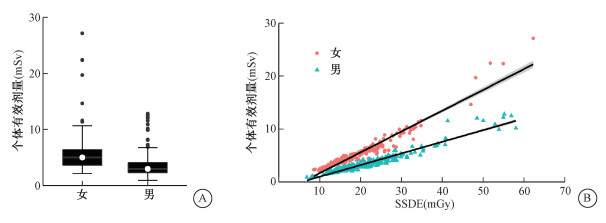
421例患者的个体有效剂量平均值为(4.4±2.9) mSv。分布见图 4,冠状动脉CTA检查中,女性的个体有效剂量高于男性。SSDE与个体有效剂量呈线性相关(男R2=0.92, 女R2=0.93,P < 0.05)。
|
注:图中男性数据用绿色表示,女性数据用红色表示,B图中黑线均为线性回归线 图 4 个体有效剂量 A.不同性别间个体有效剂量分布对比; B. SSDE与个体有效剂量的关系 Figure 4 Specific effective dose A. The sex-specific distribution of effective dose; B. The relationship between SSDE and specific effective dose |
5、使用SSDE估算器官剂量和个体有效剂量的转换系数
根据式(3)分别推导了转换系数a和b,以及估算值的平均误差(表 1)。
|
|
表 1 使用SSDE估算器官剂量和个体有效剂量的转换系数 Table 1 The conversion coefficients for estimation of effective dose with SSDE |
讨论
本研究希望能够定义一个更为便捷可行的方法对冠状动脉CTA检查中患者的个性化剂量指标:器官剂量和个体有效剂量进行估算。首先验证了冠状动脉CTA检查中,SSDE与患者受照射的器官剂量和个体有效剂量存在线性相关,然后通过线性回归分析推导出了使用SSDE估算器官剂量和个体有效剂量的转换系数。通过该方法,可以使用SSDE和相应转换系数快速估算冠状动脉CTA检查中患者个体化辐射剂量水平,这将有助于临床决策中对患者辐射相关危险的评估和扫描协议优化。
冠状动脉CT检查中器官吸收剂量还不能实时物理测量,目前最为准确的方法为通过Monte Carlo模拟进行估算[11],所以本研究中采用该方法作为器官剂量参考标准。但Monte Carlo模拟需要配套的硬件和软件平台,配置较为复杂,在常规临床工作环境下有一定操作难度,所以更为便捷的估算方法是目前研究热点。早期研究报道了通过设备输出剂量参数CTDIvol进行器官剂量估算的方法[12]。但是CTDIvol与人体真实吸收剂量有一定偏差,Kidoh等[5]对比CTDIvol和SSDE评估CCTA辐射剂量研究中,指出SSDE是反映患者实际吸收剂量更为合适的指标,通过对比CTDIvol和SSDE后,发现CTDIvol会低估普通及小体型成年患者的辐射剂量。本研究将SSDE与CTDIvol进行对比,同样发现大部分患者的CTDIvol低于SSDE,CTDIvol会低估其辐射剂量水平;且患者WED越小,CTDIvol对其辐射计量低估程度越大;此外亦发现WED>30 cm的患者数据CTDIvol均高于对应SSDE,可能提示CTDIvol对于大体型患者实际吸收剂量的高估。这是因为患者体型以及身体构成差异都会影响射线衰减效应,而改变人体对射线的吸收程度,体型较大患者体内实际吸收剂量会更低。所以,考虑患者体型差异因素的SSDE被认为更能真实反映受检者的真实吸收剂量[7]。本研究在此基础上,进一步探讨使用SSDE估算CCTA中患者的相关器官剂量。
虽然SSDE可以更真实地反映患者的吸收剂量,但该数值并不等同于被照射的各器官组织的吸收剂量。本研究对比发现,SSDE比完全照射的器官剂量(心脏和乳腺)平均高出约6.7%,比部分被照射的器官剂量(肺和肝脏)平均高出约2倍。但通过将SSDE分别与各器官进行线性回归分析后,证明SSDE与各器官剂量之间存在线性相关性,说明SSDE是可用于通过线性拟合的方法估算这些器官的吸收剂量。同时结果显示,各器官与SSDE的线性相关程度与其在照射视野(FOV)中所分布的位置有关:心脏和乳腺这两个分布在扫描范围之内的器官与SSDE的存在极高相关性(R2=0.91,P < 0.05),肺脏大部分在扫描范围内相关性较强(R2=0.86,P < 0.05),均高于处在扫描范围边缘的肝脏(R2=0.64,P < 0.05)。对比各器官剂量估算的平均误差,发现SSDE评估完全在FOV内的器官的准确性高于被部分照射的器官。对比其他研究,Moore等[7]探讨了SSDE评估胸腹CT检查中器官吸收剂量的工作,亦发现使用SSDE估算完全处于FOV内器官的吸收剂量准确性更高,平均器官剂量误差<10%,这与本研究的评估误差结果相似。所以CCTA中,对于照射视野内器官可以使用SSDE精准估算,被部分照射的器官剂量可在一定误差范围进行估算。
个体有效剂量用于在放射防护工作中评估患者辐射危险[10]。若可在正式扫描前提前预估患者的个体有效剂量将有助于技师评估患者风险并优化扫描协议,具有临床意义。目前还没有使用SSDE估算冠状动脉CTA中个体有效剂量的相关报道。本研究结果显示,SSDE与有效剂量存在强线性相关性(男,R2=0.92;女,R2=0.93),提示冠状动脉CTA中使用SSDE估算个体有效剂量是可行的。对比同样通过线性回归方法使用SSDE估算患者个体有效剂量的工作,Martin等[13]报道了该方法在胸腹盆CT扫描中的应用,显示不同性别之间的转换系数值(转换系数a)相近,这与本研究不同。本研究中女性的转换系数值约为男性的两倍。这可能与本研究对象的扫描范围相关。本研究中,冠状动脉CTA为针对心脏的局部小范围扫描,被完全照射器官仅包括心脏和乳腺,这两者对个体有效剂量贡献权重最大,考虑到乳腺较高的吸收剂量和辐射敏感性,故最终个体有效剂量会表现出明显性别差异;而Martin等[13]的研究中扫描范围为整个胸腹部,照射视野内涵盖众多器官,其中女性乳腺对于个体有效剂量的权重被弱化,所以最终的个体有效剂量分布没有明显性别之间差异。该研究结果显示,使用SSDE估算个体有效剂量的平均误差<5%,与本研究结果一致(平均误差<3%),亦验证了SSDE估算个体有效剂量的可行性。
目前,临床中常用的估算冠状动脉CTA个体有效剂量的方法是剂量长度乘积(DLP)乘以胸部K因子,该算法是基于早期单排CT数据推导,对于目前冠状动脉CTA常使用64排及以上的多排CT,该算法会低估患者个体有效剂量[14]。此外冠状动脉CTA中个体有效剂量存在性别差异,如本研究发现相同水平SSDE情况下,女性的个体有效剂量会高于男性,而K因子并未考虑性别差异。所以本研究中基于患者的SSDE值,且根据性别使用不同转换系数的估算方法可能是临床中估算个体有效剂量的一种更为准确的替代方法。
从放射防护角度考虑,基于SSDE估算器官剂量和个体有效剂量是实用且非常有临床意义的。根据美国物理师协会(AAPM)报告的标准化方法[3],在获取CT扫描定位图后就可以得到患者体型信息(如患者有效直径或WED),即可根据预估CTDIvol计算出SSDE。所以,未来CT厂家有能力做到将SSDE作为每次扫描的常规辐射参数展示到操作界面中,与目前使用CTDIvol相似;这样在每次冠状动脉CTA检查中得到定位图后就可以实现患者器官剂量和个体有效剂量的实时估算,在正式扫描前即可对患者的辐射危险进行精准评估,帮助扫描协议优化和降低辐射危险。
本研究也存在一定局限性。首先,本研究为单中心研究,数据来源相对单一。未来需要使用不同设备的数据对本研究的方法进行泛化验证,但目前临床上双源CT在冠状动脉CTA检查的使用率较高,对于这些情况本方法可以适用。其次,计算WED的标准方法为使用横断位图像,而本研究中使用定位图计算WED,是因为本研究的目的是在患者正式扫描前计算出SSDE;同时AAPM 220报告中亦指出,基于定位图计算WED是可行的,误差<20%。最后本研究对象均为成人,所以该方法不能使用于儿童,未来需要进一步通过扩大研究对象所涵盖的人群进一步验证。
随着放射防护意识的提高,对CT检查进行优化以达到诊断图像质量和辐射危险之间正确平衡的需求已引起广泛关注,故需要更多个性化反映患者辐射剂量及风险的参数辅助临床决策。本研究中展示了在冠状动脉CT检查中通过少量参数快速估算患者个体化辐射剂量的可行性:既通过SSDE和相应的转换系数,可快速计算被照射器官剂量和个体有效剂量,有助于临床工作中实现患者辐射剂量及风险的个性化评估和精准管理。
利益冲突 本研究具有独立性与科学性,研究设计、收集、分析和文章撰写均由本文的共同作者完成,共同作者间无利益冲突关系。本研究与商业机构间无财务往来
作者贡献声明 聂壮设计研究方案、撰写论文;雷子乔、余建明协助图像分析和文稿审阅;杨明负责图像采集
| [1] |
Nicol ED, Feuchtner GM, Villines TC. Following the evidence: The pre-eminent role of coronary CT angiography in 2021[J]. J Cardiovasc Comput Tomogr, 2021, 15(3): 285-287. DOI:10.1016/j.jcct.2021.03.009 |
| [2] |
National Research Council. Health Risks from Exposure to Low Levels of Ionizing Radiation: BEIRVII_Phase 2[M]. Washington: National Academies Press, 2006.
|
| [3] |
American Association of Physicists in Medicine. AAPM Report No. 204: size-specific dose estimates (SSDE) in pediatric and adult body CT examinations[R]. Alexandria: AAPM, 2011.
|
| [4] |
余佩琳, 范文亮, 雷子乔, 余建明. 不同年龄段儿童与成人肺部CT扫描体型特异性剂量估计[J]. 中华放射医学与防护杂志, 2019, 39(1): 26-30. Yu PL, Fan WL, Lei ZQ, Yu JM. Size-specific dose estimation for chest CT examination in pediatric and adult patients[J]. Chin J Radiol Med Prot, 2019, 39(1): 26-30. DOI:10.3760/cma.j.issn.0254-5098.2019.01.006 |
| [5] |
Kidoh M, Utsunomiya D, Oda S, et al. Validity of the size-specific dose estimate in adults undergoing coronary CT angiography: comparison with the volume CT dose index[J]. Int J Cardiovasc Imaging, 2015, 31(Suppl 2): 205-211. DOI:10.1007/s10554-015-0782-z |
| [6] |
Westra SJ, Li X, Gulati K, et al. Entrance skin dosimetry and size-specific dose estimate from pediatric chest CTA[J]. J Cardiovasc Comput Tomogr, 2014, 8(2): 97-107. DOI:10.1016/j.jcct.2013.08.002 |
| [7] |
Moore BM, Brady SL, Mirro AE, et al. Size-specific dose estimate (SSDE) provides a simple method to calculate organ dose for pediatric CT examinations[J]. Med Phys, 2014, 41(7): 071917. DOI:10.1118/1.4884227 |
| [8] |
McCollough C, Bakalyar DM, Bostani M, et al. Use of water equivalent diameter for calculating patient size and size-specific dose estimates (SSDE) in CT: the report of AAPM task group 220[J]. AAPM Rep, 2014, 2014: 6-23. |
| [9] |
Daudelin A, Medich D, Andrabi SY, et al. Comparison of methods to estimate water-equivalent diameter for calculation of patient dose[J]. J Appl Clin Med Phys, 2018, 19(5): 718-723. DOI:10.1002/acm2.12383 |
| [10] |
Cléro E, Vaillant L, Hamada N, et al. History of radiation detriment and its calculation methodology used in ICRP Publication 103[J]. J Radiol Prot, 2019, 39(3): R19-R36. DOI:10.1088/1361-6498/ab294a |
| [11] |
Deak P, van Straten M, Shrimpton PC, et al. Validation of a Monte Carlo tool for patient-specific dose simulations in multi-slice computed tomography[J]. Eur Radiol, 2008, 18(4): 759-772. DOI:10.1007/s00330-007-0815-7 |
| [12] |
Kost SD, Fraser ND, Carver DE, et al. Patient-specific dose calculations for pediatric CT of the chest, abdomen and pelvis[J]. Pediatr Radiol, 2015, 45(12): 1771-1780. DOI:10.1007/s00247-015-3400-2 |
| [13] |
Martin CJ, Abuhaimed A, Lee C. Dose quantities for measurement and comparison of doses to individual patients in computed tomography (CT)[J]. J Radiol Prot, 2021. DOI:10.1088/1361-6498/abecf5 |
| [14] |
Trattner S, Halliburton S, Thompson CM, et al. Cardiac-specific conversion factors to estimate radiation effective dose from dose-length product in computed tomography[J]. JACC Cardiovasc Imaging, 2018, 11(1): 64-74. DOI:10.1016/j.jcmg.2017.06.006 |
 2021, Vol. 41
2021, Vol. 41


