头颈深部区域如颅底区、颞下凹区、眶底区、咽旁区位置深在,包含颈动脉、眼球、颅神经等重要组织结构,治疗发生于此区的肿瘤手术难度大,常常无法达到肿瘤根治性切除,预后较差,且术后患者颌面部功能及外形受到较大影响[1]。放射治疗作为头颈深部肿瘤的一种重要治疗手段,增加照射剂量可提高肿瘤的局部控制率,但会加重肿瘤周围正常组织的放射性损伤,增加放射治疗并发症[2]。
放射性粒子植入近距离放射治疗在治疗头颈部肿瘤中取得了很好的疗效[3-4]。低剂量率放射性粒子(125I、192Ir、103Pd等)通过插植针被永久性植入至治疗靶区,使其受到较高而适形的放射剂量照射,而靶区周围剂量陡降,保护了肿瘤周围正常的组织器官。近距离放射治疗头颈深部肿瘤有其特点与优势[5-7]。在放射性粒子植入前,需要在治疗计划系统中根据肿瘤的位置和肿瘤周围解剖结构特点设计插植针穿刺位置和粒子植入位置。由于放射剂量场由粒子的位置决定,而粒子的位置又由插植针针尖位置与穿刺方向决定,因而能否将插植针精确按照术前计划穿刺至既定位置,成为治疗成功与否的关键。头颈深部解剖结构复杂,穿刺风险高,术者在穿刺时需要精确的引导从而保证治疗效果和安全性。
数字化外科技术是基于三维重建及手术模拟、逆向工程、快速成型和手术导航技术发展成的现代外科技术,它可在术前为医生提供患者术区的三维模型以进行手术设计和模拟,并通过制作3D打印个体化穿刺引导模板或借助手术导航系统实现术中精确定位,极大地提高了手术的精确性和安全性[8-9]。而目前国内外应用数字化外科技术引导头颈部肿瘤近距离放射治疗的报道较少。本中心率先建立了基于数字化外科技术的近距离放射治疗引导方法和临床工作流程,将手术导航系统与3D打印个体化穿刺引导模板相结合,以实现术中实时按照可视化治疗计划引导不同穿刺路径上的插植针穿刺和放射性粒子植入[10]。本研究旨在探索和评价数字化外科技术用于引导125I粒子植入近距离放射治疗头颈深部肿瘤的精确性、适形性和临床应用价值。
资料与方法1. 一般资料:回顾性选取2016年12月至2019年11月于北京大学口腔医院就诊行数字化外科技术引导下125I粒子植入近距离放射治疗的头颈深部肿瘤患者。纳入标准:病理诊断为头颈部肿瘤,符合放射性粒子近距离放射治疗适应证;肿瘤位于颅底区、颞下凹区、咽旁区、腮腺深叶区、眼眶区;接受导航系统、3D打印个体化穿刺引导模板联合引导下近距离放射治疗。排除标准:肿瘤位于腮腺浅叶区、唇颊部、舌部、颌下腺、口底等头颈浅部区域者;因全身疾病无法耐受全身麻醉者。根据以上标准纳入患者12例,其中男性6例,女性6例。本研究已经过北京大学口腔医院伦理委员会批准。
2. 术前准备
(1) 近距离放射治疗计划制定:拍摄患者头颈部CT,并将数据导入至近距离放射治疗治疗计划系统中(brachytherapy treatment planning system, BTPS,北京天航科霖科技发展有限公司), 根据病变的范围勾画靶区(gross tumor volume, GTV),计划靶区(planning target volume, PTV)包含GTV和根据肿瘤病理类型外扩区域。设计插植针穿刺针道及粒子植入位置,使针道避开重要的血管、组织器官,且粒子剂量场与靶区高度适形,均匀分布。125I放射性粒子由中国原子能科学院原子高科公司生产,放射性活度范围为0.5~0.7 mCi/颗(1 Ci=3.7×1010Bq)。
(2) 数字化虚拟准备:将患者CT图像导入Mimics 10.01 (Materialise,比利时)软件中,重建出头颈部表面轮廓三维外形模型。后采用数字化技术设计制作3D打印个体化穿刺引导模板[11]。将患者头颈部表面轮廓外形模型文件及治疗计划数据导入至Geomagic studio 2012(3D system,美国)软件中,根据患者头颈部外形及治疗计划中插植针空间位置坐标设计模板模型,使得模型的整体外形与患者头颈部表面轮廓外形相匹配,以利于模板在头颈部的准确就位。其上所设计的导向孔可引导插植针按照治疗计划中的位置进行穿刺,将模板模型通过三维快速成形设备和医用半透明树脂材料打印制作出模板。在Geomagic软件中以所设计的针道最末端粒子中心点为顶点,以针道为轴线,构建定位针道模型。模板模型与针道模型通过布尔运算相加后组成定位模型。将所构建的定位模型与患者CT图像共同导入至iPlan CMF 3.0(BrainLAB,德国)软件中进行导航计划设计,以定位针道模型顶端作为靶点,轴线为方向构建导航穿刺针道,以实现治疗计划的跨平台转移。在软件中勾画出颈动、静脉、眼球等危险区。
(3) 导航设备准备:将数字化设计数据导入至手术导航系统(BrainLAB公司,德国),并将手术导航系统在CT室进行设置和调试。手术导航系统由显示器和定位装置组成,定位装置包含两个摄像机,其周围的红外光源可发射红外光。摄像机通过接收由定位球反射回的红外光实时探测定位球的位置,进而通过定位球实时探测导航参考架、导航探针及插植针的空间位置。显示器可实时显示患者CT图像、危险区、定位模型、导航穿刺针道、插植针的空间位置。
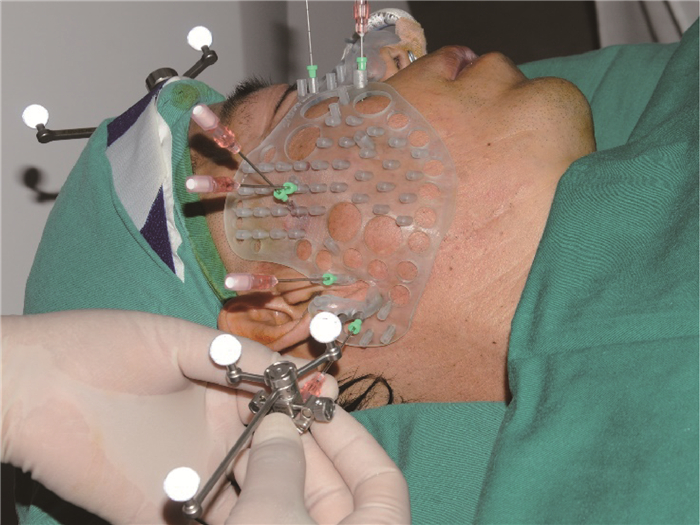
3. 术中引导下插植:患者平卧于CT床,行全身麻醉后在其头部安装头戴式导航参考架,在导航系统定位装置下进行患者头部位置注册及插植针注册。然后将3D打印个体化穿刺引导模板在患者面部按照外形初步就位,并在导航中的定位模型位置引导下进行模板位置的精细核准和确定。在导航系统的实时可视化定位针道和模板上的导向孔联合引导下,行插植针经皮穿刺进入针道,穿刺方向根据导航显示器中的定位针道实时调整,当显示插植针到达靶点时完成穿刺(图 1)。拍摄[HJ]头颈部CT评估实际插植针位置,并进行必要的位置调整。按照治疗计划通过插植针植入125I放射性粒子,全部粒子植入完成后拍摄头颈部CT,即刻评估粒子实际位置与剂量分布。
|
图 1 术中导航和模板联合引导下穿刺针插植 Figure 1 Needle insertion guided by the navigation system and the individual template |
4. 临床应用评价:记录数字化设计定位针道数目及入路,记录术中导航设备的准备工作所需时间。描述并评价术中引导下插植操作过程,记录操作时间。通过CT观察实际插植针、粒子与治疗计划中的位置、数目符合程度及其空间分布。基于术后CT,采用BTPS系统进行术后剂量验证。肿瘤靶区剂量验证指标包括D90(90%PTV接受的剂量)、V100(PTV接受100%处方剂量的百分比)、V150(PTV接受150%处方剂量的百分比)。随访观察穿刺中及穿刺后是否出现血肿、疼痛、感染、穿刺点不愈合、肿瘤细胞种植等不良反应。
结果1. 数字化准备过程:12例患者均成功完成数字化术前准备工作,3D打印个体化穿刺引导模板12块,共设计定位针道70个,定位针道从腮腺咬肌区至颞下凹、颅底区,从颌下、颌后区至颞下凹、颅底区,从眶下区至翼下颌区,从眼睑区至眶内。定位模型均成功导入至导航系统。术中导航系统准备顺利,导航系统准备工作(从导航设备连接启动至患者头部及插植针在导航中注册完毕)用时平均29.3 min。在导航引导下模板就位位置均达到与术前设计位置吻合。
2. 引导下插植操作:12例患者均在3D打印个体化穿刺引导模板和手术导航系统的联合引导下顺利完成插植针穿刺,共完成70个定位针道穿刺,实时可视化引导效果佳。平均每例患者完成定位针道穿刺过程用时13.9 min。
3. 插植后验证:本组病例中插植针实际穿刺位置和方向与计划相符,未发现因穿刺致重要组织器官损伤。穿刺从腮腺咬肌区至颞下凹、颅底区,深度15.7~74.6 mm;从颌下、颌后区至颞下凹、颅底区,深度15.6~73.2 mm;从眶下区至翼下颌区,深度63.7~69.7 mm;从眼睑区至眶内,深度47.6~61.8 mm。植入粒子数目与治疗计划相符,空间分布均匀。术后剂量验证D90范围为83.7~131.0 Gy,平均107.5 Gy;V100范围为89.6%~99.3%,平均94.6%;V150范围为40.2%~58.9%,平均47.8%,见表 1。
|
|
表 1 12例患者粒子植入情况 Table 1 Dose distribution of 12 cases of patients |
4. 不良反应及并发症观察:术中、术后未发现穿刺相关不良反应,随诊期未发现穿刺点、针道肿瘤细胞种植。
讨论放射性粒子近距离放射治疗具有适形和微创的特点,在治疗头颈深部肿瘤中具有优势。术前在治疗计划系统中,医生根据肿瘤的临床及病理特点严谨设计插植针和粒子位置,从而优化靶区剂量分布,减小周围组织器官的机械性和放射性损伤,减少术中插植的不确定性。然而只有将优化的术前治疗计划精确地付诸实践,才能保证治疗的安全性和有效性。但针对头颈深部肿瘤,精确按照计划行放射性粒子植入存在多重困难和挑战:头颈深部有许多重要的组织器官如颈内动脉、眼球、颅神经等;骨性结构对深部组织穿刺造成阻碍,且可能影响放射剂量的分布;窦腔结构可能影响粒子的安放和稳定性;头颈深部穿刺需全身麻醉,如术中反复调整插植针位置延长手术时间,或术后验证粒子位置不佳重新插植,都会增加患者的风险。
目前近距离放射治疗引导方式主要有影像学(如超声、CT、MRI)、模板、手术导航系统和增强现实系统[10, 12-17]。针对头颈深部肿瘤,Bale等[16]报道了3例手术导航系统引导下的颅底区近距离放射治疗,导航系统可在术中实时引导穿刺针避开重要组织结构到达靶区,提升了穿刺的精确性和安全性。本中心首创的头颈部3D打印个体化穿刺引导模板应用在头颈深部肿瘤近距离放射治疗,在模板的引导及辅助下,术者可一次性实现多个插植针穿刺,无需手持固定已经插入针的位置,操作过程精准而简捷[5, 10-11]。本研究创新性地将手术导航系统和3D打印个体化穿刺引导模板相结合,构建了数字化工作流程,集合了这两种引导方式的优点。在术前准备阶段,由于治疗计划系统BTPS与导航软件iPlan CMF数据不兼容,数字化定位模型充当了“桥梁”的作用,精确实现了治疗计划的跨平台转移。初步临床应用结果证明,引导下插植针穿刺精度高,放射剂量分布很好地满足了治疗要求。
数字化外科技术引导头颈深部肿瘤近距离放射治疗有以下优势:治疗计划中的针道位置和实际穿刺针位置可在导航系统实时显示,术者可在穿刺过程中比较二者偏差并及时调整穿刺方向和深度;每例患者可设计和引导多个不同方向的插植针穿刺;在手术导航系统引导下,3D打印个体化穿刺引导模板就位更加精确,减小了人为误差;术前的优化设计和术中的精确引导缩短了插植的时间,降低了治疗风险,也使得实际粒子分布更加合理,减少了粒子植入数量。而数字化外科技术引导近距离放射治疗在应用过程中也会受到一些因素的影响。例如,数字化设计是基于患者术前CT图像,如患者在手术时的组织外形相对于术前拍摄CT时发生变化,将会影响引导精度。另外,在插植针穿刺过程中面部软组织外形的变化可能会影响模板位置和插植针位置。因此,后续研究将继续探索术前数字化准备过程,缩短设计及准备时间,以实现模板模型的快速设计和床旁模板3D打印,并以此为基础实现基于术中即刻CT图像的数字化设计和引导。个体化穿刺引导模板的设计将不断改进,使其覆盖范围包含硬组织,以进一步提高其就位的精确性和稳定性,使得数字化外科技术引导下头颈深部近距离放射治疗更加精准、适形和微创。
综上,采用数字化外科技术将手术导航系统与3D打印个体化穿刺引导模板结合共同引导插植针穿刺和125I粒子植入,提高了近距离放射治疗的精确性和适形性,在头颈部近距离放射治疗特别是深部解剖结构复杂区具有临床应用价值。
利益冲突 无
作者贡献声明 张国昊负责收集、整理数据和论文撰写;张建国、张益指导论文撰写和修改;伍文杰、吕晓鸣负责数字化设计;郑磊、黄明伟负责手术操作和患者随访
| [1] |
Ivan ME, Han SJ, Aghi MK. Tumors of the anterior skull base[J]. Expert Rev Neurother, 2014, 14(4): 425-438. DOI:10.1586/14737175.2014.892830 |
| [2] |
Debus J, Schulz-Ertner D, Schad L, et al. Stereotactic fractionated radiotherapy for chordomas and chondrosarcomas of the skull base[J]. Int J Radiat Oncol Biol Phys, 2000, 47(3): 591-596. DOI:10.1016/s0360-3016(00)00464-8 |
| [3] |
Wu ZY, Wu WJ, Zheng L, et al. Efficacy of combined surgery and 125I seed brachytherapy for treatment of primary mucoepidermoid carcinoma of the parotid gland[J]. Head Neck, 2019, 41(9): 3219-3225. DOI:10.1002/hed.25813 |
| [4] |
赵丹, 郑磊, 吕晓鸣, 等. 125I放射性粒子植入近距离放疗在儿童口腔颌面-头颈部肉瘤治疗中的应用[J]. 中华医学杂志, 2017, 97(1): 33-37. Zhao D, Zheng L, Lyu XM, et al. Clinical application of 125I radioactive seeds brachytherapy in the treatment of the pediatric soft tissue sarcoma in head and neck[J]. Nat Med J China, 2017, 97(1): 33-37. DOI:10.3760/cma.j.issn.0376-2491.2017.01.009 |
| [5] |
刘树铭, 张建国, 黄明伟, 等. 个体化模板辅助颅底区永久性组织间近距离治疗的可行性研究[J]. 中华放射医学与防护杂志, 2013, 33(1): 42-45. Liu SM, Zhang JG, Huang MW, et al. Feasibility of permanent interstitial brachytherapy for skull base region through individual template assistance[J]. Chin J Radiol Med Prot, 2013, 33(1): 42-45. DOI:10.3760/cma.j.issn.0254-5098.2013.01.011 |
| [6] |
Xu N, Zheng L, Wu WJ, et al. Definitive I brachytherapy of locally advanced adenoid cystic carcinoma involving the skull base with satisfying efficacy and safety[J]. J Oral Maxillofac Surg, 2019, 77(10): 2143-2153. DOI:10.1016/j.joms.2019.03.031 |
| [7] |
Chen P, Wu WJ, Yi ZQ, et al. 125I interstitial brachytherapy in management of pediatric skull base tumors[J]. Pediatr Blood Cancer, 2019, 66(5): e27622. DOI:10.1002/pbc.27622 |
| [8] |
Zheng L, Lv X, Zhang J, et al. Translating computer-aided design and surgical planning into successful mandibular reconstruction using a vascularized iliac-crest flap[J]. J Oral Maxillofac Surg, 2018, 76(4): 886-893. DOI:10.1016/j.joms.2017.10.026 |
| [9] |
张益. 数字化外科技术及眼眶骨折精确重建[J]. 中华口腔医学杂志, 2012, 47(8): 463-465. Zhang Y. Digital surgery technique to accurately reconstruct orbital fracture[J]. Chin J Stomatol, 2012, 47(8): 463-465. DOI:10.3760/cma.j.issn.1002-0098.2012.08.004 |
| [10] |
Zhang GH, Lv XM, Wu WJ, et al. Evaluation of the accuracy of computer-assisted techniques in the interstitial brachytherapy of the deep regions of the head and neck[J]. Brachytherapy, 2019, 18(2): 217-223. DOI:10.1016/j.brachy.2018.12.003 |
| [11] |
Huang MW, Zhang JG, Zheng L, et al. Accuracy evaluation of a 3D-printed individual template for needle guidance in head and neck brachytherapy[J]. J Radiat Res, 2016, 57(6): 662-667. DOI:10.1093/jrr/rrw033 |
| [12] |
Davis BJ, Horwitz EM, Lee WR, et al. American Brachytherapy Society consensus guidelines for transrectal ultrasound-guided permanent prostate brachytherapy[J]. Brachytherapy, 2012, 11(1): 6-19. DOI:10.1016/j.brachy.2011.07.005 |
| [13] |
Lee LJ, Damato AL, Viswanathan AN. Clinical outcomes of high-dose-rate interstitial gynecologic brachytherapy using real-time CT guidance[J]. Brachytherapy, 2013, 12(4): 303-310. DOI:10.1016/j.brachy.2012.11.002 |
| [14] |
de Arcos J, Schmidt EJ, Wang W, et al. Prospective clinical implementation of a novel magnetic resonance tracking device for real-time brachytherapy catheter positioning[J]. Int J Radiat Oncol Biol Phys, 2017, 99(3): 618-626. DOI:10.1016/j.ijrobp.2017.05.054 |
| [15] |
Paley PJ, Koh WJ, Stelzer KJ, et al. A new technique for performing Syed template interstitial implants for anterior vaginal tumors using an open retropubic approach[J]. Gynecol Oncol, 1999, 73(1): 121-125. DOI:10.1006/gyno.1998.5326 |
| [16] |
Bale RJ, Freysinger W, Gunkel AR, et al. Head and neck tumors:fractionated frameless stereotactic interstitial brachytherapy-initial experience[J]. Radiology, 2000, 214(2): 591-595. DOI:10.1148/radiology.214.2.r00fe33591 |
| [17] |
Krempien R, Hoppe H, Kahrs L, et al. Projector-based augmented reality for intuitive intraoperative guidance in image-guided 3D interstitial brachytherapy[J]. Int J Radiat Oncol Biol Phys, 2008, 70(3): 944-952. DOI:10.1016/j.ijrobp.2007.10.048 |
 2021, Vol. 41
2021, Vol. 41


