近距离放射治疗至今已有一百多年历史,在放射治疗领域起着不可替代的重要作用。然而,早期近距离治疗都是采用人工施源的方式,因此医务人员接受到大量不必要的辐射。为了减小这种辐射的危害,手动后装和远程后装设备应运而生[1-2]。施源器在后装近距离治疗时期起着重要的作用,它实现了植入与治疗在时间和空间上的分离。早期的高剂量率近距离治疗施源器大多使用不锈钢材质[3-6]。聚亚苯基砜树脂(polyphenylene sulfone resins,PPSU)材质因其在CT扫描时没有伪影,且适合磁共振成像(MRI)扫描,在施源器设计中得到广泛应用[4-5]。有机玻璃材料和3D打印聚乳酸材质常被用来制作插植引导模板[7-8]或施源器[9-10]。
基于TG43号报告[11]的近距离治疗计划系统并未考虑到施源器材料对放射源的影响。因此,实测施源器材料对放射源的影响,对肿瘤精确放射治疗的意义重大,也是放射防护的重要内容之一。本研究选取上述4种常用施源器材料进行相对剂量测量,为各种材质施源器在临床应用中消除剂量影响提供依据,同时为施源器的开发与设计提供一定参考。
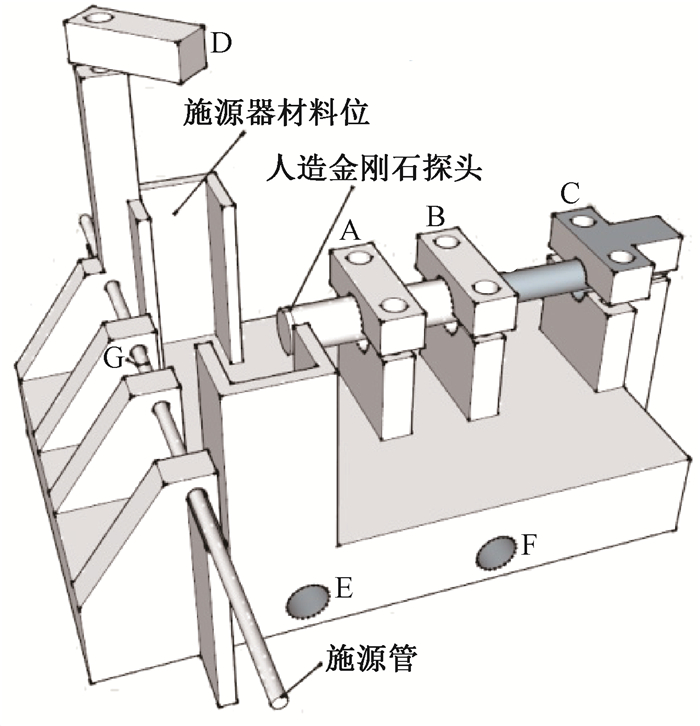
材料与方法1.材料与设备:3D打印支架使用Google SketchUp(版本8.0,美国Trimble公司)软件进行3D建模,见图 1。将模型输出为“*.stl”格式文件,导入MakerBot Print(版本2.8,美国MakerBot industries公司)切片软件,使用“Draft”打印模式。软件切片完成后,导出“*.makerbot”格式文件至3D打印机(型号Replicator+,美国MakerBot industries公司)进行3D打印支架制作。3D打印支架安装在一维水箱(德国IBA公司)探头夹持器上。
|
注:A、B、C为探头固定夹;D为施源器材料固定夹;E、F为一维水箱固定连接孔;G为测量时放射源驻留位 图 1 3D支架建模图 Figure 1 The modeling of a 3D printed holder |
在3D打印中,填充率是决定打印物品内部填入多少物料的参数,一般是以百分比设定,0是完全空心,100%则是完全实心。在设计和制作3D打印物品时,需综合考虑物品强度和打印时间与打印材料消耗来确定填充率。施源器材料的长和宽均为5 cm,正好适合3D打印支架的施源器材料位。304不锈钢材料每块厚度为0.1 mm,共10块;PPSU材料每块厚度为1.5 mm,共6块;有机玻璃材料每块厚度为1 mm,共10块;3D打印聚乳酸材质的厚度均为10 mm,其填充率分别为10%、20%、30%、40%、50%、60%、80%、100%,填充率采用记号笔标于材料上便于区分。采用塑料插植针作为施源管,与3D打印支架固定。选择人造金刚石探头(microDiamond/TW60019,德国PTW公司)作为剂量测量探头,灵敏体积半径为1.1 mm厚度为1 μm的超薄圆柱体,有效测量体积为0.004 mm3,其响应为9.928×10-10 C/Gy。金刚石探头与静电计(Unidose Webline,德国PTW公司)连接,测量用192Ir放射源来自于后装治疗机(Flexitron,荷兰核通公司)。根据3D打印支架设计,金刚石探头有效测量点距离放射源实际驻留位置为2 cm。
2.测量方法:测量前,使用井型电离室检查放射源活度显示值,并使用随机质量控制工具验证驻留位置精度。使用模拟源尺(荷兰核通公司)找到插植针中距离金刚石探头有效测量点中心最近的驻留位置。通过实际测量,该驻留位置为248 mm。使用逐点测量法找最大响应位置来确认该驻留位置。由于放射源周围的剂量梯度很大,与放射源的距离变化会影响测量结果,因此,在整个测量过程中保持施源管和金刚石探头与3D打印支架位置不变。由于后装机的放射源驻留具有出源和收源动作,因此,在测量时采用剂量率作为测量参数以避免出源和收源对结果的影响。另一方面,金刚石探头的响应较低,因此,在测量时,等待出源动作完成后剂量率达到稳定后记录10个剂量率数值。在测量每组数据时记录相应的空气比释动能强度(air kerma strength,AKS)作为放射源强度的参考值,计算相对剂量时考虑AKS变化的影响。每种材料测量前,先测量无材料时的剂量率,然后,放入不同厚度(填充率)材料再次测量,按无材料时的剂量率进行归一。数据测量是在3D打印支架下降到一维水箱水面之下进行的。
3.分析方法:对每组材料的剂量率按照未放置测量材料时的剂量率进行归一。使用Excel 2016版(美国微软公司)软件,计算每组数据的中位数和四分位值,并对每组数据相对剂量的中位数进行线性拟合。
结果1. 304不锈钢材料对192Ir放射源的衰减:随着材料厚度的增加,相对剂量减少。不同厚度304不锈钢材料的测量数据列于表 1。有机玻璃材料对192Ir放射源的影响较复杂,7 mm有机玻璃材料时的剂量影响最小,1 cm以下的有机玻璃材料对剂量的影响均 < 1.5%。不同厚度有机玻璃材料的测量数据列于表 2。
|
|
表 1 不同厚度304不锈钢材料的测量数据(Gy/min) Table 1 Measured data for 304 stainless steel materials with different thickness (Gy/min) |
|
|
表 2 不同厚度有机玻璃材料的测量数据(Gy/min) Table 2 Measured data for polymethyl methacrylate materials with different thickness (Gy/min) |
2.不同填充率3D打印聚乳酸材料对192Ir放射源的影响:40%~60%填充率的3D打印材料对192Ir放射源的影响 < 1%,小于该填充率范围,相对剂量增加,反之减小。不同填充率3D打印材料的测量数据列于表 3。
|
|
表 3 不同填充率3D打印聚乳酸材料测量数据(Gy/min) Table 3 Measured data for 3D printed polylactic acid material with different infill (Gy/min) |
3.不同厚度PPSU材料对192Ir放射源的影响:PPSU材料对192Ir放射源的影响均 < 1%,不同厚度PPSU材料的测量数据见表 4。
|
|
表 4 不同厚度PPSU材料测量数据(Gy/min) Table 4 Measured data for PPSU material with different thickness (Gy/min) |
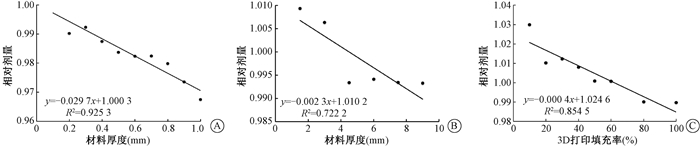
4.数据拟合:对各种材料的不同厚度或不同填充率数据的中位数的线性拟合见图 2。304不锈钢材料的线性拟合公式为y=- 0.029 7x+1.000 3,拟合优度R2=0.925 3。这一结果表明,每毫米304不锈钢材料对于192Ir源的剂量衰减约为3%。对于PPSU材料,线性拟合公式为y= -0.002 3x+1.010 2,拟合优度R2=0.722 2。表明每厘米的PPSU材料对192Ir源的剂量衰减为2.3%。对于3D打印聚乳酸材料,线性拟合公式为y=-0.000 4x+1.024 6,拟合优度R2=0.854 5。拟合结果表明1 cm厚3D打印聚乳酸材料,填充率为60%时正好抵消材料中空气和聚乳酸材料对剂量的影响。有机玻璃材料的归一化中位数大部分 < ±1%,且数据没有特定规律,未进行数据拟合。
|
图 2 材料厚度或填充率与相对剂量的箱形图和线性拟合 A. 304不锈钢;B. PPSU材料;C. 3D打印聚乳酸 Figure 2 Box plots or linear fitting for relative dose vs. material thickness or filling density A. 304 stainless steel material; B. PPSU material; C. 3D printed PLA material |
讨论
3D打印技术在医学上的应用包括:颌面外科手术管理的医学建模[12]、骨重建[13-14]和口腔外科手术[15]。有多项研究已验证了医疗应用中3D打印机具有高精度[12, 16]。由于近距离治疗中剂量梯度很大,因此在实验设计中采用3D打印技术进行3D打印支架制作,以提高施源管和金刚石探头固定的精度,从而提高测量的准确性。同时,本研究选择的金刚石探头经Nakano等[17]的研究证实可用于近距离治疗的剂量测量。在探头摆放上将灵敏体积对称轴与放射源对称轴在一个平面内且相互垂直[18]。本研究设计中将测量距离设定为2 cm,即金刚石探头的中心与放射源中心距离2 cm。这是考虑了宫颈癌近距离治疗的曼彻斯特系统中A点的定义,同时平衡测量响应与测量不确定度因素综合确定的。
随着近距离治疗技术的进步,包括核磁影像的应用及个体化治疗方案的实施,制作施源器的材料也越来越丰富。美国医学物理师协会(American Association of Physicists in Medicine,AAPM)TG43号报告[11]及其更新版本[19]是目前全世界范围内公认的低能光子近距离治疗剂量计算标准。该方法以水中单一源的剂量沉积为基准,通过各驻留点的放射源方向与驻留时间进行叠加。该方法计算迅速,在临床上具有实用性,但其并未考虑组织不均匀性给剂量带来的影响。对于192Ir放射源的近距离治疗,已有研究报道了组织不均匀性带来的剂量偏差。Anagnostopoulos等[20]报道了一个食管癌近距离治疗研究,结果显示靶区内的剂量,在TG-43方法和蒙特卡罗算法之间没有偏差,但TG-43方法的剂量结果高估了脊髓的剂量达13%,而胸骨剂量低估了15%。Lymperopoulou等[21]研究显示在乳腺插植近距离治疗中,对于PTV,TG-43方法的剂量与蒙特卡罗算法结果吻合度较好;然而,对于皮肤则高估了5%,而肺则高估达到了10%。同样对于金属施源器,由于其在放射源周围形成屏蔽体,可造成剂量衰减。对于典型的137Cs宫腔管,此衰减量级约为2%,而在早期Fletcher施源器中,因金属厚壁造成的衰减约为6%[22-23]。在本研究中,线性拟合结果认为,每毫米304不锈钢材料会带来3%的剂量衰减。王先良等[24]通过蒙特卡罗模拟得出不同厚度不锈钢材料在不同径向距离的剂量衰减结果,通过数据拟合发现在径向距离2 cm处的误差为每毫米衰减2.7%。本研究通过实测数据拟合得到的结果与其基本一致。目前金属Fletcher施源器的宫腔管外径约为3.0 mm,金属外壁厚约1.0 mm,因此其引起的剂量衰减约为3%。
由于金属材质的施源器在CT扫描时会产生伪影,并且不能实施基于核磁影像引导的三维近距离治疗,PPSU材质由于抗冲击性和化学稳定性逐渐取代了金属材质用于制作施源器。本研究中1 cm以内PPSU材质对剂量的影响 < 1.5%;而王先良等[24]的蒙特卡罗模拟研究结果显示,1 cm以内的PSU材料对剂量的影响 < 1.5%。而PPSU和PSU材质的相对密度非常接近,分别为1.29和1.24,这说明了本研究与既往的研究结果相一致。同时,本研究发现,当PPSU材质较薄时,实测剂量比未放置材料时有所增加。这说明PPSU材质的引入有两种效应,第1种效应能增加前向散射;第2种效应对射线具有衰减作用。衰减作用随着材料厚度的增加而增加,逐渐抵消散射带来的剂量增加,根据线性拟合公式,当PPSU材质厚度为4.5 mm时两种效应近似相抵消。
在组织间插植治疗中,为保持插植针的相互关系与合理分布,常常使用插植模板引导。由于有机玻璃材质采用激光切割可制成精确的引导孔,且该材质适合高温消毒处理,常常用来制作插植引导模板[7-8]。如其仅作为插植针的准直引导,则不会对剂量产生影响。但在某些情况下,如通过阴道柱形模板[7-8]对阴道黏膜进行照射,放射源先通过准直部分再进入组织,则其会对剂量产生影响。本研究中1 cm以下的有机玻璃材质对剂量的影响均 <1.5%。
由于有机玻璃材质很难制作出复杂形状及弯曲针道的模板,3D打印技术的发展有效的解决了这一难题,可制作个体化复杂插植模板[16]或施源器[9-10]用于具有复杂解剖结构的患者。聚乳酸是3D打印中常用的材质之一,其具有热稳定性好、耐菌、抗紫外线特性,生物相容性好,适合医疗卫生领域。使用聚乳酸材质的3D打印一般采用熔融沉积技术制作,填充率作为其重要指标兼顾3D打印器件的强度和打印时间的平衡。为了防止光子通过3D打印空隙穿透入射到金刚石探头,在3D打印时选择器件直立模式,而非器件平躺模式。根据本研究的拟合公式,填充率 < 60%时,相对剂量有所上升;而填充率>60%时,相对剂量减小。造成这一结果的原因是,填充率较小时,未填充部分为空气,空气相对水的密度小很多,对射线的衰减作用小于水;聚乳酸的相对密度为1.20~1.30,其对射线的衰减作用大于水。因此,随着填充率的增加,聚乳酸的占比增加,相对剂量逐渐下降,呈线性下降趋势。本研究的结果显示,在填充率为40%~80%时,1 cm聚乳酸材料对剂量的影响 < 1%。
本研究中,测量结果出现一定的离散性,即相同条件下各次测量结果存在一定差异。测量结果的不确定性主要来自金刚石探头与放射源距离的不确定度。在各次测量中,放射源均从后装机出源到达测量驻留点,虽后装机在测量前进行了驻留位置精度验证,但仍存在一定的驻留位置不确定度。Flexitron后装机的驻留位置不确定度 < ±1.0 mm,这是放射源的径向方向上的不确定度。横向不确定度来自塑料插植针内径与放射源外径之差,约为±0.2 mm。基于此,Kaveckyte等[18]研究发现,1.5~5.5 cm距离范围内的金刚石探头读数偏差 < 2%。此外,金刚石探头的响应较小,约为10-9 C/Gy,因此静电计中的漏电流(低于0.01 pA)会对测量结果产生一定影响。Kaveckyte等[18]研究发现,金刚石探头短期稳定性引起的读数相对标准差不超过0.2%。基于上述不确定度的影响,会造成某些测量条件下测量数据的偏离,这也是造成本研究中部分线性拟合效果不佳的主要原因,拟合优度范围为0.722 2~0.925 3。其中,PPSU材料的拟合优度最低,然而从拟合曲线看,各测量点的中位值与拟合曲线的纵向距离最大值仅为0.006 3,即相对剂量偏差为0.63%。这一偏差显著小于因放射源驻留位置不确定度引起的2%偏差。
由于基于TG 43号报告的剂量计算的局限性,2012年AAPM发布了基于模型的剂量计算算法的TG 186[25]号报告,其摒弃了单纯水的模体,建立了采用非水介质中辐射传输模型,可以更精确地重建实际传递给患者的剂量分布。
综上所述,施源器材料,尤其是高密度材料(如304不锈钢)和新型技术材料(如3D打印聚乳酸),对192Ir后装源的吸收剂量影响需引起施源器开发人员和临床应用者的足够重视。为保证近距离治疗剂量投照的准确性,在施源器设计时需考虑材质、厚度或填充率,同时在基于TG43号报告剂量计算的治疗计划设计中,需考虑施源器材料对剂量的影响。
志谢 本研究受吉林省科技厅社发处项目(20090458)、吉林省卫生计生委项目(2014ZC054)资助
利益冲突 无
作者贡献声明 赵红福负责论文撰写、指导数据采集与处理;程光惠负责实验设计与指导论文修订;赵志鹏负责实验数据处理;韩东梅负责数据采集
| [1] |
Haybittle JL, Mitchell JS. A simple after-loading technique for the treatment of cancer of the cervix[J]. Br J Radiol, 1975, 48(568): 295-298. DOI:10.1259/0007-1285-48-568-295 |
| [2] |
Goldson AF, Alexander GA, Mahan DG, et al. Remote afterloading for intracavitary irradiation of cervix carcinoma[J]. J Natl Med Assoc, 1978, 70(1): 51-54. |
| [3] |
Basu B, Basu S, Chakraborti B, et al. A comparison of dose distribution from Manchester-style and Fletcher-style intracavitary brachytherapy applicator systems in cervical cancer[J]. J Contemp Brachytherapy, 2012, 4(4): 213-218. DOI:10.5114/jcb.2012.32555 |
| [4] |
Berger D, Dimopoulos J, Pötter R, et al. Direct reconstruction of the Vienna applicator on MR images[J]. Radiother Oncol, 2009, 93(2): 347-351. DOI:10.1016/j.radonc.2009.07.002 |
| [5] |
Smolic M, Sombroek C, Bloemers M, et al. Needle use and dosimetric evaluation in cervical cancer brachytherapy using the Utrecht applicator[J]. Radiother Oncol, 2018, 126(3): 411-416. DOI:10.1016/j.radonc.2017.11.007 |
| [6] |
Sharma DN, Rath GK, Thulkar S, et al. Computerized tomography-guided percutaneous high-dose-rate interstitial brachytherapy for malignant lung lesions[J]. J Cancer Res Ther, 2011, 7(2): 174-179. DOI:10.4103/0973-1482.82914 |
| [7] |
Weitmann HD, Knocke TH, Waldhäusl C, et al. Ultrasound-guided interstitial brachytherapy in the treatment of advanced vaginal recurrences from cervical and endometrial carcinoma[J]. Strahlenther Onkol, 2006, 182(2): 86-95. DOI:10.1007/s00066-006-1420-4 |
| [8] |
Martinez A, Cox RS, Edmundson GK. A multiple-site perineal applicator (MUPIT) for treatment of prostatic, anorectal, and gynecologic malignancies[J]. Int J Radiat Oncol Biol Phys, 1984, 10(2): 297-305. DOI:10.1016/0360-3016(84)90016-6 |
| [9] |
Sethi R, Cunha A, Mellis K, et al. Clinical applications of custom-made vaginal cylinders constructed using three-dimensional printing technology[J]. J Contemp Brachytherapy, 2016, 8(3): 208-214. DOI:10.5114/jcb.2016.60679 |
| [10] |
Jones EL, Tonino Baldion A, Thomas C, et al. Introduction of novel 3D-printed superficial applicators for high-dose-rate skin brachytherapy[J]. Brachytherapy, 2017, 16(2): 409-414. DOI:10.1016/j.brachy.2016.11.003 |
| [11] |
Nath R, Anderson LL, Luxton G, et al. Dosimetry of interstitial brachytherapy sources:Recommendation of the AAPM Radiation Therapy Committee Task Group No. 43[J]. Med Phys, 1995, 22(2): 209-234. DOI:10.1118/1.597458 |
| [12] |
Chow LK, Cheung LK. The usefulness of stereomodels in maxillofacial surgical management[J]. J Oral Maxillofac Surg, 2007, 65(11): 2260-2268. DOI:10.1016/j.joms.2006.11.041 |
| [13] |
Cohen A, Laviv A, Berman P, et al. Mandibular reconstruction using stereolithographic 3-dimensional printing modeling technology[J]. Oral Surg Oral Med Oral Pathol Oral Radiol Endod, 2009, 108(5): 661-666. DOI:10.1016/j.tripleo.2009.05.023 |
| [14] |
Schrank ES, Hitch L, Wallace K, et al. Assessment of a virtual functional prototyping process for the rapid manufacture of passive-dynamic ankle-foot orthoses[J]. J Biomech Eng, 2013, 135(10): 101011-101017. DOI:10.1115/1.4024825 |
| [15] |
Winder J, Bibb R. Medical rapid prototyping technologies:state of the art and current limitations for application in oral and maxillofacial surgery[J]. J Oral Maxillofac Surg, 2005, 63(7): 1006-1015. DOI:10.1016/j.joms.2005.03.016 |
| [16] |
Laan RC, Nout RA, Dankelman J, et al. MRI-driven design of customised 3D printed gynaecological brachytherapy applicators with curved needle channels[J]. 3D Print Med, 2019, 5(1): 8. DOI:10.1186/s41205-019-0047-x |
| [17] |
Nakano T, Suchowerska N, Bilek MM, et al. High dose-rate brachytherapy source localization:positional resolution using a diamond detector[J]. Phys Med Biol, 2003, 48(14): 2133-2146. DOI:10.1088/0031-9155/48/14/307 |
| [18] |
Kaveckyte V, Malusek A, Benmakhlouf H, et al. Suitability of microDiamond detectors for the determination of absorbed dose to water around high-dose-rate 192Ir brachytherapy sources[J]. Med Phys, 2018, 45(1): 429-437. DOI:10.1002/mp.12694 |
| [19] |
Rivard MJ, Butler WM, DeWerd LA, et al. Supplement to the 2004 update of the AAPM Task Group No. 43 report[J]. Med Phys, 2007, 34(6): 2187-2205. DOI:10.1118/1.2736790 |
| [20] |
Anagnostopoulos G, Baltas D, Pantelis E, et al. The effect of patient inhomogeneities in oesophageal 192Ir HDR brachytherapy:a Monte Carlo and analytical dosimetry study[J]. Phys Med Biol, 2004, 49(12): 2675-2685. DOI:10.1088/0031-9155/49/12/014 |
| [21] |
Lymperopoulou G, Papagiannis P, Angelopoulos A, et al. A dosimetric comparison of 169Yb and 192Ir for HDR brachytherapy of the breast, accounting for the effect of finite patient dimensions and tissue inhomogeneities[J]. Med Phys, 2006, 33(12): 4583-4589. DOI:10.1118/1.2392408 |
| [22] |
Yorke ED, Schell MC, Gaskill JW, et al. Using measured dose distribution data of the Fletcher-Suit-Delclos colpostat in brachytherapy treatment planning[J]. Int J Radiat Oncol Biol Phys, 1987, 13(9): 1413-1419. DOI:10.1016/0360-3016(87)90239-2 |
| [23] |
Sharma SC, Gerbi B, Madoc-Jones H. Dose rates for brachytherapy applicators using 137Cs sources[J]. Int J Radiat Oncol Biol Phys, 1979, 5(10): 1893-1897. DOI:10.1016/0360-3016(79)90579-0 |
| [24] |
王先良, 王培, 袁珂, 等. 施源器材料和厚度对近距离放射治疗剂量的影响[J]. 肿瘤预防与治疗, 2015, 28(2): 67-70. Wang XL, Wang P, Yuan K, et al. A dosimetry study of applicator material and thickness in brachytherapy[J]. J Cancer Control Treat, 2015, 28(2): 67-70. DOI:10.3969/j.issn.1674-0904.2015.02.003 |
| [25] |
Beaulieu L, Carlsson Tedgren A, Carrier JF, et al. Report of the Task Group 186 on model-based dose calculation methods in brachytherapy beyond the TG-43 formalism:current status and recommendations for clinical implementation[J]. Med Phys, 2012, 39(10): 6208-6236. DOI:10.1118/1.4747264 |
 2020, Vol. 40
2020, Vol. 40


