肛管癌发病率较低,仅占消化道肿瘤的1%~2%。来自美国的数据显示,年发病率为1/10万[1]。《2010年中国肿瘤登记年报》数据显示,2007年我国报道的肛管癌发病仅161例。治疗上,直到20世纪80年代,手术仍然是主要的治疗手段。腹会阴联合切除术(APE)是推荐的手术术式,然而局部失败率高达50%,5年生存率在50%~70%。目前,同步放化疗是肛管鳞癌的主要治疗手段,生存率与腹会阴联合切除术相当,并且可以保留肛管功能[2]。本研究回顾性分析本院2011年以来接受容积旋转调强放疗的肛管鳞癌,讨论同步放化疗的疗效及影响因素。
资料与方法1.入组患者:本研究收集北京大学肿瘤医院自2011年以来收治的肛管癌,共计47例,其中,初治、未转移、鳞癌患者共计19例。所有患者均由本院病理证实为鳞状细胞癌。
2.肿瘤情况:该组患者有1例为肛周鳞癌,余18例为肛管内鳞癌。肿瘤下缘距离肛门缘的中位距离为1.0 cm(-2.0~3.0 cm)。肿瘤长径(轴位)中位值3.0 cm(1.4~5.1 cm)。按照美国癌症联合会(AJCC)第8版分期,Ⅰ期0例,Ⅱ期6例,Ⅲ期13例。
3.治疗方案:19例患者中,有5例患者曾于外院接受局部切除手术,后就诊本院行根治性放疗。放疗技术采用容积旋转调强放疗(VMAT)。所有患者均未行诱导化疗。19例患者中,1例因分期早、局部切除术后,行单纯放疗;余18例患者行同步化疗。同步化疗方案包括:铂类+5-氟尿嘧啶(5-FU)、铂类+卡培他滨、丝裂霉素+卡培他滨、单药卡培他滨。铂类药物为顺铂、奈达铂。根据化疗药物不同分为同步化疗方案A、同步化疗方案B。前者指同步化疗方案中含5-FU或者卡培他滨,共18例纳入分析;后者指同步化疗方案中含丝裂霉素或者铂类,共17例纳入分析。
放射治疗:19例患者均接受了VMAT。患者取仰卧位,平躺于腹平板,双手上举抱肘置于额前,腹部热塑膜固定体位。定位前1 h排空膀胱及直肠,一次性饮水600~800 ml(含碘造影剂),待膀胱充盈、尿意明显时进行CT扫描。肿瘤下缘或者肛门口贴铅点。扫描上界至第四腰椎水平、下界至股骨上段,扫描层厚0.5 cm,CT扫描时静脉注射碘造影剂。原发肿瘤靶区(GTV):GTVp包括肛管大体肿瘤,GTVnd包括区域转移淋巴结。临床靶区(CTV)包括肿瘤原发灶及其周围2.0~2.5 cm,并包括淋巴引流区。淋巴引流区参考澳大利亚胃肠试验组共识[3],包括直肠系膜区、骶前区、坐骨直肠窝、髂内、髂外、闭孔、腹股沟等淋巴引流区。本中心以S3下缘为界将CTV分为上方CTV1、下方CTV2。计划靶区(PTV):PGTVp、PGTVnd、PTV分别为相应靶区周围外扩0.5 cm,上下外扩1.0 cm形成。处方剂量:PGTVp、PGTVnd 50 Gy/25次,PTV1(L5~S3)40 Gy/25次,PTV2(S3~腹股沟)45 Gy/25次,肿瘤原发灶和转移淋巴结序贯补量10 Gy/5次。本研究中,4例局部切除术后患者,原发灶给予50~55 Gy,余15例给予60 Gy。
4.观察指标:近期、远期不良反应评估参考常见不良事件评价标准CTCAE 3.0。近期疗效评估参考实体瘤疗效评价标准RECIST 1.0。远期生存评估:记录局部复发、区域淋巴结复发、远处转移、死亡等事件,自患者肛管癌确诊至上述事件发生的时间为无事件生存时间,如无局部复发生存率(LFS)、无区域复发生存率(RFS)、无远处转移生存率(DFS)、总生存率(OS)。并定义自患者确诊至出现肿瘤局部、区域复发,或者远处转移,或者死亡的时间为无疾病进展时间(PFS)。
5.统计学处理:采用SPSS 22.0进行数据收集、整理与分析。通过Kaplan-Meier法描述患者生存情况。将患者按照肿瘤是否进展分为对照组、病例组,进行病例对照分析,探索患者一般状况、分期、治疗方案等对肿瘤进展的影响。分类变量采用Fisher′s确切概率法检验,年龄资料不符合正态分布采用秩和检验。P<0.05为差异有统计学意义。
结果1.患者一般情况:19例患者中,男性5例(26.3%),女性14例(73.7%),男:女比例为1:2.8。中位年龄51岁(44~68岁)。体力评分ECOG 0~1分,仅有2例患者分别合并糖尿病、高血压,余无基础疾病。19例患者均为鳞状细胞癌,其中,T1~2 13例,T3~4 6例;按照淋巴结分期,N0 6例,N1 13例。中位随访时间31个月(范围6~93个月)。放疗结束后1~3个月内,所有患者行盆腔MR评价效效,其中,完全缓解(CR)者10例(52.6%),部分缓解(PR)者8例(42.1%),稳定(SD)者1例(5.3%),无进展(PD)者。
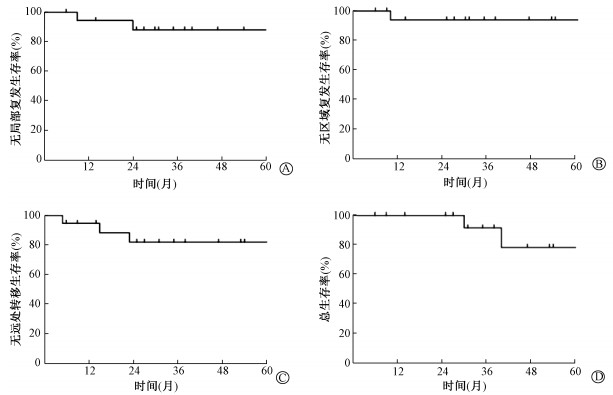
2.远期生存:末次随访日期为2019年4月,共有6例患者出现进展,中位进展时间为16.5个月。其中5例患者(83.3%)进展发生在两年以内。6例进展的患者中,局部复发者3例、区域淋巴结复发1例、远处转移3例、死亡者2例。3年无局部复发生存率、无区域复发生存率、无远处转移生存率、总生存率分别为88.1%、94.1%、82.1%、91.7%。生存曲线示于图 1。
|
图 1 肛管鳞癌同步放化疗的无局部复发生存率(A)、无区域复发生存率(B)、无远处转移生存率(C)、总生存率(D) Figure 1 Local failure-free survival (A), regional failure-free survival (B), distant failure-free survival (C) and overall survival (D) of the anal squamous cell carcinoma with concurrent chemoradiotherapy |
3.肿瘤进展风险分析:以放疗后出现疾病进展的6例患者为病例组,剩余患者为对照组进行病例对照研究。将年龄、性别、肿瘤分化程度、T分期、N分期、局部切除病史、同步化疗方案等因素分别纳入分析。结果显示,同步化疗方案中,应用5-FU或者卡培他滨在两组病例中的分布不同,差异有统计学意义(P=0.013)。其他纳入统计的暴露因素在两组中的分布差异均无统计学意义(P>0.05)。单因素分析结果如表 1。
|
|
表 1 影响肿瘤进展的潜在危险因素(病例对照分析) Table 1 The distribution of exposure factors in case and control groups |
4.治疗相关不良反应:所有患者均顺利完成治疗,放化疗期间未出现≥4级的治疗不良反应。3级不良反应主要表现为白细胞减低(15.8%)、血小板减低(10.5%)、腹泻(15.8%)、皮肤反应(31.6%)。远期不良反应有肛门区疼痛、便血、里急后重、大便失禁。截止到随访之日,远期不良反应主要表现为1~2级不良反应。具体近期和远期不良反应分别列于表 2,3。
|
|
表 2 放化疗相关近期不良反应 Table 2 Acute toxicities of radiation and chemotherapy |
|
|
表 3 放疗相关远期不良反应 Table 3 Long-term toxicities of radiation |
讨论
多项临床研究显示,同步放化疗可以取得类似手术的生存率,同时可以保留肛门功能,目前已经作为标准治疗[4-6]。男性、肿瘤长径>5 cm、淋巴结阳性是肛管鳞癌的不良预后因素[5-7]。本研究采用病例对照分析,性别、T分期、N分期均未显示与肿瘤进展有关,考虑可能与本组研究样本量较小有关。近年来,有报道显示,HPV和/或p16阳性患者的总体预后较好[8-9]。本组患者未提供HPV感染状态,HPV对肛管鳞癌预后的影响有待进一步探讨。
早在20世纪末,来自英国的ACT1研究[4, 6]和欧洲的欧洲癌症研究与治疗组织(EORTC)22861研究[5]分别证明了同步放化疗在肿瘤局部区域控制率、肿瘤相关生存率、结肠造口率等方面优于单纯放疗,同时也奠定了丝裂霉素+ 5-FU方案在肛管鳞癌同步放化疗中的地位。同样地,美国肿瘤放疗协作组(RTOG) 8704对比丝裂霉素+5-FU双药同步化疗与5-FU单药同步化疗,结果显示,丝裂霉素+5-FU双药同步化疗在治疗反应、无结肠造口生存率、无病生存率方面均优于5-FU单药同步化疗。在双药同步化疗中,顺铂是否可以替代丝裂霉素呢,针对此问题,2012年RTOG 9811的远期随访结果显示,与顺铂+5-FU组相比,丝裂霉素+5-FU组在5年DFS(67.8% vs. 57.8%)和OS(78.3% vs. 70.7%)方面均有明显获益[11],证明丝裂霉素+5-FU同步放化疗仍然是肛管鳞癌的标准治疗。在结直肠腺癌中,卡培他滨可以替代5-FU作为一线化疗。而在肛管鳞癌的同步放化疗中,卡培他滨是否可以替代5-FU,对这一问题,2014年有回顾性研究纳入105例肛管鳞癌患者,结果显示,卡培他滨组和5-FU组的完全缓解率、3年局部区域控制率、3年总生存率差异均无统计学意义[12]。而本研究结果显示,同步卡培他滨化疗可能比同步5-FU化疗有更好的预后(P=0.013)。然而该研究为小样本回顾性研究,卡培他滨是否优于5-FU有待进一步探讨。从现有的回顾性数据看,同步卡培他滨化疗在生存率、治疗不良反应方面均不劣于或者优于同步5-FU化疗。因此,尽管数据有限,美国国立综合癌症网络(NCCN)指南推荐丝裂霉素+卡培他滨同步放化疗可以作为丝裂霉素+5-FU同步放化疗的替代方案。
常规技术放疗年代,肛管鳞癌同步放化疗的3年OS为70%~85%[7, 10],而本研究19例患者均采用VMAT调强技术放射治疗,3年OS为91.7%,有高于常规技术放疗的趋势。从急性期不良反应看,RTOG 0529研究结果显示,调强技术放疗较常规技术降低了≥2级血液学不良反应(73% vs. 85%)、≥3级消化道不良反应(21% vs. 36%)和≥3级皮肤不良反应(23% vs. 49%)[13]。RTOG 9811报道了常规技术放疗治疗肛管磷癌的近期不良反应,≥3级血液学不良反应61%,≥3级消化道不良反应36%,≥3级皮肤反应49%[7]。而本研究中,≥3级血液学不良反应21.1%、消化道不良反应15.8%、皮肤不良反应31.6%,均明显低于RTOG 9811报道的急性期不良反应。因此,对比历史数据,本院VMAT调强放疗在肛管鳞癌的治疗中疗效和正常组织保护方面似乎均有优于常规技术放疗的趋势。然而历史数据对照难以规避性别、分期、HPV状态、化疗等混杂因素,因此放疗技术的进步是否提高肛管鳞癌的疗效有待进一步研究。目前本院肛管鳞癌的靶区及处方剂量参考RTOG靶区勾画指南[14]和澳大利亚胃肠试验组共识[3]。肿瘤原发灶及阳性淋巴结处方剂量55~60 Gy,高危亚临床病灶50 Gy,低危亚临床病灶45 Gy,25~30次分割。由于本研究中放疗靶区及处方剂量一致,因此,没有探讨放疗靶区、处方剂量对肿瘤进展的影响。
本研究显示,调强技术放疗治疗肛管鳞癌在疗效和正常组织保护方面可能更有优势。同步化疗采用含卡培他滨的双药方案可能是降低肿瘤进展的有利因素。
利益冲突 本研究由署名作者按以下贡献声明独立开展,不涉及任何利益冲突,排名无争议作者贡献声明 王洪智负责数据分析和论文撰写;张扬子、耿建昊负责数据收集、整理,协助撰写论文;朱向高参与统计分析,指导论文书写;李永恒、蔡勇参与研究设计和论文审阅;王维虎负责研究设计,指导论文修改
| [1] |
Jemal A, Simard EP, Dorell C, et al. Annual report to the nation on the status of cancer, 1975-2009, featuring the burden and trends in human papillomavirus(HPV)-associated cancers and HPV vaccination coverage levels[J]. J Natl Cancer Inst, 2013, 105(3): 175-201. DOI:10.1093/jnci/djs491 |
| [2] |
Glynne-Jones R, Nilsson PJ, Aschele C, et al. Anal cancer:ESMO-ESSO-ESTRO clinical practice guidelines for diagnosis, treatment and follow-up[J]. Radiother Oncol, 2014, 111(3): 330-339. DOI:10.1016/j.radonc.2014.04.013 |
| [3] |
Ng M, Leong T, Chander S, et al. Australasian Gastrointestinal Trials Group (AGITG) contouring atlas and planning guidelines for intensity-modulated radiotherapy in anal cancer[J]. Int J Radiat Oncol Biol Phys, 2012, 83(5): 1455-1462. DOI:10.1016/j.ijrobp.2011.12.058 |
| [4] |
Northover J, Glynne-Jones R, Sebag-Montefiore D, et al. Chemoradiation for the treatment of epidermoid anal cancer:13-year follow-up of the first randomised UKCCCR Anal Cancer Trial (ACT I)[J]. Br J Cancer, 2010, 102(7): 1123-1128. DOI:10.1038/sj.bjc.6605605 |
| [5] |
Bartelink H, Roelofsen F, Eschwege F, et al. Concomitant radiotherapy and chemotherapy is superior to radiotherapy alone in the treatment of locally advanced anal cancer:results of a phase Ⅲ randomized trial of the European Organization for Research and Treatment of Cancer Radiotherapy and Gastrointestinal Cooperative Groups[J]. J Clin Oncol, 1997, 15(5): 2040-2049. DOI:10.1200/JCO.1997.15.5.2040 |
| [6] |
Epidermoid anal cancer: results from the UKCCCR randomised trial of radiotherapy alone versus radiotherapy, 5-fluorouracil, and mitomycin. UKCCCR Anal Cancer Trial Working Party. UK Co-ordinating Committee on Cancer Research[J]. Lancet, 1996, 348(9034): 1049-1054.
|
| [7] |
Ajani JA, Winter KA, Gunderson LL, et al. Fluorouracil, mitomycin, and radiotherapy vs. fluorouracil, cisplatin, and radiotherapy for carcinoma of the anal canal:a randomized controlled tria[J]. JAMA, 2008, 299(16): 1914-1921. DOI:10.1001/jama.299.16.1914 |
| [8] |
Rodel F, Wieland U, Fraunholz I, et al. Human papillomavirus DNA load and p16INK4a expression predict for local control in patients with anal squamous cell carcinoma treated with chemoradiotherapy[J]. Int J Cancer, 2015, 136(2): 278-288. DOI:10.1002/ijc.28979 |
| [9] |
Serup-Hansen E, Linnemann D, Skovrider-Ruminski W, et al. Human papillomavirus genotyping and p16 expression as prognostic factors for patients with American Joint Committee on Cancer stages Ⅰ to Ⅲ carcinoma of the anal canal[J]. J Clin Oncol, 2014, 32(17): 1812-1817. DOI:10.1200/JCO.2013.52.3464 |
| [10] |
Flam M, John M, Pajak TF, et al. Role of mitomycin in combination with fluorouracil and radiotherapy, and of salvage chemoradiation in the definitive nonsurgical treatment of epidermoid carcinoma of the anal canal:results of a phase Ⅲ randomized intergroup study[J]. J Clin Oncol, 1996, 14(9): 2527-2539. DOI:10.1200/JCO.1996.14.9.2527 |
| [11] |
Gunderson LL, Winter KA, Ajani JA, et al. Long-term update of US GI intergroup RTOG 98-11 phase Ⅲ trial for anal carcinoma:survival, relapse, and colostomy failure with concurrent chemoradiation involving fluorouracil/mitomycin versus fluorouracil/cisplatin[J]. J Clin Oncol, 2012, 30(35): 4344-4351. DOI:10.1200/JCO.2012.43.8085 |
| [12] |
Meulendijks D, Dewit L, Tomasoa NB, et al. Chemoradiotherapy with capecitabine for locally advanced anal carcinoma:an alternative treatment option[J]. Br J Cancer, 2014, 111(9): 1726-1733. DOI:10.1038/bjc.2014.467 |
| [13] |
Kachnic LA, Winter K, Myerson RJ, et al. RTOG 0529:a phase 2 evaluation of dose-painted intensity modulated radiation therapy in combination with 5-fluorouracil and mitomycin-C for the reduction of acute morbidity in carcinoma of the anal canal[J]. Int J Radiat Oncol Biol Phys, 2013, 86(1): 27-33. DOI:10.1016/j.ijrobp.2012.09.023 |
| [14] |
Myerson RJ, Garofalo MC, El NI, et al. Elective clinical target volumes for conformal therapy in anorectal cancer:a radiation therapy oncology group consensus panel contouring atlas[J]. Int J Radiat Oncol Biol Phys, 2009, 74(3): 824-830. DOI:10.1016/j.ijrobp.2008.08.070 |
 2019, Vol. 39
2019, Vol. 39


