宫颈癌是常见的妇科恶性肿瘤之一[1]。腔内近距离放射治疗作为外照射的补充,在宫颈癌的治疗中发挥着极其重要的作用[2]。与外照射放疗计划的制定类似,近距离三维后装放疗计划的制定方式同样包括正向计划和逆向计划两种。图形拖拽的正向优化(GRO)和模拟退火的逆向优化算法(IPSA)分别为广西医科大学附属肿瘤医院放疗中心常用的正、逆向三维后装治疗计划的制定方式。目前国外已有多篇文献报道了近距离三维后装治疗计划的制定方式,总体来说,相比于GRO计划,IPSA计划可以显著提高靶区覆盖度,降低危及器官接受的照射剂量,同时可缩短计划制定所用时间[3-5]。前期研究结果与国外的相关报道类似[6]。然而,对于初始使用GRO计划而得到较差剂量分布结果的病例,再次使用IPSA重新制定计划并不能从本质上改变剂量分布的结果[7]。其他的相关研究提示,当近距离放疗的施源器为环形施源器或宫腔管联合插植针时,IPSA可以大幅度提高靶区的覆盖度[8-9]。结合前期研究[7],认为IPSA计划的优势可能会随着施源管数目的增多而增大。本研究通过对60例局部晚期宫颈癌患者腔内联合组织间插植治疗剂量的分析,对比GRO和IPSA两种优化方式制定的三维后装放疗计划的剂量学差异,同时探讨了插植针数目对这两种计划方式剂量学差异的影响。
资料与方法1.临床资料:选取2016年10月至2018年7月在广西医科大学附属肿瘤医院接受根治性放疗的60例宫颈癌患者,所有患者均经病理检查确诊,年龄为28~54岁,平均年龄47岁,中位年龄45岁,根据国际妇产科联盟(FIGO)标准分期为ⅡB~ⅢB期。患者先行外照射,总剂量为50 Gy,分25次,每次2.0 Gy,5次/周,在完成体外照射36~40 Gy后开始三维后装腔内放疗,1次/周。所选取的60例患者腔内放疗均采用宫腔管联合组织间插植技术,施源器为1根宫腔管+1~4根插植针,每种插植针数目的病例数各15例,每病例只取其中一次后装腔内放疗计划纳入本研究。
2.施源器置入及CT图像采集:患者排空直肠后以截石位平躺在妇科治疗床上,常规消毒后插入Folcy导尿管,使球囊位于膀胱颈的位置,并向球囊内注入8 ml的生理盐水。选用荷兰Nucletron公司生产的Fletcher宫腔管及直径1.9 mm、长20 cm的插植针为施源器。插植针的数目、植入的位置和深度、排列方式等由妇瘤科医生根据每个患者的阴道/宫腔的病变情况及周围危及器官的位置、结合相关循证资料[10]及医生的经验决定,并尽量保证各施源器间的距离 < 2 cm。在植入宫腔施源器及插植针之后,在阴道处填塞纱布固定,夹闭尿管,经尿管向膀胱注入150~250 ml的生理盐水。患者的扫描定位使用的是通用公司生产的4排80 cm大孔径CT模拟机,扫描范围从髂前上脊至坐骨结节下缘,层厚2.5 mm。
3.靶区和危及器官勾画:患者完成CT扫描后,图像传至后装治疗计划系统(瑞典医科达公司,Oncentra® Brachy V4.3)。由医师参照每一位患者相应的影像及查体结果,参考欧洲放射肿瘤学会工作组(GEC-ESTRO)工作组推荐的靶区定义标准,在CT图像上勾画高危临床靶区(HR-CTV)和直肠、膀胱、乙状结肠等危及器官。
4.治疗计划的制定:治疗处方为7 Gy/次,1次/周,共4次。危及器官限量:膀胱2 cm3体积接受的放疗剂量D2 cm3≤4.5 Gy,直肠D2 cm3≤4.0 Gy。在完成施源管重建后,对每例病例分别完成GRO及IPSA计划。
(1) GRO:将处方剂量的归一位置设为HR-CTV,计划系统会自动在HR-CTV表面生成一定数目的剂量归一点,这些归一点可以大致描绘出HR-CTV的轮廓,以保证HR-CTV得到处方剂量。因此,GRO的计划是优先满足了靶区的剂量分布,再通过人工拖拽剂量线的方式在保证危及器官不超量的情况下,尽可能提高靶区的剂量。
(2) IPSA:通过添加逆向优化的目标函数,同时将靶区和危及器官的照射剂量纳入考虑范围,以调整剂量分布。IPSA优化模板的各参数设置如下:靶区HR-CTV表面最小剂量7.0 Gy,权重200;表面最大剂量7.6 Gy,权重200;体积最小剂量7.2 Gy,权重100;膀胱表面最大剂量4.0 Gy,权重100;直肠表面最大剂量3.5 Gy,权重80。IPSA中驻留时间离差限制(dwelling time deviation constraint,DTDC)值设置为0.2。调用函数模板后获得初次优化结果,然后根据每个病例的具体剂量分布调整相关函数再次优化以使剂量分布满足医师要求。为了便于比较,使用逆向优化的计划不再使用人工拖拽剂量线的方法调整剂量分布。
5.观察指标:比较GRO和IPSA计划的剂量学参数:靶区覆盖度(D90、D100、V100)、靶区高量(V150、V200、V300)、危及器官(膀胱、直肠)的D1 cm3和D2 cm3值以及靶区一致性指数(CI)和靶区适形指数(COIN)。其中D90是指包含90%靶区体积的剂量,D100是指包含100%靶区体积的剂量;V100、V150、V200、V300表示100%、150%、200%、300%及以上处方剂量包含靶区的体积百分比。通过计算得出CI值和COIN值:CI=CTVref/Vref,CTVref为接受≥100%剂量的HR-CTV的体积,Vref为接受≥100%剂量的体积;CI值越接近1说明处方剂量落在靶区外的剂量越少。COIN=TC×CI,TC=CTVref/VCTV, 式中,VCTV为HR-CTV的体积[4];COIN值越接近1,说明处方剂量线与靶区的适形度越高。
6.统计学处理:数据符合正态分布,用x±s表示。采用SPSS 16.0软件进行分析,对两种计划方式的剂量学参数进行配对t检验。P < 0.05为差异有统计学意义。
结果1. IPSA与GRO计划参数比较:与GRO相比,IPSA提高了靶区覆盖度(D90、V100)(t=-4.742、-4.823,P < 0.05),两组计划方式的D100差异无统计学意义(P>0.05)。IPSA与GRO的靶区高量(V150、V200、V300)比较差异无统计学意义(P>0.05)。GRO计划的CI、COIN高于IPSA(t=9.642、8.783,P < 0.05)。危及器官:IPSA与GRO的膀胱D1 cm3和D2 cm3差异均无统计学意义(P>0.05);IPSA直肠的D1 cm3较GRO降低7 cGy(t=2.070, P < 0.05),但直肠的D2 cm3两者比较差异无统计学意义(P>0.05)。见表 1、图 1。
|
|
表 1 GRO与IPSA的剂量学参数比较(x±s) Table 1 Dosimetric comparison between IPSA and GRO plans(x±s) |
|
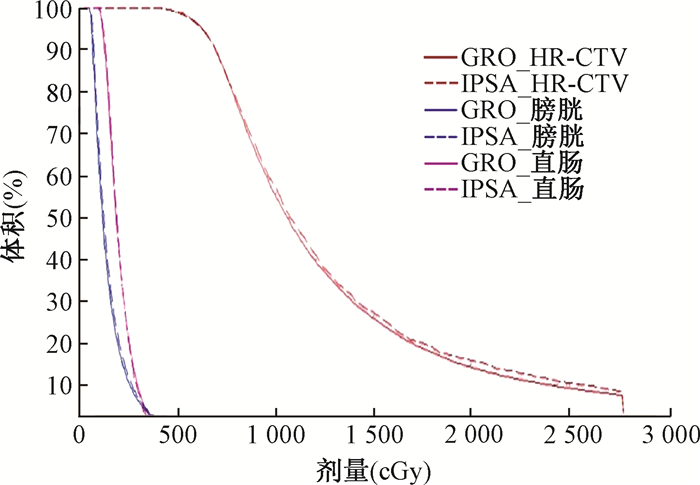
注:GRO.图形拖拽的正向优化;IPSA.模拟退火的逆向优化 图 1 1例宫颈癌患者GRO和IPSA计划的剂量体积直方图 Figure 1 Typical Dose-Volume Histogram of GRO and IPSA plans |
2.插植针管数对两种计划方式的影响:宫腔管联合1根插植针时,IPSA较GRO的平均D90只提高了4 cGy(P>0.05),但随着插植针管数的增加,IPSA相比于GRO,D90提高的幅度也逐渐增加,当增加到4根插植针时,IPSA较GRO的平均D90增加了14 cGy(t=-3.180,P < 0.05)。同样,与GRO相比,IPSA的V100提高的幅度也随着插植针管数的增加而逐渐增加。IPSA与GRO两种计划方式中膀胱、直肠的D1 cm3和D2 cm3相近,且受插植针管数的影响不大(表 2~5)。
|
|
表 2 宫腔管+1根插植针时的IPSA与GRO相关参数比较(x±s) Table 2 Dosimetric comparison between IPSA and GRO plans for patients treated by tandem combined with one needle(x±s) |
|
|
表 3 宫腔管+2根插植针时的IPSA与GRO相关参数比较 Table 3 Dosimetric comparison between IPSA and GRO plans for patients treated by tandem combined with two needles |
|
|
表 4 宫腔管+3根插植针时的IPSA与GRO相关参数比较 Table 4 Dosimetric comparison between IPSA and GRO plans for patients treated by tandem combined with three needles |
|
|
表 5 宫腔管+4根插植针时的IPSA与GRO相关参数比较 Table 5 Dosimetric comparison between IPSA and GRO plans for patients treated by tandem combined with four needles |
讨论
随着CT、磁共振成像(MRI)等影像技术在后装放疗中的应用,三维腔内后装相对于传统的二维腔内后装显著改善了放疗的剂量学结果[11]。Oncentra® Brachy V4.3三维治疗计划系统可完成GRO和IPSA两种三维后装治疗计划。在实际工作中, 对于部分病例使用GRO并不能获得临床上满意的剂量分布结果。相关的研究认为,逆向计划的IPSA方式相对于正向计划的GRO方式在不牺牲靶区覆盖度和危及器官受量的前提下,具有更高的靶区适形度和均一度[12]。Palmqvist等[4]研究认为,只要选择合适的参数,IPSA的计划质量将优于GRO计划。前期研究中已经对IPSA的优化参数进行了探讨[6],本研究在前期的基础上制定了IPSA函数模板,调用函数模板首次优化后,再根据具体的剂量分布情况,通过多次调整相关函数和权重不断进行优化,直到获得临床上满意的剂量分布结果。最终的结果显示,IPSA计划较GRO计划可以提高靶区覆盖度,同时未显著增加靶区内的高量和直肠、膀胱的受量。这与其他的相关研究结果类似[3, 13]。说明通过拖拽剂量线的GRO正向优化方式虽然直观,然而往往在某一CT层面拖拽剂量线后,由于放射源驻留时间的改变,在该层面上下几层的剂量分布也往往会受到影响而导致剂量分布变差;而IPSA借助计算机强大的运算能力,可以将整个靶区和周围危及器官的关系纳入考虑来优化剂量分布,因而,得到的剂量分布结果更佳,制定计划所需时间也相对GRO缩短[14-16]。
虽然IPSA较GRO可以改善靶区覆盖度,但对于以宫腔管联合阴道管为施源器的后装计划来说,如果初始使用GRO并未获得临床满意的剂量分布,再次应用IPSA重新制定计划并不能从本质上大幅度提高计划的质量[7]。Liu等[17]研究认为,当施源器为宫腔管联合插植针时,其在剂量学上会相对于宫腔管联合阴道管这种传统三维后装施源方式有明显的优势。其他研究也发现当施源器为环形施源器或宫腔管联合插植针时,IPSA可以大幅度提高靶区的覆盖度[8-9]。这可能是因为,宫腔管联合插植针或者环形施源器的方式相对于传统的三管施源器,增加了施源管数,进而增加了逆向算法的优化空间;而且由于插植针可以根据病变的范围选择植入的位置和数量,相比于阴道管只能局限的置于阴道穹窿处,使得计算机在统筹优化时有更多的放射源驻留位以供选择,因而进一步增加了优化空间,可以做到更加巧妙的使得危及器官的受照剂量更低且靶区的覆盖度更高。然而,本研究中,IPSA较GRO虽然可以改善剂量分布,但平均D90只提高了0.09 Gy,远低于Yoshio等[9]报道的1.64 Gy。这是因为在植入插植针时,如果靶区剂量不满意或者插植针太靠近危及器官,Yoshio等[9]会选择对患者重新植入插植针,以获得满意的剂量分布;而本中心为了减少和避免反复插入插植针对患者的损伤和可能造成的危险,往往对患者一次治疗只行一次插植,如果剂量分布不满意,在保证危及器官接受的剂量不超限的情况下,日后对该患者再追加一次后装治疗以补足GYN GEC-ESTRO指南推荐的靶区剂量。这样就导致了Yoshio插植针的分布方式相对于本研究可能会更加合理。在实际工作中,发现如果插植针相对于病灶没有很好的分散开而聚成一堆,则会造成大量的驻留位在三维空间中的距离十分靠近,使得这些不同施源管的驻留位只在局部病灶起作用,而其他病灶区则缺乏驻留位,进而影响了计算机优化的空间。因此,Yoshio逆向计划的结果提高的幅度优于我们的结果,可能得益于插植针布置地更加合理而使得计算机有了更大的优化空间。类似的,本研究发现,随着插植针管数的增多,靶区覆盖度提高的幅度也明显增加,这可能也与增加施源管数会增加IPSA的优化空间有关。
总之,IPSA较GRO可以显著改善靶区覆盖度,并且随着插植针管数的增加,靶区的覆盖度也明显提高。合理的植入插植针、增加插植针管数可能是显著改进三维后装剂量分布的一种方式。
志谢 感谢广西医科大学青年科学基金(GXMUYSF201627)对本研究的支持利益冲突 无
作者贡献声明 谭华艳搜集和整理数据、统计分析和起草论文;刘志杰设计研究方案和修改论文;付庆国指导论文和试验进行;杨海明、杨超凤负责病例筛选;邓烨、罗庭军负责放疗计划设计
| [1] |
陈文娟, 江楠, 倪晓雷, 等. 宫颈癌图像引导下调强放疗中危及器官变化对靶区的影响[J]. 中国癌症防治杂志, 2018, 10(2): 109-113. Chen WJ, Jiang N, Ni XL, et al. Effect of changes in organs at risk on target volume during image-guided radiation therapy for cervical cancer[J]. Chin J Oncol Prev Treat, 2018, 10(2): 109-113. DOI:10.3969/j.issn.1674-5671.2018.02.08 |
| [2] |
刘忠山, 赵杨祉, 郭杰, 等. CT引导下局部晚期宫颈癌组织间插植近距离治疗剂量学分析[J]. 中华放射肿瘤学杂志, 2017, 26(5): 550-554. Liu ZS, Zhao YZ, Guo J, et al. CT-guided interstitial brachytherapy for locally advanced cervical cancer:introduction of the technique and report of dosimetry[J]. Chin J Radiat Oncol, 2017, 26(5): 550-554. DOI:10.3760/cma.j.issn.1004-4221.2017.05.015 |
| [3] |
Kannan RA, Gururajachar JM, Ponni A, et al. Comparison of manual and inverse optimisation techniques in high dose rate intracavitary brachytherapy of cervical cancer:A dosimetric study[J]. Reports Prac Oncol Radiother, 2015, 20(5): 365-369. DOI:10.1016/j.rpor.2015.05.003 |
| [4] |
Palmqvist T, Dybdahl WA, Langeland MAB, et al. Dosimetric evaluation of manually and inversely optimized treatment planning for high dose rate brachytherapy of cervical cancer[J]. Acta Oncol, 2014, 53(8): 1012-1018. DOI:10.3109/0284186X.2014.928829 |
| [5] |
Pelagade S, Maddirala HR, Misra R, et al. Dosimetric comparison of volume-based and inverse planning simulated annealing-based dose optimizations for high-dose rate brachytherapy[J]. Med Dosim, 2015, 40(3): 235-239. DOI:10.1016/j.meddos.2015.01.003 |
| [6] |
刘志杰, 朱小东, 付庆国, 等. 逆向优化算法在宫颈癌三维近距离放疗计划制定中的应用[J]. 广西医学, 2017, 39(12): 1805-1807. Liu ZJ, Zhu XD, Fu QG, et al. Application of inverse planning simulated annealing to fomulating three-dimensional radiobrachytherapy plans for cervical cancer[J]. Guangxi Med J, 2017, 39(12): 1805-1807. DOI:10.11675/j.issn.0253-4304.2017.12.11 |
| [7] |
Liu Z, Liang H, Wang X, et al. Comparison of graphical optimization or IPSA for improving brachytheraphy plans associated with inadequate target coverage for cervical cancer[J]. Sci Rep, 2017, 7(1): 16423. DOI:10.1038/s41598-017-16756-w |
| [8] |
Jamema S, Mahantshetty U, Deshpande D, et al. Does help structures play a role in reducing the variation of dwell time in IPSA planning for gynaecological brachytherapy application?[J]. J Contemp Brachyther, 2011, 3(3): 142-149. DOI:10.5114/jcb.2011.24821 |
| [9] |
Yoshio K, Murakami N, Morota M, et al. Inverse planning for combination of intracavitary and interstitial brachytherapy for locally advanced cervical cancer[J]. J Radiat Res, 2013, 54(6): 1146-1152. DOI:10.1093/jrr/rrt072 |
| [10] |
张宁, 程光惠. 宫颈癌腔内联合组织间插植近距离放疗应用进展[J]. 中华放射肿瘤学杂志, 2016, 25(8): 895-901. Zhang N, Cheng GH. Recent advances of intracavitary/interstitial brachytherapy in cervical cancer[J]. Chin J Radiat Oncol, 2016, 25(8): 895-901. DOI:10.3760/cma.j.issn.1004-4221.2016.08.023 |
| [11] |
晏俊芳, 于浪, 孙玉亮, 等. 以CT图像为基础的宫颈癌三维腔内放疗[J]. 中华放射肿瘤学杂志, 2014, 23(5): 377-381. Yan JF, Yu L, Sun YL, et al. A clinical study of CT image-based 3D brachytherapy for cervical cancer[J]. Chin J Radiat Oncol, 2014, 23(5): 377-381. DOI:10.3760/cma.j.issn.1004-4221.2014.05.002 |
| [12] |
Jamema SV, Sharma S, Mahantshetty U, et al. Comparison of IPSA with dose-point optimization and manual optimization for interstitial template brachytherapy for gynecologic cancers[J]. Brachytherapy, 2011, 10(4): 306-312. DOI:10.1016/j.brachy.2010.08.011 |
| [13] |
Palmqvist T, Dos SML, Marthinsen AB, et al. Radiobiological treatment planning evaluation of inverse planning simulated annealing for cervical cancer high-dose-rate brachytherapy[J]. Anticancer Res, 2015, 35(2): 935-939. |
| [14] |
Sharma M, Fields EC, Todor DA. A novel two-step optimization method for tandem and ovoid high-dose-rate brachytherapy treatment for locally advanced cervical cancer[J]. Brachytherapy, 2015, 14(5): 613-618. DOI:10.1016/j.brachy.2015.05.003 |
| [15] |
Jameson MG, Ohanessian L, Batumalai V, et al. Comparison of Oncentra® Brachy IPSA and graphical optimisation techniques:a case study of HDR brachytherapy head and neck and prostate plans[J]. J Med Radiat Sci, 2015, 62(2): 168-174. DOI:10.1002/jmrs.107 |
| [16] |
Dinkla AM, van der Laarse R, Kaljouw E, et al. A comparison of inverse optimization algorithms for HDR/PDR prostate brachytherapy treatment planning[J]. Brachytherapy, 2015, 14(2): 279-288. DOI:10.1016/j.brachy.2014.09.006 |
| [17] |
Liu ZS, Guo J, Zhao YZ, et al. Computed tomography-guided interstitial brachytherapy for locally advanced cervical cancer:introduction of the technique and a comparison of dosimetry with conventional intracavitary brachytherapy[J]. Int J Gynecol Cancer, 2017, 27(4): 768-775. DOI:10.1097/IGC.0000000000000929 |
 2019, Vol. 39
2019, Vol. 39


