2. 100013 北京全域医疗技术有限公司
2. Beijing Allcure Medical Technology Co., Ltd, Beijing 100013, China
鼻咽癌是我国高发的恶性肿瘤之一,放射治疗是首选治疗方式,一直以来,因鼻咽癌具有临床靶区复杂、处方剂量要求严格、危及器官众多的特点,造成治疗计划设计难度增加,计划设计时间增多。调强放射治疗(IMRT)以其良好的适形度,紧凑的剂量收敛能力和危及器官剂量限制能力,成为目前鼻咽癌放射治疗的主流技术之一[1]。鼻咽癌的治疗计划设计,除了需要精确的靶区勾画,还需要有能力的物理师在设计计划时,手动尝试多种布野方式,修改优化参数,经过大量经验计算后设计完成满足临床需求的治疗计划。对于较为复杂的计划靶区,将耗费更多时间和人力去完成治疗计划的设计。因此为了提高治疗计划设计的效率,降低人为造成的计划质量差异,自动计设计的理念与研究近年来在国内外放疗物理界得到持续发展[2]。本研究采用MD安德森癌症治疗中心(MDACC)研发、搭载Pinnacle3(荷兰Philips公司)9.10计划系统的MdaccAutoPlan自动计划设计软件,该软件目前处于调试改善阶段并未有相关文献做出明确的特性研究,使用此软件完成20例鼻咽癌初治患者的首程IMRT治疗计划,与河南省肿瘤医院肿瘤放射治疗中心通过人工设计的治疗计划进行剂量学、剂量分布情况和计划设计效率进行比较,并分析其临床应用的可行性。
材料与方法1.一般资料:病例选自于2016年10月至2017年6月在河南省肿瘤医院进行放疗的鼻咽癌患者,按照第7版国际抗癌联盟(UICC)分期标准,因患者期别不同会造成靶区结构差异过大,所以本研究为保证计划对比质量,仅从Ⅱ、Ⅲ期患者中筛选出20例,其中男性14例,女性6例,年龄为29~57岁(中位年龄43岁)。其中Ⅱ期12例,Ⅲ期8例。所选病例均已在Pinnacle3 9.10计划系统中实施临床治疗计划设计,对这些病例重新使用MdaccAutoPlan软件进行IMRT自动计划设计。
2.靶区勾画及处方剂量:靶区定义:GTV大体肿瘤体积,包括原发肿瘤靶区和转移淋巴结,CTV1为亚临床病灶及高危临床病灶靶区,CTV2为低危临床靶区及颈部淋巴结预防照射区。考虑患者呼吸运动和摆位误差因素,本研究将临床靶区均匀外扩0.5 cm后的体积定义为计划靶区,分别对应为PGTV、PTV1和PTV2。本次治疗为鼻咽癌的首程治疗计划,故本疗程处方剂量PGTV为60.2 Gy/28次、PTV1为56.0 Gy/28次、PTV2为50.4 Gy/28次。危及器官限量参照Quantec(2010版)危及器官限值标准,其中本研究中涉及的危及器官剂量限值如下:眼晶状体Dmax<10 Gy、视神经Dmax<54 Gy、视交叉Dmax<54 Gy、脑干D5%<54 Gy、腮腺D50%<35 Gy、腮腺V30<50%、脊髓Dmax<45 Gy、口腔Dmax<45 Gy。本研究暂未考虑第二疗程的5次加量的计划设计。
3.计划设计
(1) 人工计划设计:采用荷兰Philips公司Pinnacle39.10治疗计划系统,瓦里安600C/D加速器6 MV X射线。为保证计划可比性,由1名经验丰富的物理师制作治疗计划,使用IMRT治疗技术,射野设置为共面9照射野平均分配,射野角度按照逆时针排序分别为160°、120°、80°、40°、0°、320°、280°、240°和200°。最大子野数设置为100,最小子野面积为4 cm2,最小剂量监测跳数为4 MU。要求95%的PTV满足处方剂量。
(2) MdaccAutoPlan计划设计(MDAP):MDAP应用计算机编程语言进行数据表达,搭载于Pinnacle39.10计划系统,通过调用脚本,实现自动添加射野并通过穷举搜索策略筛选射野角度[3],辅助轮廓自动生成,其中包括了计划靶区的外扩结构、计划靶区外的多层环限制结构、危及器官的外扩、正常组织的限制轮廓、冷热点剂量的提取轮廓等,所有轮廓通过统一的命名规则,进行计算机语言的排列,从而在执行脚本的过程中计算机可以通过搜索轮廓名称将对应的轮廓添加优化条件,通过添加这些优化条件来提升计划质量,反复进行计划的自动优化[4],以智能辅助技术得到优秀的放疗计划。自动计划采用与人工计划设计相同的软硬件设置,由于自动计划具有自动添加照射野的功能,为保证计划可比性,将照射野总数设置为共面9照射野即最终共筛选出最优的9个照射野,其筛选原则是,首先通过共20射野同时参与运算,得到各个射野迭代函数最接近的解的值,通过其解的接近程度筛选最优的9个解,这9个最优解对应的即是自动计划认为最优的9个射野角度。由人工设计中的同一名物理师操作运行MDAP后完成自动计划设计。
4.计划评估:根据国际辐射单位和测量委员会(ICRU)83号报告[5]中对IMRT计划评估要求,评估靶区近似最小剂量D98%,近似最大剂量D2%,平均剂量Dmean,并引入靶区适形指数CI及靶区剂量均匀性指数HI。对脊髓、脑干、视神经、视交叉、眼晶状体评估最大剂量Dmax和平均剂量Dmean,对腮腺评估中位剂量D50%及腮腺体积中大于30 Gy的剂量体积V30。CI=(Vpref/Vptv)×(Vpref/Vref),式中Vpref为PTV被处方剂量包括的体积,cm3;Vptv为PTV的体积,cm3;Vref为处方剂量等剂量线所包绕的体积,cm3。HI=(D2%-D98%)/D50%,式中,D2%为2%靶区体积剂量,cGy;D98%、D50%同D2%。对比两种计划的剂量体积直方图(DVH)和等剂量线分布情况。
5.计划效率评估:一个完整治疗计划设计的时间可分为人工操作时间和计算机处理时间,因此在人工计划和MDAP计划设计时,分别记录人工操作时间和计算机处理时间,其中人工操作时间规定为所有需要物理师操作计算机的时间总和,计算机处理时间规定为物理师操作结束后计算机自主运行的时间总和。在自动计划设计中,物理师需要操作的部分为调用脚本前的计划设计步骤,即新建患者、导入图像和轮廓、重新命名轮廓、调用脚本并填写计划所需的参数要求如处方剂量、分次数、加速器型号等。对每一病例的两个计划中,定义:计划设计效率值E=人工操作时间/计算机处理时间;计划设计效率差A=E手动-E自动,其中E值的大小并不直接代表效率的高低,此定义仅仅通过A值确定两种计划的效率高低。当A>0,则说明人工计划设计的效率低于MDAP计划;A<0,则说明人工计划设计的效率高于MDAP计划。
6.统计学处理:使用SPSS 17.0软件分析,数据符合正态分布均采用x±s表示,应用t检验对两种放疗计划的剂量学参数进行比较。P<0.05为差异有统计学意义。
结果1.靶区剂量分布的比较:MDAP计划的PGTV D98%、PGTV Dmean、PTV1 D98%、PTV1 Dmean、PTV2 D98%、PTV2 Dmean的平均值较人工计划分别降低2.5%、0.3%、0.1%、0.5%、0.6%、1.0%,PGTV D2%、PTV1 D2%、PTV2 D2%的平均值较人工计划分别上升1.7%、1.5%、0.6%。其中PGTV D98%、PGTV D2%和PTV2 D98%两组比较差异具有统计学意义(t=5.519、6.701、0.937,P<0.05)。人工计划的PGTV CI和PGTV HI略优于MDAP计划,但差异无统计学意义(t=3.181、3.290,P<0.05,表 1)。
|
|
表 1 两种治疗计划靶区剂量学比较(cGy,x±s) Table 1 Dosimetric comparison on treatment planning target areas between two methods (cGy, x±s) |
2.危及器官剂量:MDAP计划的右侧腮腺D50%、左侧腮腺D50%、脊髓Dmax、脊髓Dmean的平均值较人工计划分别减少24.8%、27.7%、11.4%、14.0%,两组比较,差异具有统计学意义(t=5.447、5.375、6.786、3.810,P<0.05)。MDAP计划的两侧眼晶状体Dmax的平均值较人工计划分别升高65.0%、19.3%,两组比较,差异有统计学意义(t=9.863、3.440,P<0.05),视神经、视交叉和脑干两组比较差异均无统计学意义(表 2)。
|
|
表 2 两种治疗计划危及器官剂量学比较(cGy,x±s) Table 2 Dosimetric comparison on OARS between two methods (cGy, x±s) |
3.计划总MU的对比:MDAP计划的总MU数为764±73.2,人工计划的总MU数为715±77.8。MDAP计划的总MU数平均值较人工计划增加了6%,两组数据比较差异无统计学意义(P>0.05)。
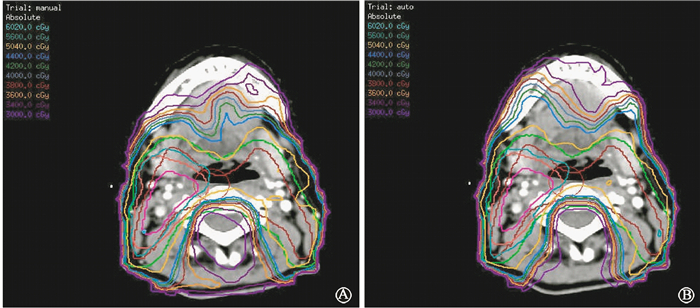
4.等剂量线分布的比较:MDAP计划的后颈区剂量分布略优于人工计划。在重要危及器官脑干和脊髓附近的靶区评价中,人工计划略优于MDAP计划,从DVH图中得出,MDAP计划的脑干脊髓剂量受量均低于人工计划,因此人工计划靶区的曲线优于MDAP,其余部位剂量分布无明显差异,低剂量区的收敛程度与人工计划无明显差异(图 1,2)。
|
图 1 两种治疗计划后颈区剂量分布图示例A.MDAP计划;B.人工计划 Figure 1 Typical dosimetric distributions on post neck area for two planning methos, A. MDAP plans; B. Manual plans |

|
图 2 两种治疗计划的靶区与脑干、脊髓的剂量体积直方图 Figure 2 Dose volume histograms with planning target volumes, brainstem and spinal cord for two planning methods |
5.计划完成时间和计划完成效率比较:人工计划中,计划设计的人工操作时间为(29.95±3.07)min,计算机处理时间为(35.40±4.49)min;MDAP计划的人工操作时间为(12.15±1.49)min,计算机处理时间为(47.60±4.08)min;MDAP计划的人工操作时间较人工计划减少了59.4%,计算机处理时间较人工计划增加了34.4%。两者的计划设计效率差A为0.58±0.11。
讨论近年来,IMRT一直作为放射治疗的主流技术,并且随着容积旋转调强放疗(VMAT)、螺旋断层放疗(TomoTherapy)等越来越多的新技术的出现,对IMRT的发展和理念也产生巨大的促进作用。国内目前临床放射治疗应用中,IMRT依旧是最重要的技术之一。IMRT治疗计划设计中,其中心思想是照射野的分布和优化参数的设置,因此高质量的IMRT治疗计划设计需要一名实践经验丰富的物理师通过多次试验,花费大量时间才能够完成。随着人工智能理念的广泛应用,为实现治疗计划设计的自动实施,本研究引进MDAP软件,尝试提高IMRT治疗计划设计的效率和质量,试图将其应用于临床。
本研究选取了20例鼻咽癌初治患者,通过对比MDAP软件设计和人工设计的治疗计划剂量学差异发现,在靶区剂量分布方面,人工计划的靶区在点剂量评估(D98%,D2%)、CI、HI[5]均略优于MDAP,这可能是由于MDAP在优化中不断增加和修改目标函数的设置导致了最优解的不断改变,运行中的目标函数为不可控因素,其目标是计划靶区和危及器官达到最优解数值的平衡,而人工计划更着重于危及器官在耐受范围内得到更优的计划靶区,虽然保证了完全一致的开始,但两者在计划设计的思路上存在了一定的差异,因此计划靶区最小剂量平均降低了近1.1%,但笔者认为这并不能说明MDAP的计划质量无法满足临床需求。MDAP对于危及器官和其他危及体积(RVR)的剂量限制优于人工计划设计,例如腮腺、脊髓、后颈部等,但在眼晶状体的剂量限制中,MDAP与人工计划存在明显差距,笔者认为因MDAP计划设计中,充分利用计划危及器官靶区(planning organ at risk volume,PRV)对危及器官轮廓的修正和限制,同时在设置优化参数时,采取吸收剂量与等效生物剂量同时限制的手段[7],缩小对危及器官剂量限制的目标函数的求解范围,故对于危及器官的剂量计算更加充分,得到更优解,这也与MDAP计划靶区最小剂量略微降低的结果相对应,但MDAP中眼晶状体的剂量明显高于人工计划,这可能与MDAP研发时对于眼晶状体剂量限值要求与本中心有较大差异有关,因此对于眼晶状体剂量限制的目标函数有更广泛的解,造成计划结果中眼晶状体的最大剂量明显高于本中心人工计划,在后续研究中将尝试对优化条件的循环进行调整,尝试改变眼晶状体的判断条件从而得到更好的计划质量[8]。在对治疗计划剂量分布情况的研究中发现,人工计划对于靶区与危及器官较近或有重叠时,计划靶区剂量分布更优,这可能由于MDAP单纯使用目标函数的当前最优解进行计划结果的判断,是一种仅靠数学方法的判断模式,而人工计划则更多的通过直观判断与经验相结合的手段完成治疗计划设计。在计划设计效率比较中,MDAP的物理师操作时间明显低于人工计划,且计划效率差A值大于0,说明MDAP的计划设计效率可能优于人工计划,能够尽可能缩短物理师计划设计的常规操作时间,对于提高物理师临床工作效率有一定提升。
Tol等[9]应用Rapid Plan技术研究了20例头颈部肿瘤患者的治疗计划,评估该技术的应用价值。对于计划中的危及器官,在预测和实际达到的平均剂量之间发现具有显著线性相关关系(R2=0.94~0.99)。Rapid Plan通常会高估危及器官与计划靶区重叠部分体积的剂量限制能力。独立应用Rapid Plan Quality Assurance的剂量预测功能可以确定,10例手动优化的计划中复合唾液腺,口腔或复合吞咽肌的剂量至少可以降低3、5或7 Gy,对比其中4例Automatic Interactively Optimized计划也可印证上述结果。这表明使用Rapid Plan DVH预测头颈部自动计划的计划质量是可行的,已应用于多家中心和临床试验中。本研究中MDAP软件是一种经验性、循环判断性的执行方式,并不以庞大的数据库直接作为计划完成和评估的判断基准,而是以原始开发者所收集的大量经验数据所推导出的计算机函数判断语句构成,因此不能完成对于计划中DVH的预测功能,但对于本研究的临床应用不造成根本的影响。
Krayenbuehl等[10]选取50例头颈部肿瘤患者,应用Pinnacle3计划系统的Auto-Planning技术与Eclipse VMAT技术设计的治疗计划进行对比发现,PTV的剂量覆盖和剂量均匀性在自动计划中有显著改善,危及器官例如腮腺、口腔黏膜、吞咽肌、后颈区的平均剂量和脊髓的最大剂量显著降低,在64%的计划中,任一危及器官(不包括脊髓)的平均剂量降低至少20%。与手动计划相比,使用自动计划的平均有效工作时间分别为(3.8±1.1)和(48.5±6.0)min。使用自动计划大大降低了有效工作时间。此结果与本研究中关于计划效率的结果相一致,MDAP软件的运用也可以有效的降低物理师的操作时间,使用计算机去完成更多的工作与运算,从而提高物理师在临床中的工作效率。本研究所使用的MDAP与Pinnacle3计划系统的Auto-Planning有着相似的运行机理,但其本质不同,MDAP是一种计算机语言式的循环判断过程,是一种正向的计划设计流程,最终得到的计划是通过计算机语言判断得到的一个完整的循环,可一键完成从轮廓逻辑处理到优化计算结束的工作。在临床工作中,为使计划做到精益求精,笔者认为可以对MDAP和人工计划加以结合,以MDAP作为快速完成治疗计划的基准,加以物理师对于计划靶区的主观判断,从而更加快捷的得出更优的治疗计划。
综上所述,MDAP软件对于鼻咽癌的放射治疗计划设计有一定的临床应用价值,在靶区剂量学差异很小的情况下,危及器官剂量有一定降低,并且能够明显提高治疗计划设计效率,减少人工参与时间,但这种以智能辅助,一键式操作方法的自动计划设计软件尚未在国内外广泛使用,还需要进一步的临床研究与分析。
利益冲突 全体作者未因进行研究而接受任何不正当的职务或财务利益,在此对研究的独立性和科学性予以保证作者贡献声明 程志垚负责收集文献、采集数据和撰写初稿;李定杰修改和完善论文;吴慧、黄蓉负责筛选病例和临床内容指导;尹小芳、王枫负责软件的调试和维护工作
| [1] |
Sheng K, Molloy JA, Read PW. Intensity-modulated radiation therapy (IMRT) dosimetry of the head and neck:a comparison of treatment plans using linear accelerator-based IMRT and helical TomoTherapy[J]. Int J Radiat Oncol Biol Phys, 2006, 65(3): 917-923. DOI:10.1016/j.ijrobp.2006.02.038 |
| [2] |
Nelms BE, Robinson G, Markham J, et al. Variation in external beam treatment plan quality:An inter-institutional study of planners and planning systems[J]. Pract Radiat Oncol, 2012, 2(4): 296-305. DOI:10.1016/j.prro.2011.11.012 |
| [3] |
Wang X, Zhang X, Dong L, et al. Development of methods for beam angle optimization for IMRT using an accelerated exhaustive search strategy[J]. Int J Radiat Oncol Biol Phys, 2004, 60(4): 1325-1337. DOI:10.1016/j.ijrobp.2004.06.007 |
| [4] |
Zhang X, Yang Y, Jiang S, et al. Combining automatic contouring and automatic planning to achieve the fully automatic planning for head and neck cancer[J]. Int J Radiat Oncol Biol Phys, 2015, 93(3): E623. DOI:10.1016/j.ijrobp.2015.07.2136 |
| [5] |
International Commission on Radiation Units and Measurements. ICRU Report No 83. prescribing, recording and reporting photon-beam intensity-modulated radiation therapy (IMRT)][J]. Oxford; ICRU, 2010. |
| [6] |
Zhang X, Li X, Quan EM, et al. A methodology for automatic intensity-modulated radiation treatment planning for lung cancer[J]. Phys Med Biol, 2011, 56(13): 3873-3893. DOI:10.1088/0031-9155/56/13/009 |
| [7] |
Thomas E, Chapet O, Kessler ML, et al. Benefit of using biologic parameters (EUD and NTCP) in IMRT optimization for treatment of intrahepatic tumors[J]. Int J Radiat Oncol Biol Phys, 2005, 62(2): 571-578. DOI:10.1016/j.ijrobp.2005.02.033 |
| [8] |
Hansen CR, Bertelsena A, Hazella I, et al. Automatic treatment planning improves the clinical quality of head and neck cancer treatment plans[J]. Clini & Translat Radiat Oncol, 2016, 119: S396-S397. DOI:10.1016/j.ctro.2016.08.001 |
| [9] |
Tol JP, Dahele M, Delaney AR, et al. Can knowledge-based DVH predictions be used for automated, individualized quality assurance of radiotherapy treatment plans?[J]. Radiat Oncol, 2015, 10(1): 234. DOI:10.1186/s13014-015-0542-1 |
| [10] |
Krayenbuehl J, Norton I, Studer G, et al. Evaluation of an automated knowledge based treatment planning system for head and neck[J]. Radiat Oncol, 2015, 10(1): 226. DOI:10.1186/s13014-015-0533-2 |
 2018, Vol. 38
2018, Vol. 38


