2. 200040 上海, 复旦大学附属华东医院放疗科
2. Department of Radiotherapy, Huadong Hospital Affiliated to Fudan University, Shanghai 200040, China
乳腺癌是危害女性健康最常见的恶性肿瘤,其发病率呈逐年上升的趋势,并呈现年轻化的趋势[1]。放射治疗是早期乳腺癌治疗的重要手段之一。在对单侧乳腺癌患者进行放射治疗过程中,健侧乳腺距离靶区较近,难免会受到不必要的照射,理论上有可能诱发健侧乳腺癌[2]。为此,本研究在统计分析健侧乳腺受照剂量的基础上,使用包含特定器官和暴露年龄以及相应发病率参数的美国电离辐射生物效应委员会报告Ⅶ第2部分(BEIR Ⅶ phase 2)推荐的风险模型[3],估算了单侧乳腺癌患者接受放射治疗诱发健侧乳腺癌的终生归因风险(lifetime attribute risk,LAR)[2, 4-5],以期大致了解其诱发健侧乳腺癌风险的水平,并为今后降低相应风险提供参考建议。
资料与方法1.调查对象与内容:复旦大学附属华东医院2016年1月到6月期间共开展单侧乳腺癌放射治疗49例(左侧25例,右侧24例),所有患者的处方剂量均为5 000 cGy/25次。放射治疗计划在治疗计划系统(Eclipse V13.6®,Varian medical systems)中生成,采用6 MV X射线,治疗方案均采用共面的切线野,处方剂量统一设置为100%的等剂量线包绕90%的计划靶区体积(PTV)。从放射治疗计划系统中得到患者的相关信息,包括年龄、放疗过程中健侧乳腺受到的平均剂量、最大点剂量(剂量网格大小为2 mm×2 mm×2 mm)等。
2.乳腺癌二次风险模型:电离辐射诱发癌症风险预测的基本模型采用BEIR Ⅶ phase 2推荐的线性无阈模型[3]。其LAR是基于超额绝对风险与超额相对风险基础上获取的,每10万人接受100 mGy的辐射照射后诱发癌症的LAR定义为:
| $\begin{array}{l} LAR\left( {D,e} \right) = {\left[ {\sum\limits_a^{100} {ERR\left( {D,e,a} \right)\lambda _I^CS\left( a \right)/S\left( e \right)} } \right]^{{t_1}}}\\ \quad \quad \quad {\left[ {\sum\limits_a^{100} {EAR\left( {D,e,a} \right)S\left( a \right)/S\left( e \right)} } \right]^{{t_2}}} \end{array}$ | (1) |
式中,D为器官吸收剂量,Gy;e为患者受照时的年龄,岁;a为到达年龄(即受照年龄+潜伏期),岁;λIC为各个癌症部位在到达年龄时的性别全人口的基线癌症发病率,10-5;S(a)为存活到年龄为a时的生存概率,%;S(a)/S(e)是以年龄e存活为条件存活到年龄a的生存概率,%;t1和t2分别表示相对风险转移和绝对风险转移的不同权重,%。
基于Preston等[6]对8个队列的乳腺癌发病率和寿命队列研究的综合分析,发现乳腺癌更符合超额绝对风险模型[公式(1)中的t1和t2可分别取为0和1],其潜伏期约为5年;取剂量/剂量率因子(DDREF)为1.5,BEIR Ⅶ给出每万人每年接受1 Gy电离辐射可诱发乳腺癌的超额绝对风险(EAR)计算公式如下:
| ${\rm{EAR = 9}}{\rm{.9exp}}\left[ { - 0.05\left( {e - 30} \right)} \right]{\left( {\frac{a}{{60}}} \right)^\eta }$ | (2) |
式中,η为到达年龄的指数(a<50时,η=3.5;a≥50时,η=1)。
生存概率S和死亡概率iqx的计算公式如下:
| $S = 1{ - _i}{q_x}$ | (3) |
| $_i{q_x} = \frac{{2 \times i{ \times _i}{m_x}}}{{2 + i{ \times _i}{m_x}}}$ | (4) |
式中,i为年龄组距,岁;x为实足年龄,岁;imx为不同性别年龄别的死亡率,10-3。
3.统计学处理:采用STATA 14.0软件对健侧乳腺剂量进行分析。不同年龄段健侧乳腺平均剂量的比较采用多组比较的秩和检验,健侧乳腺最大剂量和平均剂量的相关分析使用Pearson相关分析。P<0.05为差异有统计学意义。
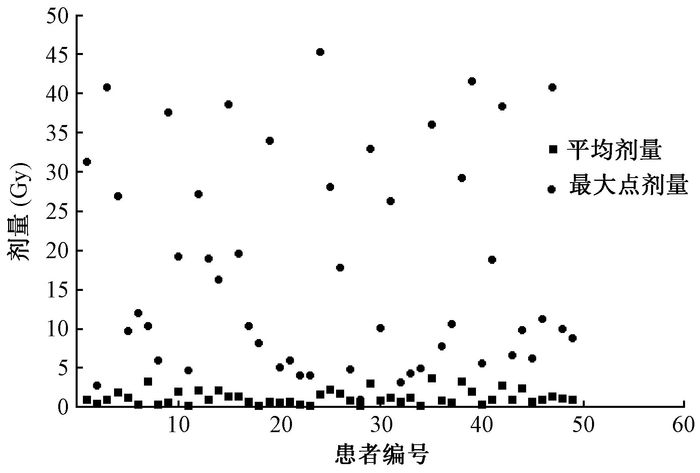
结果1.健侧乳腺剂量:49例患者的年龄分布和不同年龄段患者健侧乳腺的平均剂量见表 1。经检验,不同年龄段的患者平均剂量差异无统计学意义(P>0.05)。49例患者健侧乳腺的平均剂量和最大点剂量的散点分布见图 1。经统计,健侧乳腺的平均剂量在0.14~3.59 Gy之间,健侧乳腺的最大点剂量在0.98~45.27 Gy之间,不同患者健侧乳腺平均剂量和最大点剂量变化幅度很大,此现象可以解释为不同患者的健侧乳腺腺体大小、健侧乳腺与治疗靶区距离、放疗医师对靶区的勾画等不同导致的;经Pearson相关分析,发现健侧乳腺的最大点剂量与平均剂量呈显著正相关(R=0.527,P=0.000)。
|
|
表 1 不同年龄段患者健侧乳腺的平均剂量分布(Gy,x±s) Table 1 Distribution of the ages and mean doses in contra-lateral breasts(Gy, x±s) |
|
图 1 患者健侧乳腺的平均剂量和最大点剂量分布 Figure 1 Distribution of the mean and maximum point doses in the contra-lateral breasts |
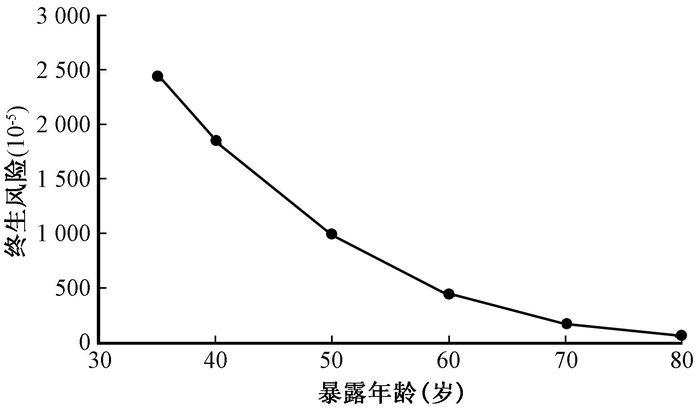
2.终生归因风险:基于BEIR Ⅶ的终生归因风险模型,并结合我国人口寿命表[7],预测出我国35~80岁女性接受单侧乳腺癌放疗可能诱发的健侧乳腺癌风险如图 2所示。图 2的预测结果是以健侧乳腺受到的平均剂量1.21 Gy作为剂量参考值,终生风险表示每10万该年龄段单侧乳腺癌患者接受放射治疗后可能发生健侧乳腺癌的人数。当受照年龄为35、40、50、60、70、80岁时,其健侧乳腺癌的终生风险分别为2 449/10万人、1 857/10万人、994/10万人、446/10万人、173/10万人、55/10万人。从图中可以看出,单侧乳腺癌患者,接受放疗所致健侧乳腺癌的终生归因风险与受照年龄关系很大。较之于我国女性乳腺癌的基线风险3 340/10万人口[8],单侧乳腺癌放疗可能诱发健侧乳腺癌的终生风险在上述6个年龄段分别可增加73.3%、55.6%、29.8%、13.4%、5.2%和1.6%。
|
图 2 不同暴露年龄健侧乳腺癌的终生风险 Figure 2 LAR of contra-lateral breast cancer and exposure ages |
讨论
从本研究结果可看出,虽然单侧乳腺癌患者治疗的处方剂量相同(50 Gy),但不同患者健侧乳腺平均剂量却有很大差异(0.14~3.59 Gy),49例患者健侧乳腺平均剂量为1.21 Gy。对于同类研究,国内的王华芳[9]报道了15例单侧乳腺癌患者接受放射治疗的健侧乳腺平均剂量为(0.9±1.4)Gy,国外的Tamburella等[10]报道了49例接受单侧乳腺癌放疗患者,健侧乳腺平均剂量为(1.15±0.8)Gy。上述研究结果表明,单侧乳腺癌患者接受放射治疗的健侧乳腺平均剂量可达1 Gy量级,且不同患者的健侧乳腺平均剂量变化幅度很大。另一方面,在乳腺癌治疗过程中,通常还会用到X射线来进行定位或图像引导,这无疑还会增加健侧乳腺的受照剂量。Donovan等[11]研究表明,使用锥形束CT(CBCT)进行位置验证和图像引导,将增加乳腺癌放疗中危及器官(OAR)的剂量10%~20%。本研究还发现,在接受单侧乳腺癌治疗时,同一患者的健侧乳腺受照剂量很不均匀,最大点剂量的均值约为整个乳腺平均剂量的15倍。因此,在开展单侧乳腺癌放射治疗时,很有必要加强对健侧乳腺受照剂量的评价与控制。
从本研究结果可看出,单侧乳腺癌患者接受放射治疗后存在有不同程度地诱发健侧乳腺癌的终生风险,患者受照时年龄越小、风险越大。类似的研究结果和现象在苏垠平[12]研究X射线CT诊断所致女性乳腺癌的终生风险中也已有报道。若将单侧乳腺癌患者接受放疗所致健侧乳腺剂量和X射线CT诊断所致女性乳腺剂量进行剂量归一,两个研究预测出不同受照年龄段女性的乳腺癌终生风险均非常接近。本研究的结果表明,对于50岁以下的乳腺癌患者,其接受放射治疗所诱发的健侧乳腺癌终生风险可增加29.8%以上。但也有研究表明,罹患过单侧乳腺癌的患者,其对侧乳腺癌的发生率大约是普通人群的1.5~2倍[13],且对侧乳腺癌发生与确诊时年龄、激素受体状态、初诊肿瘤大小、治疗情况和家族史等因素有关[14]。因此,对于乳腺癌患者而言,较之于放射治疗可能诱发的乳腺癌风险,首先还必须肯定放射治疗的作用。不过,本研究也显示,对于40岁以下的青年患者,单侧乳腺癌放射治疗可能诱发健侧乳腺癌的终生风险仍可达基线水平的55%以上;另一方面,本研究也发现,在施行单侧乳腺癌放射治疗时,健侧乳腺的受照剂量仍有很大可控制的空间。为此,从放射防护最优化的原则出发,认为在开展乳腺癌放疗时,放疗医生还需精益求精,尽可能为每位患者设计出各自的最佳放疗方案,以减少对健侧乳腺以及其他正常组织的辐射照射。按照当前的剂量-效应线性无阈模型预测,若健侧乳腺平均剂量能减少一半,相应健侧乳腺癌风险也会降至原来的一半。
需要说明的是,本研究的剂量数据来源于单一医院且病例数较少,今后仍需进一步收集更多的数据来评价健侧乳腺的受照剂量。另外,本研究对健侧乳腺癌风险的预测也是基于线性无阈模型和器官剂量的概念,其结果的可信度还有待于今后基于流行病学等方法的研究来验证。
利益冲突 本研究所有作者均于投稿前阅读并认可研究内容,不存在任何潜在利益冲突,排名无争议;本人与本人家属、其他研究者,未接受任何不正当的职务或财务利益,对研究的独立性和科学性予以保证作者贡献声明 黄莹负责数据整理、结果分析、论文撰写;卓维海负责研究设计和论文修改;刘海宽负责指导论文写作;郑向鹏负责患者临床诊疗;邱健健负责制定患者治疗方案及资料收集
| [1] |
李亚会, 张连花, 陈晓品. 早期乳腺癌保乳手术联合术中放疗研究进展[J]. 中华内分泌外科杂志, 2017, 11(2): 118-121. Li YH, Zhang LH, Chen XP. Progress of breast conserving surgery combined with intraoperative radiotherapy for early stage breast cancer[J]. Chin J Endocr Surg, 2017, 11(2): 118-121. DOI:10.3760/cma.j.issn.1674-6090.2017.02.008 |
| [2] |
Quinn A, Holloway L, Hardcastle N, et al. Normal tissue dose and second cancer risk due to megavoltage fan-beam CT, static tomotherapy and helical tomotherapy in breast radiotherapy[J]. Radiother Oncol, 2013, 108(2): 266-268. DOI:10.1016/j.radonc.2013.05.019 |
| [3] |
National Research Council of the National Academies. Health risks from exposure to low levels of ionizing radiation, BElR Ⅶ phase2[R]. Washington DC:National Academies Press, 2006.
|
| [4] |
Basaula D, Quinn A, Walker A, et al. Risks and benefits of reducing target volume margins in breast tangent radiotherapy[J]. Australas Phys Eng Sci Med, 2017, 40(2): 305-315. DOI:10.1007/s13246-017-0529-3 |
| [5] |
Lee B, Lee S, Sung J, et al. Radiotherapy-induced secondary cancer risk for breast cancer:3D conformal therapy versus IMRT versus VMAT[J]. J Radiol Prot, 2014, 34(2): 325. DOI:10.1088/0952-4746/34/2/325 |
| [6] |
Preston DL, Mattsson A, Holmberg E, et al. Radiation effects on breast cancer risk:a pooled analysis of eight cohorts[J]. Radiat Res, 2002, 158(2): 220-235. DOI:10.1667/0033-7587(2002)158[0220:REOBCR]2.0.CO;2 |
| [7] |
国家统计局. 中国人口和就业统计年鉴2009[M]. 北京: 中国统计出版社, 2009. National Bureau of Statistics of China. China population and employment statistics yearbook 2009[M]. Beijing: China Statistics Press, 2009. |
| [8] |
李小亮, 牛昊巍, 孙全富, 等. 我国辐射相关癌症终生危险基线值估计[J]. 中华放射医学与防护杂志, 2011, 31(6): 695-697. Li XL, Niu HW, Sun QF, et al. Estimation of lifetime risk baseline for radiation related cancers in China[J]. Chin J Radiol Med Prot, 2011, 31(6): 695-697. DOI:10.3760/cma.j.issn.0254-5098.2011.06.019 |
| [9] |
王华芳. 早期乳腺癌保乳术后4种放疗技术的剂量参数比较[D]. 乌鲁木齐: 新疆医科大学, 2014. Wang HF. A comparison of dose parameters for early stage breast cancer after breast-conserving surgery using different radiotherapy techniques[D]. Urumqi:Xinjiang Medical University, 2014. http://cdmd.cnki.com.cn/Article/CDMD-10760-1014422578.htm |
| [10] |
Tamburella C, Guibert G, Weber P, et al. Volumetric modulated arc therapy (VMAT) combined with deep inspiration breath hold (DIBH) technique for radiation therapy (RT) of the left breast[J]. Int J Radiat Oncol Biol Phys, 2016, 96(2): E45-E46. |
| [11] |
Donovan EM, Ciurlionis L, Fairfoul J, et al. Planning with intensity-modulated radiotherapy and tomotherapy to modulate dose across breast to reflect recurrence risk (IMPORT High trial)[J]. Int J Radiat Oncol Biol Phys, 2011, 79(4): 1064-1072. DOI:10.1016/j.ijrobp.2009.12.052 |
| [12] |
苏垠平. 部分地区X射线诊断照射频度调查及CT所致癌症风险的研究[D]. 北京: 中国疾病预防控制中心, 2014. Su YP. Research on the frequency of X-ray diagnostic radiation in some areas and the radiation cancer risk induced by CT[D]. Beijing:Chinese Center for Disease Control and Prevention, 2014. http://cdmd.cnki.com.cn/Article/CDMD-84501-1014348173.htm |
| [13] |
Saltzman BS, Malone KE, McDougall JA, et al. Estrogen receptor, progesterone receptor, and HER2-neu expression in first primary breast cancers and risk of second primary contralateral breast cancer[J]. Breast Cancer Res Treat, 2012, 135(3): 849-855. DOI:10.1007/s10549-012-2183-5 |
| [14] |
郑丽华, 刘荣, 张萌萌, 等. 对侧乳腺癌发生的危险因素[J]. 中华肿瘤杂志, 2015, 37(4): 241-243. Zheng LH, Liu R, Zhang MM, et al. The risk factors for contralateral breast cancer[J]. Chin J Oncol, 2015, 37(4): 241-243. DOI:10.3760/cma.j.issn.0253-3766.2015.04.001 |
 2017, Vol. 37
2017, Vol. 37


