食管癌患者的放疗疗效与固有的放射敏感性密切相关,在治疗早期找到能够预测放疗反应的方法有重要意义。磁共振弥散加权成像(diffusion-weighted magnetic resonance imaging,DWI)是分子功能成像代表之一,它可先于形态学变化早期发现肿瘤组织微环境改变[1]。近年来,应用DWI监测肿瘤放化疗反应在如非小细胞肺癌、直肠癌等均有报道[2-3],各国学者分别通过动物实验和临床研究对该成像技术的机制以及应用价值进行探索。在食管癌领域,国内也有学者通过临床研究发现DWI可作为一种有效手段预测食管癌的放化疗反应,但目前尚无关于食管癌动物实验的相关报道[4-6]。本研究拟从动物模型层面观察食管癌组织照射后DWI的图像及表观弥散系数(ADC)变化情况,探讨DWI在早期预测食管癌放疗反应的应用价值,为该种成像技术合理应用于临床提供理论依据。
材料与方法1.实验试剂及仪器:RPMI 1640培养基、胎牛血清和胰蛋白酶等购自美国GIBCO公司。德国西门子公司3.0T磁共振扫描仪及瑞典医科达Synergy VMAT直线加速器。
2.食管癌Eca-109移植瘤模型的建立:人食管癌Eca-109瘤系,由河北医科大学第四医院科研中心提供。免疫功能缺陷型BALB/c裸鼠(雄性,4~6周龄,体重18~20 g),购于北京维通利华实验动物技术有限公司,许可证号:CZSCXK(京)2012-0001。通过细胞贴壁培养及胰消化酶法扩增收集细胞悬液。接种部位为裸鼠右前肢背部,接种数量5×106/只。约12 d后即可形成最大径约10 mm的皮下移植瘤,选取移植瘤结节形状较规则、与肌肉皮肤无粘连的荷瘤裸鼠用于本实验。所有研究方案经河北医科大学第四医院动物保护委员会批准。
3.实验分组及照射方法:选取建模成功的24只荷瘤裸鼠,按照随机数表法分为两组:实验组14只,接受6 MV X射线15 Gy单次照射[9, 12]。射野2 cm×2 cm,源皮距100 cm,剂量率500 cGy/min,被覆1 cm的组织补偿膜。所有实验组的荷瘤裸鼠均取俯卧位固定于特制模具,在清醒状态下接受照射。对照组10只,不接受任何治疗。
4. MRI检查方法及图像分析:德国西门子3.0T磁共振扫描仪,loop线圈,实验组于照射前及照后1、6、13 d行MRI扫描,对照组在相同时间也进行MRI扫描。每次扫描前用2%戊巴比妥对荷瘤裸鼠进行腹腔注射麻醉(0.05 ml/只),并将荷瘤裸鼠包裹于鲜猪肉内放入loop线圈中。扫描序列包括T1WI、T2WI及DWI,其中DWI采用高清弥散序列,3 mm层厚,b值选取0、600 s/mm2。
图像分析由两名具有丰富经验的影像科医生完成,于DWI序列选取肿瘤最大层面,通过影像后处理工作站拟合ADC图像,随机在肿瘤组织内选取3个感兴趣区(ROI),避开血管、出血及坏死区,测量出ADC值,取其均值作为最终结果。测量照射前的ADC值(ADC0)和照射后的ADC值(ADCX,X=1、3、6),并计算ADC值的变化率,即ΔADCX=(ADCX-ADC0)/ADC0×100%。
5.移植瘤体积的测量:由同一测量者用电子游标卡尺来测量移植瘤的最大直径(a)及与之相垂直的短径(b),照射后第1周每天测量,之后每2天测量1次,直至照后24 d,根据公式VX=ab2/2计算体积大小,VX为照后X天移植瘤的体积。计算每只裸鼠移植瘤照射前后体积变化率,即ΔVX=(VX-V0)/V0×100%。
6.统计学处理:采用SPSS 21.0软件包行统计学分析。计量数据用x±s表示,正态性检验采用Kolmogorov-Smirnov(K-S)检验,两组移植瘤ADC及ΔADC、V和ΔV在不同时间点均符合正态分布。用重复测量的方差分析和多变量方差分析对治疗过程中不同时间点的ADC值及移植瘤体积进行统计分析和变化的描述;ADC值与肿瘤体积的相关分析采用Pearson相关分析法。P<0.05为差异有统计学意义。r>0.3为直线相关,0.3~0.5为低度相关,0.5~0.8为显著相关(中等程度相关),0.8以上为高度相关。
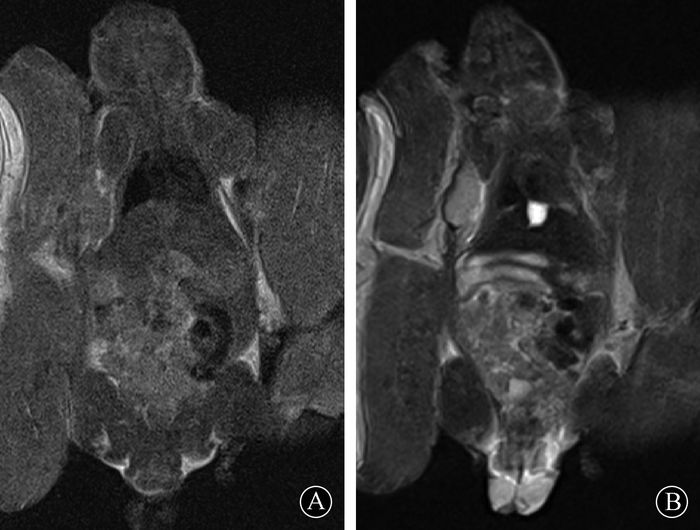
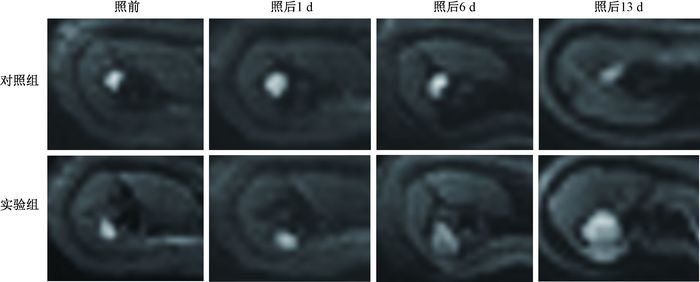
结果1.荷瘤裸鼠模型的核磁共振成像效果:如图 1所示,移植瘤在T1WI序列中呈现为均一低信号,在T2WI序列中呈轻度均一高信号,未见明显液化坏死及出血征象。图 2是移植瘤的DWI成像,从图中可以看出照后随着时间推移,实验组移植瘤的DWI图像高信号强度区域明显小于对照组。
|
图 1 荷瘤裸鼠在常规T1WI(A)、 T2WI(B)序列中的成像表现 Figure 1 Images of the tumor⁃bearing nude mice on conventional T1WI (A) and T2WI (B) sequences |
|
图 2 两组荷瘤裸鼠在照射前后不同时间点的DWI图像变化 Figure 2 DWI maps of the experiment group and the control group at different time points post irradiation |
2.实验组和对照组移植瘤照射前后ADC及ΔADC的比较:从表 1可知,实验组在照后第1天ADC值有所下降,第6、13天时逐渐升高,且ADC13高于ADC0,而对照组ADC值在照后不同时间点呈现逐渐下降的趋势。两组间各时间点ADC值差异有统计学意义(F=6.178、16.181、58.733,P<0.05)。而照射前两组的ADC0差异无统计学意义(P>0.05)。照后第1、6、13天时,两组ΔADC值差异均有统计学意义(F=9.038、12.360、35.140,P<0.05)。
|
|
表 1 实验组和对照组不同时间点的ADC值及ΔADC比较(x±s) Table 1 The difference of ADC values and its change rate between the two groups (x±s) |
为描述不同组别和测量时间点移植瘤的ADC值变化情况,本研究进行了重复测量的方差分析,主体间效应的检验结果提示两个组别之间差异有统计学意义(F=28.189,P<0.001),说明照射对ADC值有影响。
3.实验组与对照组在照射前后移植瘤V和ΔV的比较:重复测量的方差分析显示主体间效应检验结果有差异(F=28.494,P<0.001),提示照射对移植瘤体积有影响。不同时间点两组移植瘤体积和体积变化量比较,照射前两组移植瘤体积V0差异无统计学意义(P=0.393),照后第1至4天时仍无明显差异(P>0.05),从照后第5天开始,两组移植瘤V和ΔV差异有统计学意义(P<0.05),实验组裸鼠移植瘤在照后出现了生长延迟(表 2,3)。
|
|
表 2 照射后不同时间两组移植瘤体积比较(x±s) Table 2 Comparison of xenograft growth between the two groups at different time post-irradiation |
|
|
表 3 照射后不同时间两组移植瘤体积变化率(ΔVX)比较(%,x±s) Table 3 Comparison of xenografts′ change rate (ΔVX) between the two groups at different time post-irradiation (%, x±s) |
4. ADC值大小与移植瘤体积的相关分析:将两组初始ADC值(ADC0)、照后第1天的ADC值(ADC1)与各时间点的肿瘤体积做Pearson相关分析,结果发现对照组ADC0、ADC1与肿瘤体积的后期变化存在相关性,见表 4。从第3天以后,直到第24天,肿瘤体积大小与ADC0存在相关关系,并且从第6天以后,二者之间的r值上升到0.8以上,具有高度的线性相关关系。从第4天以后,直到第24天,肿瘤体积大小与ADC1存在相关关系,并且从第10天以后,二者之间的r值上升到0.8以上,具有高度线性相关关系。提示肿瘤早期ADC值大小与后期移植瘤体积变化存在关联性。
|
|
表 4 ADC值大小与肿瘤体积的相关性分析 Table 4 Correlation analysis of ADC values and xenograft volumes |
讨论
以手术或放疗为主的综合治疗是食管癌的主要治疗模式,选择敏感准确的评估方法、早期预测食管癌放化疗反应对合理治疗方案的制定及调整具有重要价值。在临床上,肿瘤体积测量被广泛用于评价其治疗反应,但食管本身为不规则空腔脏器,常规影像很难测量食管肿瘤体积,且在放化疗早期通过肿瘤体积减小或缩小率来判断是否缓解还缺乏准确性报道。DWI因其特定的成像原理对组织水分子运动情况有着较高的敏感度,细胞分子水平的微观结构变化会影响其量化指标ADC值的大小[7],目前应用DWI预测肿瘤治疗反应的研究在多种系统肿瘤中已有报道,但是结果不尽一致,并且在食管癌领域,开展的相关研究还比较少,因此本研究从动物实验的水平对食管癌移植瘤受照射后ADC值与肿瘤体积的变化规律及二者关系进行了探讨,以期为临床研究和治疗提供参考。
研究发现,接受单次大剂量照射的人食管癌裸鼠移植瘤出现了明显的生长延迟现象,相对应的,照射后食管癌移植瘤的ADC值也呈现出一系列动态变化,并且初期ADC值与后期肿瘤体积存在关联性。从ADC值的变化规律来看,照射前两组ADC值大小并无明显差异,但是在照后第1天,实验组移植瘤的ADC值即较对照组明显降低,且差异有统计意义,在照射后第6和13天,实验组ADC值均明显高于对照组,照射后第1、6、13天的ΔADC也是两组差异明显,分析原因可能是移植瘤组织在放疗早期,由于射线损伤,肿瘤组织细胞膜上的钠钾ATP酶受损、活性下降,细胞膜的通透性发生改变,造成肿瘤细胞水肿,组织细胞间隙变小,使得水分子弥散能力下降,故而ADC值降低[8],另放疗后纤维组织修复也可能是造成ADC值降低的原因之一[9],到后期,由于射线杀伤作用,肿瘤细胞坏死,肿瘤组织内细胞密度降低,水分子运动受限解除,故而ADC值逐渐升高并在肿瘤体积最低值时达到最高值。从移植瘤体积的变化规律来看,两组移植瘤体积初期无差异,射线照射后第1至4天,两组肿瘤均在增长,体积和体积变化率比较均无差异,从第5天开始,两个指标比较出现差异,实验组移植瘤生长明显延迟,照射反应出现形态学变化,分析原因,照射后初期移植瘤体积仍继续增大,一方面可能是由于组织水肿造成的体积增加,另一方面可能是由于单次剂量照射的继发效应,细胞在死亡之前可以进行几次有丝分裂,即代偿性的细胞增殖,到后期时,肿瘤细胞出现凋亡[10],并且由射线直接引起的杀伤作用导致肿瘤细胞死亡,故肿瘤大体形态上表现为体积缩小,但是单次剂量放疗不足以杀死全部肿瘤细胞,之后由于存活的克隆源性细胞的再群体化,导致实验组移植瘤体积缩小后又继续逐渐增大。从两个指标的变化规律对应来看,肿瘤的大体形态学指标(VX、ΔVX)变化相对滞后,而DWI指标(ADC、ΔADC)则能在治疗的极早期提示肿瘤的治疗反应,是一个相对敏感的指标。临床研究方面,郑向东等[11]对18例接受同步放化疗的食管鳞癌患者行DWI动态监测,发现治疗后第1周末病灶的ADC值减低,之后第3周末食管病灶ADC值升高,且明显高于治疗前ADC值,认为MR弥散加权成像对食管鳞癌放化疗的疗效评价具有一定价值,这一结果也在人体食管癌临床治疗层面上与本组研究结果相对应。
此外,国内外学者在不同恶性肿瘤的动物模型中也同样发现了DWI在早期预测放疗反应的应用价值并揭示了可能的机制。Pan等[12]在不同放射敏感性的鼻咽癌移植瘤模型中同样观察到了与本研究结果类似的移植瘤生长曲线及ADC值变化情况。Schraml等[13]观察到晚期肝癌经索拉非尼治疗后ADC值发生的变化,即早期降低,随后增高。Seierstad等[9]发现放疗后3 d,人结直肠癌移植瘤组织的ADC值也出现短暂降低,进一步行组织病理学分析,结果发现此时的瘤体纤维组织百分比与ADC值呈正相关,说明放疗后早期ADC值降低可能与纤维组织修复有关。还有学者将ADC值与患者生存状态或肿瘤组织退缩情况进行了相关分析,提示ADC值预测放化疗反应的可行性。刘辉等[14]观察到食管癌患者放疗后的生存状态与治疗期间的ADC值有显著相关性。而关于放疗前的ADC值是否能作为早期疗效评估的指标这一问题,目前尚无统一定论[15-17],这主要与采用的模型,肿瘤细胞系及应用的治疗手段有关。
综上所述,本组研究结果提示ADC值可在食管癌组织形态发生改变之前较早地发生变化,并且肿瘤早期ADC值大小可能与其后期体积变化存在相关关系,DWI在早期预测食管癌放疗反应方面具有临床应用前景和价值。
利益冲突 无作者贡献声明 聂梦林负责动物实验、数据测量采集、统计分析和论文撰写;王澜负责动物实验指导、数据整理、论文修改;韩春提出研究思路、设计研究方案、指导实验实施并审核论文;许立昂、任雪姣、刘树堂、刘丽虹、田华负责图像处理、协助测量和数据记录
| [1] |
Pircher A, Hilbe W, Heidegger I, et al. Biomarkers in tumor angiogenesis and anti-angiogenic therapy[J]. Int J Mol Sci, 2011, 12(10): 7077-7099. DOI:10.3390/ijms12107077 |
| [2] |
唐利荣, 冯建国. 磁共振扩散加权成像在非小细胞肺癌化疗疗效评估中的应用[J]. 中国现代医生, 2015, 53(6): 84-86. Tang LR, Feng JG. Applicaton of DWI in assesment of clinical efficacy of chemotherapyfor NSCLC[J]. Chin Mod Doctor, 2015, 53(6): 84-86. |
| [3] |
肖琴, 金晶, 叶枫, 等. 弥散加权成像在直肠癌诊断及放化疗疗效预测中的应用[J]. 中华放射肿瘤学杂志, 2013, 22(3): 260-262. Xiao Q, Jin J, Ye F, et al. Application of diffusion-weighted imaging in the diagnosis and the prediction of the radiotherapy and chemotherapy efficacy in rectal cancer[J]. Chin J Radiat Oncol, 2013, 22(3): 260-262. DOI:10.3760/cma.j.issn.1004-4221.2013/03.026 |
| [4] |
盖娟娟, 宋利强, 韩珊. 3.0T磁共振弥散加权成像评价食管癌同步放化疗疗效[J]. 实用临床医药杂志, 2014, 18(7): 154-156. Ge JJ, Song LQ, Han S. 3.0T diffusion weighted imaging in evaluating the efficacy of concurrent chemoraidotherapy in patients with esophageal carcinoma[J]. J Clin Med Pract, 2014, 18(7): 154-156. DOI:10.7619/jcmp.201407055 |
| [5] |
王澜, 韩春, 祝淑钗, 等. 磁共振弥散加权成像在食管癌放疗疗效评价中的应用价值探讨[J]. 中华放射医学与防护杂志, 2014, 34(2): 120-124. Wang L, Han C, Zhu SC, et al. Application of diffusion-weighted magnetic resonance imaging for evaluating the therapeutic effect of esophageal carcinoma[J]. Chin J Radiol Med Prot, 2014, 34(2): 120-124. |
| [6] |
陈伟, 周胜利, 苗重昌, 等. DWI在食管癌同期放化疗早期疗效评价中的初步研究[J]. 中华放射肿瘤学杂志, 2014, 23(4): 312-316. Chen W, Zhou SL, Miao CC, et al. Value of DWI for early assessment of response to concurrent chemoradiotherapy for esophageal cancer:a preliminary study[J]. Chin J Radiat Oncol, 2014, 23(4): 312-316. |
| [7] |
Tsien C, Cao Y, Chenevert T. Clinical applications for diffusion magnetic resonance imaging in radiotherapy[J]. Semin Radiat Oncol, 2014, 24(3): 218-226. DOI:10.1016/j.semradonc.2014.02.004 |
| [8] |
Van der Toorn A, Syková E, Dijkhuizen RM, et al. Dynamic changes in water ADC, energy metabolism, extracelluar space volume, and tortuosity in neonatal rat brain during global ischemia[J]. Magn Reson Med, 1996, 36(1): 52-60. DOI:10.1002/mrm.1910360110 |
| [9] |
Seierstad T, Røe K, Olsen DR. Noninvasive monitoring of radiation-induced treatment response using proton magnetic resonance spectroscopy and diffusion-weighted magnetic resonance imaging in a colorectal tumor model[J]. Radiother Oncol, 2007, 85(2): 187-194. DOI:10.1016/j.radonc.2007.09.009 |
| [10] |
Connell PP, Weichselbaum RR. A downside to apoptosis in cancer therapy?[J]. Nat Med, 2011, 17(7): 780-782. DOI:10.1038/nm0711-780 |
| [11] |
郑向东, 李天然, 吴贵成, 等. 3.0 T MR弥散加权成像对食管癌放化疗的疗效评价[J]. 功能与分子医学影像学杂志(电子版), 2015, 4(1): 579-582. Zheng XD, Li TR, Wu GC, et al. An investigation on evaluating the radio-chemotherapy effect on esophageal cancer using 3 Tdiffusion weighted MRI[J]. Funct Mol Med Imaging(Electronic Ed), 2015, 4(1): 579-582. DOI:10.3969/j.issn.2095-2252.2015.01.005 |
| [12] |
Pan J, Zang L, Zhang Y, et al. Early changes in apparent diffusion coefficients predict radiosensitivity of human nasopharyngeal carcinoma xenografts[J]. Laryngoscope, 2012, 122(4): 839-843. DOI:10.1002/lary.23208 |
| [13] |
Schraml C, Schwenzer NF, Martirosian P, et al. Diffusion-weighted MRI of advanced hepatocellular carcinoma during sorafenib treatment:initial results[J]. AJR Am J Roentgenol, 2009, 193(4): W301-307. DOI:10.2214/AJR.08.2289 |
| [14] |
刘辉, 时高峰, 李如迅, 等. 磁共振扩散加权成像在评估食管癌放射治疗后生存状态中的价值[J]. 世界华人消化杂志, 2014, 22(15): 2145-2149. Liu H, Shi GF, Li RX, et al. Value of MR-DWI imaging in evaluation of living status of patients with esophageal cancer after radiotherapy[J]. WCJD, 2014, 22(15): 2145-2149. DOI:10.11569/wcjd.v22.i15.2145 |
| [15] |
Babsky AM, Ju S, George B, et al. Predicting response to benzamide riboside chemotherapy in hepatocellular carcinoma using apparent diffusion coefficient of water[J]. Anticancer Res, 2011, 31(6): 2045-2051. |
| [16] |
Somoye G, Harry V, Semple S, et al. Early diffusion weighted magnetic resonance imaging can predict survival in women with locally advanced cancer of the cervix treated with combined chemo-radiation[J]. Eur Radiol, 2012, 22(11): 2319-2327. DOI:10.1007/s00330-012-2496-0 |
| [17] |
王欢欢, 何健, 朱丽晶, 等. 磁共振扩散加权成像动态监测中晚期宫颈癌放化疗疗效[J]. 实用放射学杂志, 2015, 31(1): 70-74. Wang HH, He J, Zhu LJ, et al. Dynamical monitoring the therapeutic response of advanced cervical cancer to concurrent chemoradiation with magnetic resonance diffusion weighted imaging[J]. J Pract Radiol, 2015, 31(1): 70-74. DOI:10.3969/j.issn.1002-1671.2015.01.019 |
 2017, Vol. 37
2017, Vol. 37


