2. 350014 福州, 福建医科大学 福建省肿瘤医院教学医院放射诊断科
2. Department of Radiation Oncology, Fujian Tumor Hospital, Fujian Medical University, Fuzhou 350014, China
放射治疗是肺癌等胸部恶性肿瘤的重要治疗手段之一。放射性肺炎(radiation pneumonitis,RP)是放疗常见的不良反应,其发生率为13%~37%[1],一旦发生,往往向肺间质纤维化发展,难以逆转,无特效治疗方法,严重者预后极差,约50%的患者于2个月内死亡[2]。然而,RP向纤维化发展是一个连续的过程,没有明确界线,其临床症状以及肺功能、肺通气或灌注改变并没有明显改变[3],因此,寻找早期诊断或预测RP发生的实验室检测指标,具有重要的临床应用价值。
已有研究发现,血清涎液化糖链抗原(KL-6)水平可以敏感地反映肺泡上皮和肺间质的损伤程度,是间质性肺炎(interstitial pneumonia, IP)的特异性诊断标志物[4-5]。RP作为间质性肺病(interstitial lung disease, ILD)的一种,有关KL-6在RP中的研究甚少,本研究对87例接受胸部放射治疗的Ⅰ ~Ⅲ期肺癌患者临床资料进行严格随访,动态观察其治疗前、治疗后3个月内血清中KL-6、转化生长因子β1(TGF-β1)和乳酸脱氢酶(LDH)改变,结合其临床症状及影像学的改变,探讨KL-6在预测或早期诊断RP中的作用。
资料与方法1.临床资料:选取2016年7月至2017年1月期间在福建省肿瘤医院就诊且接受正规随访的肺癌患者。入组条件:需进行首次肺部放射治疗,未同时或前后进行其他部位(如头部)放射治疗的Ⅰ ~Ⅲ期肺癌患者;KPS评分≥60;重要脏器功能基本正常;预计生存时间>6个月;治疗前有影像学可评价的病灶。排除标准:Ⅳ期广泛转移患者;行全肺切除手术者;有放射治疗史;有肺部纤维化病病史,如严重慢性支气管炎、肺气肿、肺心病、矽肺,FEVl<预计值60%;有其他严重疾病,如6个月内发生过心肌梗死者。按照以上标准,收集患者的姓名、性别、年龄、KPS评分、原发肿瘤大小状态、区域淋巴转移状态(根据国际肺癌研究协会2009年最新国际肺癌分期标准)、组织病理类型、是否并发放射性肺炎等临床资料。共87例接受放射治疗的肺癌患者入组,包括肺腺癌47例、肺鳞癌25例和小细胞肺癌15例。其中,13例被诊断为并发RP,具体临床病理特征见表 1。
|
|
表 1 87例接受放射治疗的肺癌患者的临床特征 Table 1 The clinical features of 87 lung cancer patients after radiotherapy |
2.血清KL-6、TGF-β1和LDH水平检测:经伦理委员会审批,所有患者开始放疗前,放疗后1、14 d,1、2、3个月空腹静脉采血3~4 ml,静置30 min,3 000 r/min,离心半径15 cm,离心5 min,分离血清,-80℃冰箱保存待测。全自动免疫分析仪检测血清KL-6水平,来自日本的171例健康者血清KL-6浓度检测数据显示平均为213 U/ml,但因地区、人种及年龄等差异,尚没有针对中国大陆人群的参考范围;采用上海酶联生物有限公司的人TGF-β1 ELISA检测试剂盒检测血清TGF-β1水平;通过乳酸底物法定量检测血清LDH水平。
3. RP的诊断标准:参照美国肿瘤放射治疗协作组和欧洲肿瘤治疗研究协作组(RTOG/EORTC)诊断分级标准,急性放射性肺炎分以下0~5级:0级,无变化;1级,轻度干咳或劳累时呼吸困难;2级,持续咳嗽需麻醉性止咳药/稍活动即呼吸困难,但休息时无呼吸困难;3级,重度咳嗽,对麻醉性止咳药无效,或休息时呼吸困难/临床或影像有急性放射性肺炎的证据/间断吸氧或可能需类固醇治疗;4级,严重呼吸功能不全/持续吸氧或辅助通气治疗;5级,致命性。
4.治疗经过与随访:入组患者治疗前完成常规病史采集及体格检查、胸部正侧位片、胸部CT等检查,87例患者均采用放化疗为主综合治疗方案,放疗均采用调强放疗(IMRT)。放疗开始前和放疗开始后1、14 d,1、2、3个月检测血清KL-6、TGF-β1和LDH水平;出院患者相应时间进行门诊随访,包括病史询问、体格检查、实验室检查、胸部CT、全身骨扫描、脑MRI等。
5.统计学处理:采用SPSS 13.0软件进行统计分析。计量资料以x±s表示。计量资料的比较经正态性检验符合正态分布,采用独立样本t检验或配对样本t检验;RP发生率的比较采用Pearson χ2检验或Fisher确切概率法;采用多因素Logistic回归分析检验各病理特征及血清KL-6水平改变等与放射性肺炎之间的关系。P<0.05为差异有统计学意义。
结果1.随访及RP发生情况:随访时间截止至放疗开始后6个月,中位随访时间为114 d,全组每例患者在接受放化疗为主的综合治疗方案过程中接受了不同放射剂量的调强放疗后,13例(14.9%)被临床诊断为并发≥2级RP,其中2、3和4级分别为8例(9.2%)、4例(4.6%)和1例(1.1%);5级0例。0~1级RP患者74例,0级52例(59.8%),1级22例(25.3%)。
13例(14.9%)被临床诊断为并发≥2级RP(表 1),其中位诊断时间为97 d(59~121 d),其中,有7例(53.9%)接受了剂量>60 Gy的照射;74例0~1级RP患者中有18例(24.3%)接受了剂量>60 Gy的照射,差异有统计学意义(χ2=4.706,P=0.030,表 1),放射剂量大小与RP发生有关。
2.放疗前后血清KL-6、TGF-β1和LDH水平改变:结果见表 2。13例≥2级RP患者在接受放射治疗后血清KL-6水平逐渐增高,最早于放射治疗后1个月由原来(247±105.44)U/ml升高至(289±104.25)U/ml,较放射治疗前增高,差异具有统计学意义(t=-3.851,P<0.01);于放射治疗后3个月最高水平达(456±202.84)U/ml(t=-5.246,P<0.01);而0~1级RP患者在放射治疗前和放疗后3个月内血清KL-6水平无明显改变。≥2级RP组患者血清TGF-β1于放疗后1个月时均值表现为轻微升高,但与放疗前基础水平差异无统计学意义;LDH在放疗前后均没有明显变化。
|
|
表 2 并发放射性肺炎患者血清KL-6、TGF-β1和LDH水平改变(x±s) Table 2 Changes of serum KL-6, TGF-β1 and LDH in patients with radioactive pneumonia (x±s) |
3.血清KL-6升高与RP的关系:13例发生≥2级RP患者和74例0~1级RP患者在接受放射治疗前,血清KL-6平均水平分别为(247±105.44)U/ml和(209±71.09)U/ml;≥2级RP患者在接受放射治疗前和放疗后的3个月内血清KL-6最高水平达(456±202.84)U/ml,放疗后与放疗前比值达(2.01±1.04)倍;而74例0~1级RP的患者放疗3个月内KL-6最高水平为(222±80.42)U/ml,放疗后与放疗前比值为(1.13±0.60)倍,两组间存在明显差异(t=2.901,P<0.05)。
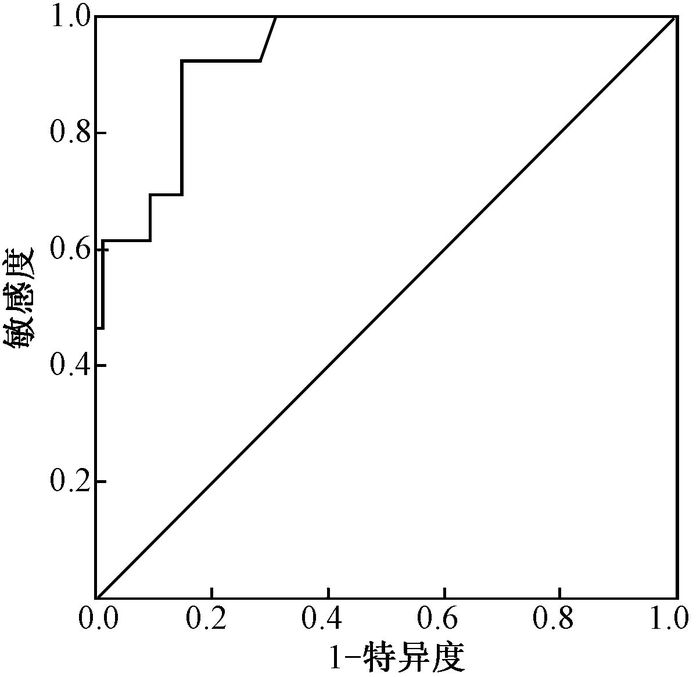
4.血清KL-6升高受试者工作特征曲线(ROC)分析:放疗开始后3个月内血清KL-6水平最高值与放疗前水平比值作ROC曲线,曲线下面积0.933(P=0.000,95%CI 0.875~0.992)。曲线显示,约登指数最大(0.774),诊断界限最佳值为1.435,其灵敏度为92.3%,特异度为85.1%(图 1)。
|
图 1 13例≥2级RP和74例0~1级RP患者血清KL-6放疗前后比值ROC分析 Figure 1 The ROC analysis of the ratio of serum KL-6 before and after radiotherapy in 13 cases ≥ 2 grade RP and 74 cases of grade 0~1 patients |
5.患者治疗后血清KL-6增高与≥2级RP之间的关系:按照血清KL-6比值≥1.435倍或<1.435倍进行二分类,结合年龄、KPS评分、TNM分期、吸烟、手术、放射总剂量等病理特征作为自变量,采用多因素Logistic回归分析,发现血清KL-6增高与≥2级RP的发生具有相关性。KL-6比值≥1.435倍(OR=12.886,95%CI=3.372~49.247;P=0.002,表 3)可作为接受放射治疗的肺癌患者发生≥2级RP的重要预测因素。
|
|
表 3 影响放射性肺炎发生的多因素Logistic回归分析 Table 3 Multivariate logistic regression analysis of RP |
讨论
放疗是肺癌等胸部恶性肿瘤治疗的重要手段之一,而RP是放射性肺损伤中常见且较严重的并发症,严重影响患者的生存质量和预后。寻找简单可行的早期发现RP的血清学监测指标,对指导临床治疗、改善患者的预后具有重要临床意义。本研究对87例接受胸部放射治疗的Ⅰ ~Ⅲ期肺癌患者临床资料进行严格随访,动态观察其治疗前、开始治疗后3个月内血清中KL-6、TGF-β1和LDH改变,结合其临床症状及影像学的改变,探讨KL-6在预测或早期诊断RP中的作用。多因素Logistic回归分析发现血清KL-6比值≥1.435倍与RP的发生存在明显相关,提示血清KL-6比值可能成为肺癌患者发生RP的预测因子。
KL-6是一个高分子量的糖蛋白,表达在各种上皮细胞的表面并且高度表达在再生Ⅱ型肺泡上皮细胞表面[6]。血清中的KL-6已经被证实为各种间质性肺病检测敏感的生物标记物,包括过敏性肺泡炎、风湿相关肺间质病、肺结节病等[7-8]。另外,KL-6是一种肺成纤维细胞潜在的促增殖和抗凋亡物质,影响作用类似于成纤维细胞生长因子及血小板源性生长因子,可能为纤维化增殖的启动因素[9]。KL-6可以促进成纤维细胞产生胶原蛋白Ⅰ、Ⅲ和诱导成纤维细胞分化为肌成纤维细胞,产生α-平滑肌肌动蛋白(α-smooth muscle actin, α-SMA),导致上皮间质转变,并且诱导产生更多的细胞外基质成分,另外KL-6通过抑制成纤维细胞表达肝细胞生长因子(hepatocyte growth factor, HGF),导致细胞外基质过度沉积、重塑,发生肺纤维化表现[10]。
然而,有关KL-6在放射性肺损伤的研究甚少,日本学者发现在6例接受放射治疗后发展RP的肺癌患者体内KL-6水平都明显升高[4];Yamashita等[5]提出,KL-6在放射治疗后升高超过1.5倍的患者发生RP的概率明显升高,并与患者的预后密切相关。本研究结果显示,治疗后血清KL-6增高与RP的发生高度相关,与Yamashita等[5]研究结果一致。本组87例接受放射治疗的肺癌患者中,13例发生≥2级RP患者和74例0~1级RP患者在接受放射治疗前血清KL-6平均水平分别为(247.0±105.44)和(209±71.09)U/ml;前者在接受放射治疗后血清KL-6水平逐渐增高,最高水平达(456±202.84)U/ml,放疗后与放疗前比值达(2.01±1.04)倍;后者放疗3个月内KL-6最高水平为(222±80.42)U/ml,与放疗前比值为(1.13±0.60)倍,两组间存在明显差异。对放疗前后血清KL-6比值进行ROC分析显示:以1.435为临界值,血清KL-6升高诊断≥2级RP的敏感性为0.923%,特异性为0.851%。进一步多因素Logistic回归分析血清KL-6比值≥1.435倍与RP的发生存在明显相关,而本组中13例发生≥2级RP患者的中位诊断时间为97 d(59~121 d),放射治疗开始后1个月内血清KL-6水平即出现增高,3个月内比值≥1.435倍,明显早于RP临床诊断时间,因此认为,血清KL-6比值可能成为肺癌患者发生RP的预测因子。
TGF-β1是一种多功能细胞因子,具有调节细胞生长、抑制免疫活性、调节细胞外基质的功能。Boothe等[11]的研究表明,TGF-β1水平与中度至重度放射性肺损伤的发展相关。Kim等[12]提出放射过程中TGF-β1与RP的发生存在相关性,联合放射生物参数可用来预测RP的发生。本研究结果显示:≥2级RP组患者血清TGF-β1于放疗后1个月时均值表现为轻微升高,但与放疗前基础水平没有统计学差异,这可能与研究的样本量比较少有关,有待加大样本量进一步研究;LDH在放疗前后均没有明显变化。
血清标志物检测及监测具有实际临床意义。有研究表明,许多进展期患者在病情出现进展前首先表现为血清标志物异常,可以提早进行有效地干预,还可以显著减少对影像学检查的依赖,放疗后血清KL-6比值≥1.435倍对RP的发生具有一定的预测价值,同时兼具快速、经济、创伤小、易操作等优点,有望扩大样本量验证后在临床广泛应用。在以后的研究中,将进一步结合化疗方案等因素,扩大样本量,延长实验观察时间,寻找理想的KL-6预测浓度和时间截点,以便更好地服务于临床。
利益冲突 无作者贡献声明 彭伟负责收集资料及论文撰写;陈津协助收集资料及临床样本;魏伟负责提供临床典型案例;崔兆磊、苏光建、陈岩松协助检测及部分论文撰写;陈燕负责提出核心问题及思路,并指导论文写作
| [1] |
Claude L, Pérol D, Ginestet C, et al. A prospective study on radiation pneumonitis following conformal radiation therapy in non-small-cell lung cancer:clinical and dosimetric factors analysis[J]. Radiother Oncol, 2005, 75(1): 120-121. DOI:10.1016/j.randoc.2005.01.002 |
| [2] |
Schild SE, Stella PJ, Geyer SM, et al. The outcome of combined-modality therapy for stage Ⅲ non-small-cell lung cancer in the elderly[J]. J Clin Oncol, 2003, 21(17): 3201-3206. DOI:10.1200/JCO.2003.12.019 |
| [3] |
王绿化, 傅小龙, 陈明, 等. 放射性损伤的诊断及治疗[J]. 中华放射肿瘤学杂志, 2015, 24(1): 4-10. Wang LH, Fu XL, Chen M, et al. Diagnosis and treatment of radioactive injury[J]. Chin J Radiat Oncol, 2015, 24(1): 4-10. DOI:10.3760/cma.j.issn.1004-4221.2015.01.003 |
| [4] |
Oguz EO, Kucuksahin O, Turgay M, et al. Association of serum KL-6 levels with interstitial lung disease in patients with connective tissue disease:a cross-sectional study[J]. Clin Rheumatol, 2016, 35(3): 663-666. DOI:10.1007/s10067-015-3167-8 |
| [5] |
Yamashita H, Kobayashi-Shibata S, Terahara A, et al. Prescreening based on the presence of CT-scan abnormalities and biomarkers(KL-6 and SP-D) may reduce severe radiation pneumonitis after stereetactic radiotherapy[J]. Radiat Oncol, 2010, 5: 32. DOI:10.1186/1748-717X-5-32 |
| [6] |
Huang H, Peng X, Nakajima J. Advances in the study of biomarkers of idiopathic pulmonary fibrosis in Japan[J]. Biosci Trends, 2013, 7(4): 172-177. DOI:10.5582/bst.2013.v7.4.172 |
| [7] |
Miyazaki Y, Tsutsui T, Inase N. Treatment and monitoring of hypersensitivity pneumonitis[J]. Expert Rev Clin Immunol, 2016, 12(9): 953-962. DOI:10.1080/1744666X.2016.1182426 |
| [8] |
Waseda K, Ocho K, Hasegawa K, et al. Increased serum KL-6 levels induced by pulmonary mycobacterium avium complex infection in a patient with RA-associated lung disease[J]. Acta Med Okayama, 2016, 70(3): 217-221. DOI:10.18926/AMO/54422 |
| [9] |
Ohshimo S, Yokoyama A, Hattori N, et al. KL-6, a human MUC1 mucin, promotes proliferation and survival of lung fibroblasts[J]. Biochem Biophys Res Commun, 2005, 338(4): 1845-1852. DOI:10.1016/j.bbrc.2005.10.144 |
| [10] |
Xu L, Yan DR, Zhu SL, et al. KL-6 regulated the expression of HGF, collagen and myofibroblast differentiation[J]. Eur Rev Med Pharmacol Sci, 2013, 17(22): 3073-3077. |
| [11] |
Boothe DL, Coplowitz S, Greenwood E, et al. Transforming growth factor β-1(TGF-β1) is a serum biomarker of radiation induced fibrosis in patients treated with intracavitary accelerated partial breast irradiation:preliminary results of a prospective study[J]. Int J Radiat Oncol Biol Phys, 2013, 87(5): 1030-1036. DOI:10.1016/j.ijrobp.2013.08.045 |
| [12] |
Kim JY, Kim YS, Kim YK, et al. The TGF-beta1 dynamics during radiation therapy and its correlation to symptomatic radiation pneumonitis in lung cancer patients[J]. Radiat Oncol, 2009, 4: 59. DOI:10.1186/1748-717X-4-59 |
 2017, Vol. 37
2017, Vol. 37


