宫颈癌调强放射治疗(intensity-modulated radiation therapy,IMRT)在保证肿瘤靶区得到高剂量照射的同时,减少了膀胱、直肠等正常器官的受照剂量,由此降低了急、慢性并发症的发生率[1]。Pinnacle3计划系统支持脚本编写计划模板和最新的AutoPlan两种方式实现半自动计划,该方式都可以节省计划设计时间,提高计划质量,弥补低年资物理师的经验,对于维持计划一致性和降低危及器官的受量均有一定的优势[2-3]。但不论哪种方式仍然需要物理师在制作模板时根据经验添加危及器官受量的物理或者生物约束条件。Roy等[4]使用四分位距值和条件概率等指标分析研究头颈部肿瘤调强计划结果表明剂量体积约束条件影响计划质量。而物理师制作模板时通常将临床要求设为优化约束参数,或根据以往经验给出,从而进行初始的优化,对于物理师的经验有很强的依赖性,为此,使用四分位距值分析既往优质治疗计划靶区和危及器官受量的剂量体积直方图(DVH)曲线变化情况,以引导自动计划模板参数更加合理的设定。
资料与方法1.一般临床资料:回顾分析山东省肿瘤医院2016年9月至2016年11月收治的22例宫颈癌患者IMRT计划,均采用仰卧位、负压袋固定。
2.计划设计:使用荷兰Philips公司的Pinnacle3 V 9.8计划系统,设计固定野等角度均分调强计划,采用6 MV X射线照射,射野角度为0°、51°、102°、153°、204°、255°和310°,直接子野优化算法(direct machine parameter optimization,DMPO),最小子野面积设为9 cm2,最小子野跳数设为9 MU,最大迭代次数为50。处方剂量为50 Gy,单次剂量2 Gy,共25次,膀胱、直肠临床约束条件为V40 < 40%、左右股骨头V40 < 5%,该22例计划均由MapCheck验证通过并治疗。
3.计划评估:通过编写的Pinnacle脚本程序,将其嵌入到Pinnacle3系统,通过执行该脚本程序可一次性输出某一个计划中靶区和感兴趣危及器官的DVH曲线,每一条DVH曲线存储为一个文本文件,每个计划输出有靶区和危及器官(膀胱、直肠和股骨头)共5组DVH曲线,输出时剂量值每间隔1 cGy进行体积的采样,通过此方法导出所有计划的DVH曲线。设计Matlab自编程软件,实现海量DVH曲线的自动分析,分别批量计算靶区和危及器官平均DVH曲线,同时计算每组DVH曲线某一剂量值的体积四分位距值IQRvol,并将该值描绘成一条连续的曲线,即该器官体积四分位距值曲线[4],代表了感兴趣区接受某一水平剂量照射的体积间的离散度,该值越大说明感兴趣区受到该剂量水平照射的体积差异越大,从而对靶区和正常组织的DVH曲线的差异性进行分析。
其中,IQRvol=Q3Di-Q1Di, Q3Di为某一组DVH曲线剂量为Di的体积值按大小顺序排列,然后将此数列分成4等份,所得第3个四分位上的值,Q1Di是第1个四分位上的值。同时自动计算靶区的均匀性(HI):
4.统计学处理:采用SPSS 17.0软件对膀胱、直肠及左右股骨头的四分位距值分别进行Wilcoxon秩和检验。P < 0.05为差异有统计学意义。
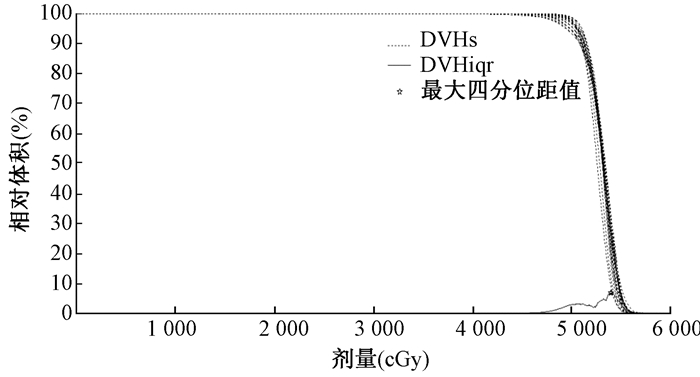
结果1.靶区DVH曲线变化:见图 1。处方剂量50 Gy所达到的靶区的体积为(96.43±1.63)%,靶区受到55 Gy剂量照射的体积为(4.99±2.27)%,计划靶区DVH在54.03 Gy处受照体积差异最大,平均体积为(24.18±6.23)%,四分位距值为6.95%。HI为0.12±0.02,CI为0.74±0.04。
|
图 1 靶区DVH曲线及体积四分位距值曲线 Figure 1 DVH curves and interquartile range (IQR) of volume as a function of dose for PTV |
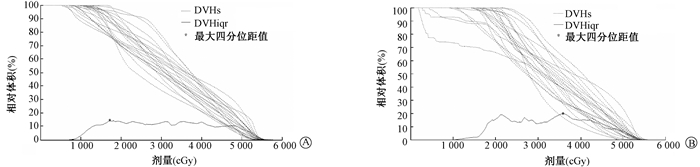
2.膀胱和直肠DVH曲线变化:见图 2。膀胱V40、V30分别为(32.79±7.06)%和(56.47±9.94)%,直肠V40、V30分别为(30.17±10.80)%和(58.16±11.99)%。膀胱DVH在17.24 Gy处受照体积差异最大,平均体积为(86.41±7.58)%,四分位距值为14.62%, 直肠DVH在35.92 Gy处受照体积差异最大,平均体积为(40.63±11.60)%,四分位距值为19.94%。膀胱和直肠体积四分位距值之间差异有统计学意义(t=-6.59,P < 0.05)。
|
图 2 膀胱、直肠DVH曲线及体积四分位距值曲线A.膀胱; B.直肠 Figure 2 DVH curves and interquartile range (IQR) of volume as a function of dose for bladder and rectum A. bladder; B. rectum |
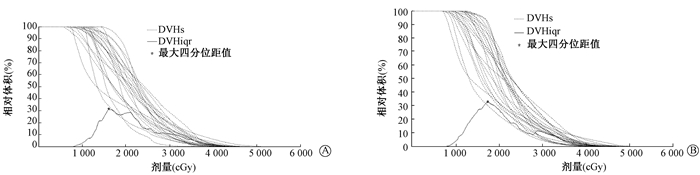
3.左右股骨头DVH曲线变化:见图 3。左股骨头V40、V30分别为(1.19±1.44)%和(13.88±6.73)%,右股骨头V40、V30分别为(1.30±1.51)%和(13.65±6.33)%。左股骨头DVH在16.06 Gy处差异最大,平均体积为(72.19±17.90)%,四分位距值为31.47%,右侧股骨头DVH在17.47 Gy处差异最大,平均体积为(65.84±18.55)%,四分位距值为32.82%,左右股骨头体积四分位距值之间差异无统计学意义(P>0.05)。
|
图 3 左右股骨头曲线及体积四分位距值曲线A.左侧股骨头; B.右侧股骨头 Figure 3 DVH curves and interquartile range (IQR) of volume as a function of dose for femoral heads A. left femoral head; B. right femoral head |
讨论
调强放射治疗通过调节射野内通量强度,相较于三维适形,能够实现更好的靶区覆盖和更低的危及器官受照剂量,减少并发症的发生,IMRT技术在宫颈癌放疗中已得到广泛应用。但调强计划设计优化过程复杂且优化条件人为设定,计划质量依赖于物理师的经验水平,通常需要高年资物理师审核调整[3]。
目前,出现的自动计划能够在保证靶区剂量的同时降低危及器官的受量。Song等[5]在Pinnacle3计划系统中利用脚本设计了直肠癌容积旋转调强(VMAT)计划自动优化的模板,自动计划均能达到临床要求,69%的计划质量得到提升,自动计划中小肠的V30、V40和V50较手动计划有显著较低,其中小肠的V30由26 Gy降低为20 Gy。在较为复杂的头颈部肿瘤中,Hazell等[2]利用Pinnacle的AutoPlan功能模块自动优化头颈部同步加量IMRT计划,利用更少的人工时间达到相似甚至更优的靶区覆盖,腮腺、脊髓和脑干的受量得到显著降低,其中对侧腮腺平均剂量由30.48 Gy降低为26.55 Gy,患侧腮腺平均剂量由35.54 Gy降低为29.73 Gy。实现自动计划的途径主要有基于影像中结构和剂量分布的先验知识和基于模板的自动计划。前者通过分析模型中危及器官和靶区的剂量与空间几何关系,预测危及器官可能的DVH范围,从而生成基于该模型下的最佳优化参数,进行优化,该方法建立模型时需要一定数量的同类型、高质量计划[6]。后者使用基于迭代算法来自动调整优化目标,约束条件和剂量成形轮廓实现临床目标[2-3],模型设立之初也需要对危及器官进行初步的剂量体积限制,该限制既要符合临床规范,也应符合个体化要求,使危及器官受照剂量尽可能低,该功能需要更高版本的软件才能支持。而通过编辑脚本程序能够大部分实现自动计划的功能,不受版本的限制且更加灵活,应用更加广泛,但目前模板的建立缺乏先验知识的引导。
本研究回顾分析了宫颈癌调强放疗中靶区和危及器官的受量情况。结果显示所有计划靶区均能达到临床要求,这也是调强计划设计的优势所在,不管人工计划还是自动/半自动各病种常见计划靶区的剂量分布都能够很好地满足[2]。但靶区受量在54.03 Gy的体积差异最大,要想使靶区受量更加均匀,在设计模板或者优化过程时在该剂量值处可以额外增加优化条件。膀胱直肠临床约束条件一样,但计划设计在达到V40 < 40%的基本要求前提下尽可能低,通常在制作模板时给与相同的初始优化目标函数,但两者由于与靶区空间位置不同,及本身充盈程度不同,应该分别设置剂量优化限值,也可以考虑在优化进程中动态调节两者的剂量体积限值和权重,再者,膀胱直肠不同的初始优化限值可以通过大量优质计划DVH曲线的回顾分析方法获得。本研究结果显示膀胱直肠在20~50 Gy剂量受照的体积差异较大,这也与基于先验知识引导的自动计划中对危及器官给出预测范围有相似之处,基于此,建议在优化时使用全局的变量来优化或者加大全局变量的权重,比如使用正常组织并发症概率(NTCP)、等效均匀剂量(EUD)等[7-11]作为高权重优化参数来整体压低危及器官的受照剂量,避免完全使用单一的剂量体积优化条件,以免计划得不到最佳的优化,使用一系列剂量体积指标优化时,权重的大小可以参考以往优质计划的体积四分位距值的分布情况,某一剂量值处体积四分位距值越大,相应的优化权重设置应越小。再者,可以通过回顾分析上述病例,建立膀胱、直肠的平均剂量,V40、V30与靶区重叠体积或者各体素到靶区表面的距离之间的相关性分析[12-14],预测膀胱、直肠的剂量,特别是EUD的预测,来制定个体化的模板,这也是下一步的研究方向。左右股骨头受量基本一致,宫颈癌调强计划优化模板中可以统一设置初始约束条件。
总之,通过使用四分位距值来回顾分析调强计划的DVH曲线,可以直观体现曲线的差异,评价计划的一致性,优化权重可以根据该值的变化趋势进行设置,指导自动计划模板的建立。
利益冲突 本研究由署名作者按以下贡献声明独立开展,未接受有关公司的任何赞助,不涉及各相关方的利益冲突作者贡献声明 李成强负责构思、采集数据、论文撰写;卢洁、朱健、尹勇设计实验、指导论文的撰写和修改;陶城负责对结果进行统计和分析;段敬豪负责采集数据、临床资料分析
| [1] | Marnitz S, Wlodarczyk W, Neumann O, et al. Which technique for radiation is most beneficial for patients with locally advanced cervical cancer? Intensity modulated proton therapy versus intensity modulated photon treatment, helical tomotherapy and volumetric arc therapy for primary radiation-an intraindividual comparison[J]. Radiat Oncol, 2015, 10 (1): 91 DOI:10.1186/s13014-015-0402-z. |
| [2] | Hazell I, Bzdusek K, Kumar P, et al. Automatic planning of head and neck treatment plans[J]. J Appl Clin Med Phys, 2016, 17 (1): 272-282. DOI:10.1120/jacmp.v17i1.5901. |
| [3] | Sharfo AW, Voet PW, Breedveld S, et al. Comparison of VMAT and IMRT strategies for cervical cancer patients using automated planning[J]. Radiother Oncol, 2015, 114 (3): 395-401. DOI:10.1016/j.radonc.2015.02.006. |
| [4] | Roy A, Das IJ, Nohadani O. On correlations in IMRT planning aims[J]. J Appl Clin Med Phys, 2016, 17 (6): 44-59. DOI:10.1120/jacmp.v17i6.6411. |
| [5] | Song Y, Wang Q, Jiang X, et al. Fully automatic volumetric modulated arc therapy plan generation for rectal cancer[J]. Radiother Oncol, 2016, 119 (3): 531-536. DOI:10.1016/j.radonc.2016.04.010. |
| [6] | Wu B, Kusters M, Kunze-Busch M, et al. Cross-institutional knowledge-based planning (KBP) implementation and its performance comparison to Auto-Planning Engine (APE)[J]. Radiother Oncol, 2017, 123 (1): 57-62. DOI:10.1016/j.radonc.2017.01.012. |
| [7] | Puzhakkal N, Kallikuzhiyil Kochunny A, Manthala Padannayil N, et al. Comparison of treatment plans:a retrospective study by the method of radiobiological evaluation[J]. Pol J Med Phys Eng, 2016, 22 (3): 61-68. DOI:10.1515/pjmpe-2016-0011. |
| [8] | Hardcastle N, Tomé WA, Foo K, et al. Comparison of prostate IMRT and VMAT biologically optimised treatment plans[J]. Med Dosim, 2011, 36 (3): 292-298. DOI:10.1016/j.meddos.2010.06.001. |
| [9] | Qi XS, Semenenko VA, Li XA. Improved critical structure sparing with biologically based IMRT optimization[J]. Med Phys, 2009, 36 (5): 1790-1799. DOI:10.1118/1.3116775. |
| [10] | Thomas E, Chapet O, Kessler ML, et al. Benefit of using biologic parameters (EUD and NTCP) in IMRT optimization for treatment of intrahepatic tumors[J]. Int J Radiat Oncol Biol Phys, 2005, 62 (2): 571-578. DOI:10.1016/j.ijrobp.2005.02.033. |
| [11] | Kierkels RG, Korevaar EW, Steenbakkers RJ, et al. Direct use of multivariable normal tissue complication probability models in treatment plan optimisation for individualised head and neck cancer radiotherapy produces clinically acceptable treatment plans[J]. Radiother Oncol, 2014, 112 (3): 430-436. DOI:10.1016/j.radonc.2014.08.020. |
| [12] |
王强, 李光俊, 宋莹, 等. 宫颈癌VMAT计划中OAR的DVH预测价值[J].
中华放射肿瘤学杂志, 2016, 25 (8): 839-842. Wang Q, Li GJ, Song Y, et al. Predictive value of dose-volume histograms of organs at risk in volumetric modulated arc therapy plans for cervical cancer[J]. Chin J Radiat Oncol, 2016, 25 (8): 839-842. DOI:10.3760/cma.j.issn.1004-4221.2016.08.010. |
| [13] |
黄伯天, 朱金汉, 杨鑫, 等. 鼻咽癌IMRT计划腮腺剂量预测模型建立与验证[J].
中华放射肿瘤学杂志, 2016, 25 (2): 150-154. Huang BT, Zhu JH, Yan X, et al. Development and evaluation of a predicting model of dose volume histograms of parotid in NPC IMRT planning[J]. Chin J Radiat Oncol, 2016, 25 (2): 150-154. DOI:10.3760/cma.j.issn.1004-4221.2016.02.014. |
| [14] | Njeh CF, Parker BC, Orton CG. Evaluation of treatment plans using target and normal tissue DVHs is no longer appropriate[J]. Med Phys, 2015, 42 (5): 2099-2102. DOI:10.1118/1.4903902. |
 2017, Vol. 37
2017, Vol. 37


