对于不能手术或不愿手术的原发性肝癌(hepatocellular carcinoma,HCC)患者,放射治疗已成为日益重要的一种治疗方式[1]。随着精确放疗技术的发展,肝动脉化疗栓塞术(transcatheter arterial chemoembolization,TACE)结合三维适形放疗(3D-CRT)在治疗HCC中取得了令人鼓舞的临床效果[2]。但肝脏随呼吸运动位移及变形较明显,靶区准确定位较为困难,同时也严重影响靶区和正常肝脏受量的准确评估[3]。近年来应用4D-CT及形变配准技术可准确获得肿瘤随呼吸运动的变化信息,便于靶区准确定位和剂量累加,进而更准确地评估患者的真实受量[4]。目前,传统3D治疗计划因未考虑呼吸运动的影响,在评估靶区和正常肝脏的实际受照剂量时存在较大误差。本研究应用4D-CT与形变配准技术,探讨呼吸运动在HCC放疗中对靶区及正常肝脏真实受量的影响。
1. 病例选择:选取19例经TACE治疗的HCC患者,所有患者病灶区碘油沉积良好,KPS评分≥80。其中,男性13例,女性6例,中位年龄61.5岁(43~72岁)。肿瘤位于肝左叶8例,肝右叶11例。该研究经山东省肿瘤医院伦理委员会讨论批准,患者均签订知情同意书。
1. 病例选择:选取19例经TACE治疗的HCC患者,所有患者病灶区碘油沉积良好,KPS评分≥80。其中,男性13例,女性6例,中位年龄61.5岁(43~72岁)。肿瘤位于肝左叶8例,肝右叶11例。该研究经山东省肿瘤医院伦理委员会讨论批准,患者均签订知情同意书。
2. 模拟定位:所有患者均在荷兰Philips Brilliance大孔径CT模拟定位机进行模拟定位,并辅以美国Varian呼吸控制管理系统进行呼吸监测。患者仰卧位,负压袋固定,头先进,双手上举,依次进行自由呼吸下3D-和4D-CT平扫。4D-CT依据呼吸周期均分为10个时相,定义CT00为吸气末(EI)时相,CT50为呼气末(EE)时相,呼吸周期的分割模式如图 1所示。将所获得的CT图像传至RayStation v3.99.0.7(RaySearch Laboratories,瑞典)治疗计划系统勾画靶区及正常器官,设计治疗计划。
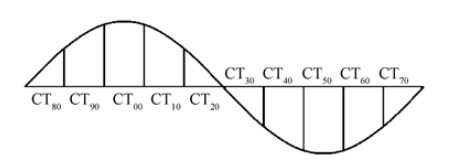 | 注:CT00为吸气末时相,CT50为呼气末时相,其余为呼吸中间状态图 1 4D-CT呼吸周期的分割模式示意图 |
3. 靶区、危及器官的定义及勾画:在所有CT图像中分别勾画大体肿瘤靶区(GTV)及肝脏。为保证勾画的重复性及准确性,所有GTV及肝脏均由同一放疗医师在相同窗宽窗位条件下勾画(W/L 350/50)。GTV定义为肿瘤区碘油沉积范围,将10个呼吸时相的GTV融合形成个体化内靶区(IGTV),计划靶区(PTV)由IGTV在各个方向边界外扩0.8 cm得到[5]。正常肝脏定义为全肝减去GTV的体积,计划评估时仅评价正常肝脏的受照剂量及体积。
4. 放疗计划设计:基于3D-CT图像制定3D适形放疗计划,采用15 MV X射线,4~5野照射,处方剂量50 Gy,常规分割。剂量参考点定义为靶区的几何中心点,100%的等剂量线覆盖≥98% PTV。正常肝脏的平均剂量<28 Gy;胃和十二指肠的最大剂量<45 Gy,并且5 cm3体积接受的剂量<25 Gy;脊髓的最大点剂量<50 Gy[6]。
5. 形变配准:本研究采用基于有限元模型的多器官形变配准(MORFEUS)算法对剂量进行形变。将3D计划中的剂量(Dose-3D)在4D-CT的10个时相中重新计算,得到各时相的剂量,其中EI和EE时相剂量分别定义为Dose-EI和Dose-EE。以EE时相作为参考图像,其余9个时相的图像作为目标图像进行形变配准,配准过程中以体表轮廓和肝脏为限定区域,将9个时相的剂量形变到EE时相并进行剂量累加得到4D剂量(Dose-4D)。对于这种算法的精度,通过比较吸气末与呼气末肝内散在的血管分支在配准前后的位移进行验证,肝脏形变的精度在左右、前后和头脚方向均小于0.2 cm[7]。
6. 评价指标:PTV的D99、D95和D1分别代表 99%、95%和1%的PTV体积的受照剂量。适形指数(CI)定义为CI=TVRI/TV×TVRI/VRI。其中,TVRI代表处方剂量线包绕的PTV体积,TV代表PTV体积,VRI代表处方剂量线包绕的所有体积;CI越接近于1,适形性越好。均匀指数(HI)定义为HI=(D2-D98)/处方剂量,HI越接近于0,均匀性越好。评价正常肝脏的平均剂量(Dmean)、V5、V10、V20、V30和V40(Vx代表正常肝脏接受≥x Gy剂量的体积与正常肝脏体积的百分比)。
7.统计学处理:数据用x±s形式表示。采用SPSS 17.0软件对靶区和正常肝脏的Dose-3D、Dose-EI、Dose-EE及Dose-4D间的剂量学指标进行比较。其中,多组数据比较采用Friedman检验,两组比较采用配对Wilcoxon检验。P<0.05表示差异有统计学意义。
1. GTV和肝脏的体积及移动度:在3D-CT图像中所勾画的GTV体积为(56.35±69.37) cm3,肝脏体积为(1 540.93±316.21) cm3;4D-CT各时相的GTV及肝脏体积为(54.74±68.51) cm3及[JP](1 541.51±301.04) cm3,与3D-CT中的体积差异无统计学意义(P>0.05)。由4D-CT的10个时相GTV融合而成的IGTV体积为(88.28±133.55) cm3。GTV及肝脏的移动度分别为(0.60±0.51)cm及(0.49±0.31)cm。
2. 形变配准评估:由膈肌、肾脏、脾脏、肝脏及肝脏内沉积的碘油颗粒的位置可以看出,如图 2所示,形变配准前肝脏及其肿瘤靶区的位置在吸气末、呼气末图像上差异较大,配准后上述器官及结构均能较好融合在一起。
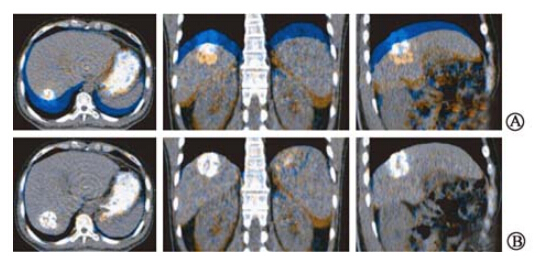 | 注:由左向右依次为横断位、冠状位和矢状位;蓝色代表呼气末肝脏位置,橘红色代表吸气末肝脏位置图 2 吸气末与呼气末时相形变配准前后的融合图像A. 形变配准前; B. 形变配准后 |
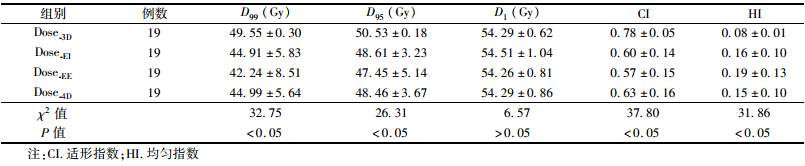
3. 剂量学指标比较:PTV剂量学指标列于表 1,对于D99和D95,Dose-3D均较Dose-EI、Dose-EE及Dose-4D增高,而CI和HI则优于三种剂量分布(χ2=32.75、26.31、37.80、31.86,P<0.05)。上述指标在Dose-4D与Dose-EI、Dose-EE间的差异无统计学意义(P>0.05);在Dose-EI与Dose-EE间的差异亦无统计学意义(P>0.05)。正常肝脏的剂量学指标Dmean、V5、V10、V20、V30和V40在Dose-3D、Dose-EI、Dose-EE及Dose-4D间差异无统计学意义(P>0.05)。
| 表 1 不同剂量分布下PTV剂量-体积指标比较(x±s) |
3D-CRT作为一种HCC的非手术疗法,已取得了令人鼓舞的临床疗效[8]。但肝脏受呼吸运动影响明显,在放疗过程中靶区易发生明显运动与变形,使HCC靶区 准确定位有一定难度。因此,不仅限制肿瘤区的剂量提升,导致正常肝脏受照体积增大,而且增加放射性肝损伤的发生率[9]。由于未考虑呼吸运动的影响,传统基于自由呼吸状态下3D-CT图像进行靶区勾画及治疗计划,设计所得的剂量-体积指标可能并未真实反映肿瘤区及正常肝脏所受剂量。
近年来4D-CT技术的发展,使评价HCC在放疗过程中随呼吸运动的变化成为可能。4D-CT通过呼吸运动管理装置记录患者的呼吸曲线,并依据呼吸周期对容积图像进行分割,获得与时间相关联的动态CT图像,可较准确地反映靶区及正常肝脏的位置及体积等信息[10]。研究显示,与常规3D-CRT相比,应用4D-CT技术可缩小靶区,在保证控制肿瘤的同时,减少正常肝脏的受照剂量及体积[11]。基于4D-CT技术,将3D计划的剂量在各分割时相图像中重新计算,并通过形变配准技术进行剂量累加,可较客观地反映HCC靶区及正常肝脏的剂量-体积关系,从而指导临床正确评估放射性肝损伤的发生。
形变配准技术通过找到两幅图像间点对点的像素一致性,不断优化空间变换参数以达到解剖特征的满意匹配[12]。本研究采用MORFEUS形变配准算法,它与基于灰度的配准技术不同,能够模仿多个器官间的表面界面,因此,只要器官的边界标志恒定,即使针对不同的影像模式也能实现多个器官间的配准。Brock等[7]已对形变配准后的结果进行了定量评估,且所有接受放疗的患者都首先经过TACE治疗,肿瘤区沉积的碘油密度高且界限清,可成为评估形变配准算法准确性的标记。形变后无论在碘油沉积区还是肝脏,都取得了良好的一致性。
本研究将4D-CT与形变配准技术相结合进行剂量累加,通过比较发现PTV中Dose-4D较处方剂量平均可以提升5.42%,而Dose-EI与Dose-EE较处方剂量平均降低4.45%和6.41%。虽然Dose-4D与Dose-EI、Dose-EE的差异并无统计学意义,但不一定表明4D-CT任一时相剂量可代表靶区的真实受量。如果能够入组呼吸动度较大的病例,或许可看到Dose-4D与4D-CT各时相剂量间的明显差异。由于呼吸运动的影响,正常肝脏不同剂量分布下的剂量-体积指标间虽有一定程度的波动,但差异并无统计学意义。正常肝脏Dose-3D与Dose-4D接近可考虑两方面原因:一是肿瘤/肝脏体积比的影响,较小的肿瘤相对于体积较大的肝脏产生的影响不明显;二是剂量计算时未引入各时相的贡献权重,剂量是在等权重的基础上累加的。
利用4D-CT与形变配准技术进行剂量累加的方法曾在多项研究中应用。Velec等[13] 通过形变呼气CT到吸气CT进行中期呼吸运动插值模拟,剂量累加后表明肿瘤最小剂量波动于-14%~8%,正常肝脏的平均剂量波动于-3%~4%。但模拟的呼吸运动并不能反映患者真正的呼吸运动,因此,最终累加的剂量也存在不确定性。Jung等[14]在4D-CT的呼气末时相设计3D计划,经4D剂量累加后表明GTV的剂量学参数无明显改变,而肝脏的Dmean和通用等效剂量(gEUD)分别增加了3.1%和2.8%。此研究虽累加了4D-CT的10个时相剂量,但3D剂量是基于EE时相CT图像计算的,与临床上大多数情况下基于自由呼吸CT图像进行3D治疗计划设计并不相符。虽然以上的研究中存在不足之处,但结果均表明在肝癌放疗中想要提升肿瘤区剂量必须充分考虑肝脏受量的个体化允许范围。因此,引入个体化呼吸追踪技术,可更客观科学地进行靶区和危及器官的受量评估。
综上所述,利用4D-CT及形变配准技术进行剂量计算,可更合理评估自由呼吸下PTV及正常肝脏的治疗剂量,有利于靶区剂量的安全提升。
| [1] | Feng M, Ben-Josef E. Radiation therapy for hepatocellular carcinoma[J]. Semin Radiat Oncol, 2011, 21(4): 271-277. |
| [2] | Zhou ZH, Liu LM, Chen WW, et al. Combined therapy of transcatheter arterial chemoembolisation and three-dimensional conformal radiotherapy for hepatocellular carcinoma[J]. Br J Radiol, 2007, 80(951): 194-201. |
| [3] | 习勉, 刘孟忠, 李巧巧, 等. 基于4D-CT的腹部器官呼吸运动分析[J]. 癌症, 2009, 28(9): 989-993. |
| [4] | Admiraal MA, Schuring D, Hurkmans CW. Dose calculations accounting for breathing motion in stereotactic lung radiotherapy based on 4D-CT and the internal target volume[J]. Radiother Oncol, 2008, 86(1): 55-60. |
| [5] | Zhao JD, Xu ZY, Zhu J, et al. Application of active breathing control in 3-dimensional conformal radiation therapy for hepatocellular carcinoma: the feasibility and benefit[J]. Radiother Oncol, 2008, 87(3): 439-444. |
| [6] | Marks LB, Yorke ED, Jackson A, et al. Use of normal tissue complication probability models in the clinic[J]. Int J Radiat Oncol Biol Phys, 2010, 76(3 Suppl): S10-19. |
| [7] | Brock KK, Sharpe MB, Dawson LA, et al. Accuracy of finite element model-based multi-organ deformable image registration[J]. Med Phys, 2005, 32(6): 1647-1659. |
| [8] | Merle P, Mornex F, Trepo C. Innovative therapy for hepatocellular carcinoma: three-dimensional high-dose photon radiotherapy[J]. Cancer Lett, 2009, 286(1): 129-133. |
| [9] | Rosu M, Dawson LA, Balter JM, et al. Alterations in normal liver doses due to organ motion[J]. Int J Radiat Oncol Biol Phys, 2003, 57(5): 1472-1479. |
| [10] | 邢军, 李建彬, 张英杰, 等. 四维CT中三种方法勾画原发性肝癌内大体靶体积的比较研究[J]. 中华放射肿瘤学杂志, 2012, 34(2): 122-128. |
| [11] | 巩贯忠, 尹勇, 刘同海, 等. RapidArc进行肝癌放疗时不同靶区确定方法的剂量学比较[J]. 中华放射医学与防护杂志, 2012, 32(3): 289-293. |
| [12] | 申艳平. 医学图像配准技术[J]. 中国医学物理学杂志, 2013, 30(1): 3885-3889. |
| [13] | Velec M, Moseley JL, Eccles CL, et al. Effect of breathing motion on radiotherapy dose accumulation in the abdomen using deformable registration[J]. Int J Radiat Oncol Biol Phys, 2011, 80(1): 265-272. |
| [14] | Jung SH, Yoon SM, Park SH, et al. Four-dimensional dose evaluation using deformable image registration in radiotherapy for liver cancer[J]. Med Phys, 2013, 40(1): 011706. |
 2015, Vol. 35
2015, Vol. 35