心血管介入操作可能使患者和医护人员接受较高的辐射剂量、造成潜在的辐射损伤[1],即使使用目前认为合适的防护措施,射线辐射仍会损伤机体。随着复杂性心律失常导管消融、尤其是房颤(atrial fibrillation,AF)导管消融的广泛开展,从事心律失常的介入治疗工作者和接受治疗的患者将面临更多剂量的辐射[2],故减少辐射剂量意义重大。磁导航(magnetic navigation system,MNS)是通过改变磁场方向而操纵消融导管进行手术的一种新设备,目前国外已越来越多的应用于AF等复杂性心律失常的导管消融治疗,初步研究认为,该设备应用于指导AF导管消融可减少术中患者的辐射剂量,但目前国内外缺乏单一对比MNS指导下AF导管消融与手动消融辐射剂量、尤其是医护人员辐射剂量的研究,故本研究将对此进行分析,探讨MNS在放射防护方面的应用价值。
1. 病例选择及手术方式:2012年10月至2014年4月南京医科大学附属无锡市人民医院心内科连续收住入院的94例行AF导管消融术患者,年龄(47.57±12.32)岁(19~73岁),其中男性60例,女性34例,AF发生时间(5.33±9.27)年(2个月~22年),前60例为手动消融组(CON组),后34例为MNS指导下导管消融组(MNS组)。符合下列条件之一为入选标准:1至少每周发作1次的阵发性房颤;2至少每月发作1次有症状的持续性房颤;3至少1种抗心律失常药物无效;4应用1种以上抗心律失常药物才能控制症状;5持久性房颤;6有1项以上血栓形成的危险因素。符合下列条件之一为排除标准:1年龄<18岁或>75岁;2临床心功能IV级;3左心室射血分数<35%;4左心房(左房)内径>60 mm,有抗凝禁忌证;5左房或左心耳有血栓形成;6合并肾功能不全、阻塞性或弥散性肺功能障碍。术中均进行双侧肺静脉造影,采用环肺静脉电隔离术式对AF进行导管消融治疗。持续性和永久性AF患者,行左房顶部和(或)二尖瓣峡部线性消融。所有患者消融前均签署知情同意书。两组患者均在同一导管室、相同数字减影血管造影机进行手术,手术医师、助手、护士均不变(同一电生理手术组)。
2.介入数字减影血管造影和患者辐射剂量监测方法:采用德国Siemens公司生产的zee biplane Angio型平板探测器数字减影血管造影机,运用自动曝光条件采集图像。对所有操作均使用悬吊式屏风、床旁铅屏防护,平板探测影像系统具有内置穿透电离室型的随机配置剂量测量系统,其数据记录包括:面积剂量乘积(DAP)、在线随机的参考点累积皮肤表面入射剂量(CD)、透视时间、最高皮肤剂量(PSD)、摄影帧数以及管电压、管电流等参数。其中管电压为60~80 kV,管电流在透视时为20~40 mA,摄影时为200~800 mA,上述参数系统根据患者体重等个体情况自动调整。采样速率在透视时为7.5帧/s,摄影时为15帧/s,投照角度在摄影时取左前斜45°和右前斜45°(摄影均用于双侧肺静脉造影),透视时为前后位(根据手术需要可能偶尔需要其他角度透视),焦片距均为90 cm。接受导管消融治疗的患者所受的辐射剂量,可以通过DSA设备的检测装置实现在线监测而得到DAP值和CD值。DAP是X射线束的横截面积乘以该照射野上的平均空气比释动能。在介入参考点位置的X射线束横截面积一定时,DAP值是累积剂量与其照射野面积的乘积。CD值是参考点累积皮肤表面入射剂量。MNS组按时间顺序将患者分为前后各17例,比较操作熟练程度对辐射剂量的影响。
3. 医护人员单次手术辐射剂量监测:每名医护人员于左侧胸前防护服外佩戴徽章式LiF(Mg,Cu,P)热释光个人剂量计,每人2枚,MNS指导下AF导管消融时佩戴一枚,手动消融时佩戴另一枚,辐射剂量检测应用RGD-2A型热释光剂量仪进行,检测时扣除本底的影响。医护人员透视时间由专人在控制室内以秒表记录。
4. 统计学处理:计量资料以x±s表示,采用SPSS 16.0软件进行分析,如两组数据为正态分布且方差齐,则采用成组t检验,如两组数据为非正态分布或方差不齐则采用Mann-Whitney U检验,两组间率的比较用χ2检验。P<0.05为差异有统计学意义。
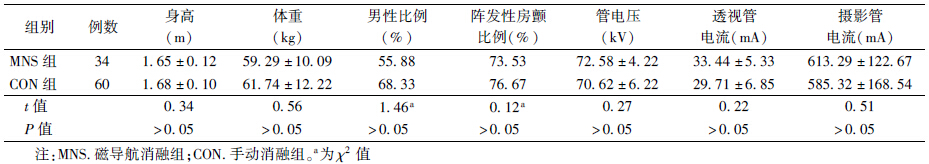
1. MNS组和CON组患者一般情况和放射影像条件对比:两组患者身高、体重、管电压、透视管电流、摄影管电流及性别比例、阵发性房颤比例差异均无统计学意义,见表 1。
| 表 1 MNS组和CON组患者一般情况和放射影像条件对比(x±s) |
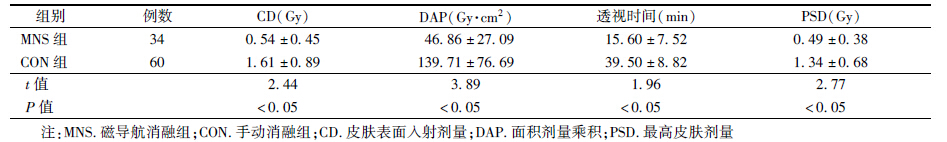
2. MNS组和CON组患者辐射剂量与透视时间比较:MNS组患者CD值、DAP值、透视时间、PSD值明显低于CON组(t=2.44、3.89、1.96、2.77,P<0.05,表 2)。
| 表 2 MNS组和CON组患者辐射剂量和透视时间比较(x±s) |
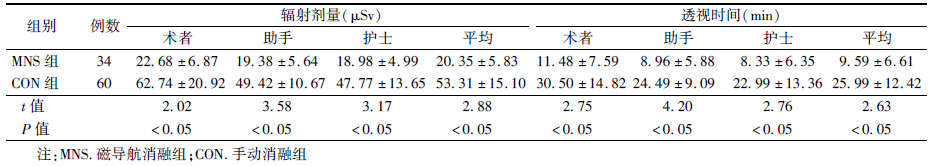
3. 参与手术的医护人员辐射剂量与透视时间比较:MNS指导手术时,医护人员辐射剂量和透视时间明显低于手动消融时(t=2.02、3.58、3.17、2.88,2.75、4.20、2.76、2.63,P<0.05,表 3)。
| 表 3 MNS组和CON组医护人员透视时间和辐射剂量比较(x±s) |
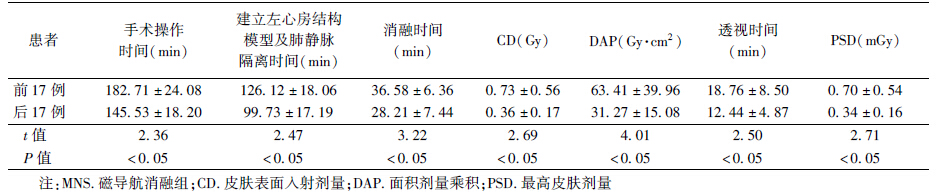
4. 操作熟练程度对MNS组手术时间、辐射剂量与透视时间的影响:前17例患者平均CD值、DAP值、PSD值明显高于后17例患者(t=2.69、4.01、2.71,P<0.05),平均手术操作时间、建立左心房结构模型及肺静脉隔离时间、消融时间和透视时间明显长于后17例患者(t=2.36、2.47、3.22、2.50,P<0.05,表 4)。
| 表 4 MNS组患者前、后17例CD、DAP、PSD和透视以及手术时间比较(x±s) |
AF的导管消融已成为反复发作且药物治疗无效和(或)疗效不佳的阵发性AF的一线治疗方法[3]。但对于该类复杂性心律失常的导管消融治疗,常需要多角度投照、手术步骤多、操作时间长,导致从事该诊疗的介入放射工作人员和接受治疗的患者不可避免地受到相当程度的辐射照射,严重影响了AF导管消融的广泛开展。
除常规透视下置管建立手术入路的操作外,AF手动导管消融辐射剂量大的主要原因有:1消融术前需要在透视指导下建立左心房结构模型;2为准确观察肺静脉口的解剖位置和结构,需要进行左右双侧肺静脉造影;3AF导管消融目前的主流术式为环肺静脉电隔离术,需要进行连续多点消融组成环状隔离线以阻隔肺静脉电位,在此过程中导管也需要不断的在透视下调整位置;4对于持续性或永久性AF可能需要加做房顶线或二尖瓣峡部线性消融等额外操作,仍需要透视指导;5手术结束之前,还需要验证双侧肺静脉是否完全隔离,再次需要透视指导。另外,AF手动消融学习曲线较长,增加了早期辐射剂量。因此,采取有效的防护措施以降低患者和医护人员的辐射剂量,是技术层面研发的热点。
MNS是近几年来用于AF导管消融的新设备,该设备主要由两块磁铁、磁消融导管和导管推送器3部分组成[4],其中两块磁铁位于患者手术台的两侧,当患者平卧于手术台时,患者心脏已置于左右两块磁铁所产生的0.08~0.10 T的磁场中,两块磁铁的作用是通过改变磁场方向而改变磁消融导管前后和左右的运动方向,而磁场的方向可通过在手术间外的控制室内操作计算机软件进行,不需要在手术台旁进行手动操作导管,故MNS为减少患者和医护人员的辐射剂量提供了切实可行的操作基础。既往多篇国外文献报道,与手动消融相比,MNS指导下AF导管消融在手术成功率相似的前提下,具有减少术中患者辐射剂量和(或)透视时间以及降低患者手术并发症等优点[5, 6, 7, 8],但没有系统的在放射及防护角度对其进行全面对比,其手术人员和所用手术方式、方法不一,参数较为单一,对照条件参差不齐,且没有对医护人员的辐射剂量进行对比。本研究利用PSD、CD、DAP等多个常用指标[9],在相同手术操作间、相同数字减影血管造影设备、相同监测方法、相同医护人员操作相同术式的基础上,对患者和医护人员的放射暴露情况同时对比,排除了混杂因素,发现CON组患者平均CD值、PSD值均大于1 Gy,透视时间较长,存在高剂量的风险,而MNS组上述指标仅相当于CON组的1/3左右。对于医护人员的测量也得到相似结果,无论是手术医师、助手还是护士,辐射剂量和透视时间明显减少,显示了MNS在放射防护方面的应用价值。
分析MNS在AF射频中明显减少辐射剂量和透视时间的原因,有如下几点:首先,建立左心房结构模型时不需要反复在透视下调整导管位置,只需要在操作间内根据已有的左心房X射线片和肺静脉造影结果为基础,利用磁场引导导管建立左心房结构模型;其次,在建立左心房模型后,MNS附带软件可将电脑三维模拟的左心房结构及导管位置与实时二维X射线片整合,之后的透视显像仅需要数次持续1~2 s的透视显像即可满足手术需求;再次,因MNS导管柔软,可随意弯曲,环状线性消融时,不需要在透视下手动调整导管位置,在磁场引导下导管可到达心腔内任意指定位置;最后,MNS附带软件可自动引导导管验证是否实现肺静脉电位的隔离,进一步减少辐射剂量。
另外,对比前、后17例患者手术总时间、建立左心房结构模型及肺静脉隔离时间、消融时间、辐射剂量和透视时间,发现后17例患者明显少于前17例,说明MNS指导下AF导管消融学习曲线短,可以很快由透视指导下手动操作导管进行消融的手术模式转换为MNS指导下磁场引导导管进行消融的手术模式,这得益于MNS安全性高、无需有长期导管操作经验,同时明显减少了早期学习阶段的辐射剂量。
MNS技术在国外已较为广泛的应用于AF的导管消融治疗,但国内尚属于早期应用,目前本中心该类手术例数虽在国内第一,但样本量仍较少,且局限于心房颤动的导管消融治疗,还需以后加大样本量并向其他类型的复杂型心律失常推广应用,进行进一步研究。MNS指导下AF导管消融在不影响手术质量的情况下,可极大限度地减少辐射剂量。可以预见,在不久的将来,MNS会应用于更多AF患者的消融治疗[10, 11],并且可能向其他心血管疾病的介入治疗甚至其他领域的介入治疗逐步延伸推广,为进一步减少对患者和医护人员的放射损害作出贡献。
| [1] | Chida K, Saito H, Otani H, et al. Relationship between fluoroscopic time, dsoe-area product, body weight, and maximum radiation skin dose in cardiac interventional procedures[J]. Am J Roentgenol, 2006, 186(3):774-778. |
| [2] | Smith IR, Rivers JT, Hayes J, et al. Reassessment of radiation risks from electrophysiology procedures compared to coronary angiography[J]. Heart Lung Circ, 2009,18(3):191-199. |
| [3] | January CT, Wann LS, Alpert JS, et al. 2014 AHA/ACC/HRS guideline for the management of patients with atrial fibrillation:executive summary:A report of the American College of Cardiology/American Heart Association task force on practice guidelines and the Heart Rhythm Society[J]. Circulation, 2014-04-10. http://www.ncbi.nlm.nih.gov/pubmed/24682348. |
| [4] | Miyazaki S, Shah AJ, Xhaet O, et al. Remote magnetic navigation with irrigated tip catheter for ablation of paroxysmal atrial fibrillation[J]. Circ Arrhythm Electrophysiol, 2010, 3(6):585-589. |
| [5] | Proietti R, Pecoraro V, Di Biase L, et al. Remote magnetic with open-irrigated catheter vs. manual navigation for ablation of atrial fibrillation:A systematic review and meta-analysis[J]. Europace, 2013, 15(9):1241-1248. |
| [6] | Bauernfeind T, Akca F, Schwagten B, et al. The magnetic navigation system allows safety and high efficacy for ablation of arrhythmias[J]. Europace, 2011, 13(7):1015-1021. |
| [7] | Arya A1, Zaker-Shahrak R, Sommer P, et al. Catheter ablation of atrial fibrillation using remote magnetic catheter navigation:a case-control study[J]. Europace, 2011, 13(1):45-50. |
| [8] | Pezawas T, Ristl R, Bilinski M, et al. Single, remote-magnetic catheter approach for pulmonary vein isolation in patients with paroxysmal and non-paroxysmal atrial fibrillation[J]. Int J Cardiol, 2014, 174(1):18-24. |
| [9] | 冯俊, 王爱玲, 程景林, 等. 不同类型心血管介入手术辐射剂量分析[J]. 中华放射医学与防护杂志, 2012, 32(4):416-419. |
| [10] | Shurrab M, Danon A, Lashevsky I, et al. Robotically assisted ablation of atrial fibrillation:a systematic review and meta-analysis[J]. Int J Cardiol, 2013, 169(3):157-165. |
| [11] | Bradfield J, Tung R, Mandapati R, et al. Catheter ablation utilizing remote magnetic navigation:A review of applications and outcomes[J]. Pacing Clin Electrophysiol, 2012, 35(8):1021-1034. |
 2015, Vol. 35
2015, Vol. 35