2. 吉林大学附属第二医院放疗科
容积旋转调强(volumetric modulated arc therapy,VMAT)并不是一个新概念,早在1995年Yu[1]提出整套的在常规加速器上实现VMAT治疗的方法。在治疗过程中,VMAT可以实现不间断出束的同时,动态调节机架运动速度、照射剂量率和射野形状来增加治疗的自由度[2, 3, 4, 5],所以,VMAT治疗模式在理论上有着潜在的剂量学优势。在肺癌的放射治疗中,很多文献都报道了VMAT技术的剂量学特性,并指出可以减少计划MU数量,很大程度地减少治疗时间[6, 7, 8, 9, 10]。但是,并无文献报道利用不同厂家的计划系统(treatment planning system,TPS),所得到的肺癌VMAT计划结果的差异。本研究评估了Monaco 3.0和Pinnacle 9.2两套TPS所产生的肺癌VMAT计划结果的差异。
1. 定位与靶区勾画:选取20例在吉林省肿瘤医院放疗科接受放射治疗的肺癌病例,其中左肺癌10例,右肺癌10例,所有患者均采用仰卧位,双臂上抬交叉置额顶,热塑模配合体部固定板固定体位,CT扫描层厚为3 mm。扫描上界至环状软骨,下界达肾上腺。
由医师勾画大体肿瘤(GTV)、临床靶区(CTV)、计划靶区(PTV)及危及器官(OARs),包括心脏、脊髓和肺组织,GTV 包括临床和影像学所见肿瘤范围,CTV 由GTV 外放得到,向肺部方向外放5 mm,向转移淋巴结一侧外放5 mm。PTV 包括CTV 加上器官运动的范围以及摆位误差,由CTV外放5 mm 获得。处方剂量为6 000 cGy/30次。
2. 治疗设备:选用瑞典Elekta公司的Synergy加速器6 MV X射线;加速器光栅40对,等中心处光栅宽度为1.0 cm;加速器标定最大剂量率为600 MU/min,共7档剂量率,每档值为前一档减半;最小机架角剂量率为0.1 MU/级;最大机架转速8.0°/s;最大叶片运动速度2.4 cm/s;最小叶片间隙0.5 cm。
3. 计划设计:为方便比较研究,2种计划全部采用200°的一个顺时针的单弧完成,其中右肺癌计划的起止角度为181°/20°;左肺癌计划的起止角度为340°/180°。为避免多叶光栅(MLC)漏射平面与机架旋转平面平行,机头角设定为10°。
Monaco 3.0版本TPS的优化参数包含生物罚分函数与物理罚分函数,首先,分别对靶区及危及器官设置相应的优化函数,在第1步的通量优化过程中,选用危及器官优先,使用物理约束模型,进行1次优化。优化完成后,根据实际情况调整优化参数,并添加危及器官的生物约束模型,继续优化通量分布,当通量分布达到预期结果后,直接进入第2步的生成子野过程,添加对靶区Dmin和剂量体积直方图(DVH)的物理限制条件,换成靶区优先继续优化。计划设计中主要的参数设置如下:扇区角度20°,网格间距0.3 cm,计算精度3.0%,最大控制点数100,剂量率300 MU/min,最小叶片间距0.5 cm,通量平滑为"中"。
Pinnacle计划系统的VMAT计划设计是基于SmartArc模块实现的,优化的目标函数是利用物理点剂量定义的,为了弥补没有生物约束模型的不足,更好地保护肺和心脏,对并行器官设置2~3个物理点剂量约束。计划设计中主要的参数设置如下:剂量网格分辨率为0.4 cm,最终机架间距为4°,最大传输时间为150 s。
4. 计划参数比较:利用DVH比较和分析两种计划的剂量分布差别,剂量分布指标包括PTV的最大剂量(Dmax)、平均剂量(Dmean);最小剂量(Dmin)及PTV的均匀性指数(HI=D5/D95,其中,D5和D95分别为5%和95%的靶区体积所受到的照射剂量)、适形度指数(CI=VPTV、ref/VPTV×VPTV、ref/Vref,其中VPTV、ref为处方剂量覆盖的PTV体积;VPTV为PTV体积;Vref为处方剂量包绕的体积)、肺和心脏的平均剂量及受到特定剂量照射的体积;比较2种计划的MU数和计划执行时间、剂量验证精度。
根据以往的计划设计经验,2套TPS都可以对脊髓达到很好的保护效果,但是过度保护脊髓会增加肺脏受照剂量,不利于肺脏的保护,所以在计划设计时,仅严格限制脊髓的最大剂量<4 000 cGy。本研究不对脊髓受照剂量作比较研究。
5. 统计学处理:数据用x±s形式表示。采用SPSS 16.0软件进行分析,组间比较采用配对t检验。P<0.05为差异有统计学意义。
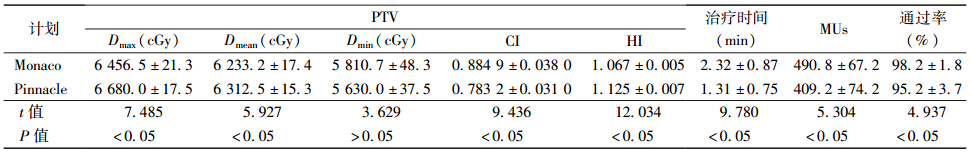
1. 剂量比较:所有计划都将覆盖95%PTV体积剂量归一为处方剂量。与Pinnacle计划相比,Monaco计划PTV的最大剂量减小约223.5 cGy(t=7.485,P<0.05);平均剂量更接近处方剂量,比Pinnacle计划少约79.3 cGy(t=5.927,P<0.05);CI(t=9.436,P<0.05)及HI(t=12.034,P<0.05)都优于Pinnacle计划。但是,PTV的最小剂量差异无统计学意义(表 1)。Monaco计划在靶区剂量分布方面的表现更加优秀。
| 表 1 20例肺癌患者2种计划PTV的剂量学参数、治疗效率及通过率的比较(x±s) |
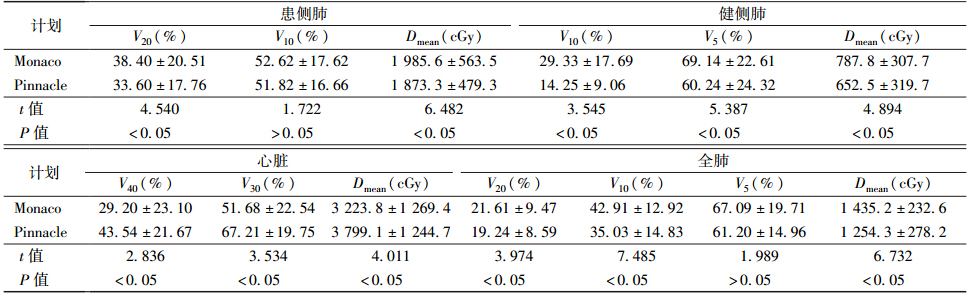
与Monaco计划相比,Pinnacle计划患侧肺、健侧肺及全肺的平均剂量分别减少约112.3 cGy (t=6.482,P<0.05)、135.3 cGy(t=4.894,P<0.05)和180.9 cGy(t=6.732,P<0.05);患侧肺的V20减少约4.8%(t=4.540,P<0.05);健侧肺的V10和V5分别减少约15.1%和8.9%(t=3.545、5.387,P<0.05);全肺的V20和V10分别减少约2.4%和7.9%(t=3.974、7.485,P<0.05)。但是,患侧肺的V10和全肺的V5差异无统计学意义(表 2)。在肺脏的保护方面,Pinnacle计划表现出明显的优势。
| 表 2 20例肺癌患者2种计划双肺及心脏的剂量比较(x±s) |
与Pinnacle计划相比,Monaco计划心脏的V40和V30 分别减少约14.34%和15.53%(t=2.836、3.534,P<0.05);心脏的平均剂量也少约575.3 cGy(t=4.011,P<0.05,表 2)。Monaco计划在心脏的保护方面明显优于Pinnacle计划。
2. 剂量投递:与Monaco计划相比,Pinnacle计划的执行时间减少约1.01 min(t=9.780,P<0.05),MU数量减少约81.6(t=5.304,P<0.05)。利用Delta4测量的两种计划γ(3 mm/3%)通过率,结果发现,Monaco的通过率要比Pinnacle高约3%(t=4.937,P<0.05,表 1)。
本研究利用Monaco和Pinnacle 2套计划系统设计肺癌VMAT计划,结果发现,Monaco 计划的靶区剂量及对心脏的保护要优于Pinnacle,但是对肺的保护方面,Pinnacle计划更具优势。和Monaco相比,Pinnacle计划有更多的剂量是集中在人体前后方向投递的,而在大部分肺癌病例中,前后方向都是保证肺脏避免接受过多低剂量照射的最佳角度,这可能是Pinnacle计划对肺保护更好、而对心脏的保护更差的原因之一。在肺癌的放射治疗中,对靶区剂量分布影响最大的危及器官是肺脏,Monaco在第2步优化时使用的"靶区优先"选项是为了获得更好的靶区剂量分布结果,而有意放松严重影响靶区剂量提升的肺脏的剂量限制。在实际应用中,就是减小为了保护肺脏而产生的剂量调制的复杂度,也就是减少前后方向射束的权重,增加靶区两侧穿射肺脏的射野权重。这样的结果就是增加肺脏的照射剂量,而对于靶区来说,因为增加靶区两侧入射方向的投射剂量,适当减小了前后方向的剂量调制压力,致使靶区剂量分布更优。同时,减少前后方向的投射剂量,也导致心脏获得了更好地保护。
由于优化、子野生成及剂量计算算法方面的差异,Pinnacle计划MU数量少,剂量投递效率高,在实际应用中发现,和Monaco相比,Pinnacle计划MLC射野面积相对较大,大面积的射野可以照射更多的靶区体积,和小面积子野相比MU利用率会更高,但是Pinnacle生成的子野偏窄,多为长条状,且不规则,而Monaco 子野安排采用"扫地序列",在光栅变换位置时,"引导光栅"先运动到一个位置,然后"跟随光栅"再按照设定的速度运动。这使得其生成的窄条野相对较少,这也许是其剂量验证结果优于Pinnacle的原因之一。同样,也可能正因为Pinnacle生成的子野形状不规则,才使得其剂量调制能力比Monaco更好,致使Pinnacle在肺脏保护方面表现更优。另外,在危及器官的DVH上Monaco可以利用生物目标函数进行无数个点位的剂量约束,虽然Pinnacle仅利用物理目标函数对危及器官进行剂量约束,但是同一器官利用多个物理目标函数对DVH上的多点进行约束时,可以适当弥补Pinnacle优化过程中缺少生物目标函数的不足。
因为Monaco的剂量计算采用蒙特卡罗算法,这使得其剂量计算更加准确,验证通过率也更高,但是优化速度相对于Pinnacle的采用的卷积/迭加算法要慢很多。另外,Monaco在计划设计时,初始的优化处方设置非常重要,优化过程中可以人为参与的地方很少,如若优化过程中发现需要修改优化的处方参数,必须重新进行第1步的通量优化,而Pinnacle进行优化时,物理师可以全程参与其中,随时根据计算结果修改处方,而不需要完全重新优化。所以,与Monaco相比,利用Pinnacle设计治疗计划需要的时间更少。
在实际工作中,很多单位会有2种或者2种以上的TPS,了解不同TPS间计划设计的区别以及同种病例利用不同TPS产生的计划结果间的差异,便于临床工作中根据实际情况选择不同的TPS设计治疗计划。
| [1] | Yu CX. Intensity-modulated arc therapy with dynamic multileaf collimation: an alternative to tomotherapy[J]. Phys Med Biol, 1995, 40(9):1435-1449. |
| [2] | Duthoy W, De Gersem W, Vergote K, et al. Whole abdominopelvic radiotherapy (WAPRT) using intensity-modulated arc therapy (IMAT): first clinical experience[J]. Int J Radiat Oncol Biol Phys, 2003, 57(4):1019-1032. |
| [3] | Otto K. Volumetric modulated arc therapy: IMRT in a single gantry arc[J]. Med Phys, 2008, 35(1):310-317. |
| [4] | Bedford JL. Treatment planning for volumetric modulated arc therapy[J]. Med Phys, 2009, 36(11):5128-5138. |
| [5] | Yu CX, Tang G. Intensity-modulated arc therapy: principles, technologies and clinical implementation[J]. Phys Med Biol, 2011, 56(5):R31-54. |
| [6] | 张矛,金海国,苏清秀,等. 肺癌静态调强与容积旋转调强放射治疗间比较[J]. 中国医学物理学杂志, 2013, 30(5):4364-4368. |
| [7] | 孙尧,刘希军,刘同海,等. 胸中段食管癌三维适形放疗、调强放疗及旋转调强放疗的剂量学研究[J]. 肿瘤研究与临床, 2013, 25(1):15-18. |
| [8] | 弓健,余荣,吴昊,等. 中心型肺癌快速旋转调强与固定射野动态调强放疗的剂量学比较[J]. 中华放射医学与防护杂志, 2010, 30(4):448-451. |
| [9] | Bedford JL, Nordmark Hansen V, McNair HA, et al. Treatment of lung cancer using volumetric modulated arc therapy and image guidance: a case study[J]. Acta Oncol, 2008, 47(7):1438-1443. |
| [10] | Chan OS, Lee MC, Hung AW, et al. The superiority of hybrid-volumetric arc therapy (VMAT) technique over double arcs VMAT and 3D-conformal technique in the treatment of locally advanced non-small cell lung cancer—a planning study[J]. Radiother Oncol, 2011, 101(2):298-302. |
 2015, Vol. 35
2015, Vol. 35