放射性臂丛神经损伤是一种少见的放疗后并发症,但其严重影响肿瘤放疗患者的生存质量,多见于鼻咽癌及其他头颈部肿瘤放射治疗后,顽固性神经病理性疼痛是放射性臂丛神经损伤的显著特征[1]。Chen等[2]报道在头颈部肿瘤患者放疗后发生放射性臂丛神经损伤潜伏期在6~135个月,平均56个月,12%的患者出现明显症状。目前,放射性臂丛神经损伤的治疗方法包括手术治疗和药物治疗等,但疗效都不确切[3, 4]。
普瑞巴林是一种新型钙离子通道拮抗剂,它与电压门控的钙离子通道α2-δ亚基结合,通过调节神经递质的释放影响疼痛传导通路,普瑞巴林已被证实在多种周围及中枢神经病理性疼痛中有治疗效果[5, 6],目前被多项指南认为是治疗神经病理性疼痛的一线用药[7, 8]。本研究旨在探索普瑞巴林治疗放射后臂丛神经疼痛的疗效和耐受性,以及患者的其他症状改善情况。
1. 临床资料及入组标准:中山大学孙逸仙纪念医院神经科2009年1月至2015年5月收治鼻咽癌放疗后臂丛神经损伤患者103人,其中疼痛伴或不伴有上肢乏力的患者49人,轻度疼痛4人,中重度疼痛45人,单纯上肢乏力14人,上肢麻木或感觉减退29人,麻木或感觉减退伴上肢乏力11人。
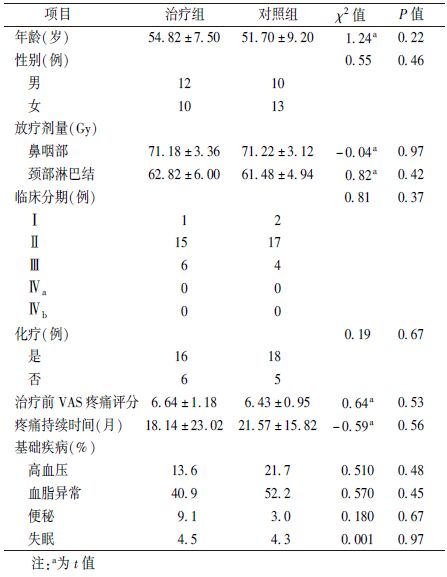
满足以下入组条件的病例并服用普瑞巴林治疗的患者入组普瑞巴林治疗组,符合入组标准但未服用普瑞巴林治疗的患者为对照组。入组标准:①既往有确诊鼻咽癌且有放射治疗史;②放射治疗后出现单侧或双侧上肢中重度疼痛3个月以上;③MRI证实臂丛神经损伤。排除标准:①具有肿瘤复发或转移表现;②严重认知功能障碍;③肩关节周围炎、脊髓损伤等神经系统其他原因导致的上肢疼痛。共入组患者45人,其中,治疗组22人,对照组23人。两组患者一般资料及基础疾病情况见表1。
| 表1 患者一般资料 |
2. 治疗及评估方法:两组患者均进行根治性放射治疗,并且均为首程放疗。22例普瑞巴林治疗组中行常规二维放疗17例,行三维适形放疗/调强适形放疗5例;采用面颈联合野+耳前野(19例)或面颈联合野+耳前野+颈前切线野(3例)两种照射治疗;鼻咽部放疗剂量为66 ~76 Gy,平均照射剂量为(71.18±3.36)Gy,颈部淋巴结放疗总剂量为56~72 Gy,平均照射剂量为(62.82±6.00)Gy。23例对照组患者中行常规二维放疗16例,行三维适形放疗/调强适形放疗7例;采用面颈联合野+耳前野(19例)或面颈联合野+耳前野+颈前切线野(4例)两种照射治疗;鼻咽部放疗剂量为66 ~76 Gy,平均照射剂量为(71.22±3.12)Gy,颈部淋巴结放疗总剂量为52~70 Gy,平均照射剂量为(61.48±4.94)Gy,治疗组与对照组相比差异无统计学意义。
治疗组患者普瑞巴林起始剂量为口服75 mg,2次/d,维持1周,第2周用药方案调整为150 mg,2次/d,第3周根据患者的临床疗效和耐受程度决定剂量是否加量至300 mg,2次/d。治疗组和对照组患者均接受糖皮质激素、B族维生素、营养神经药物治疗及对症治疗。每周用视觉模拟评分法(VAS)对患者进行评分,以应答率(与基线相比,疼痛量表减分率达到30%~50%的患者比例)作为主要疗效终点,神经病理性疼痛症状量表(NPSI)、医院焦虑抑郁量表(HADS)、临床总体印象(CGIC)、患者总体变化印象(PGIC)和睡眠干扰评分作为次要疗效终点。各评定量表均由本院2位神经专科医师进行独立评定。
3.统计学处理:采用SPSS 19.0软件进行数据统计,定量资料采用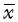 ±s表示。定量资料符合正态分布方差齐者进行t检验,不符合正态分布者行Wilcoxon秩和检验;定性资料采用χ2检验。P<0.05为差异有统计学意义。
±s表示。定量资料符合正态分布方差齐者进行t检验,不符合正态分布者行Wilcoxon秩和检验;定性资料采用χ2检验。P<0.05为差异有统计学意义。
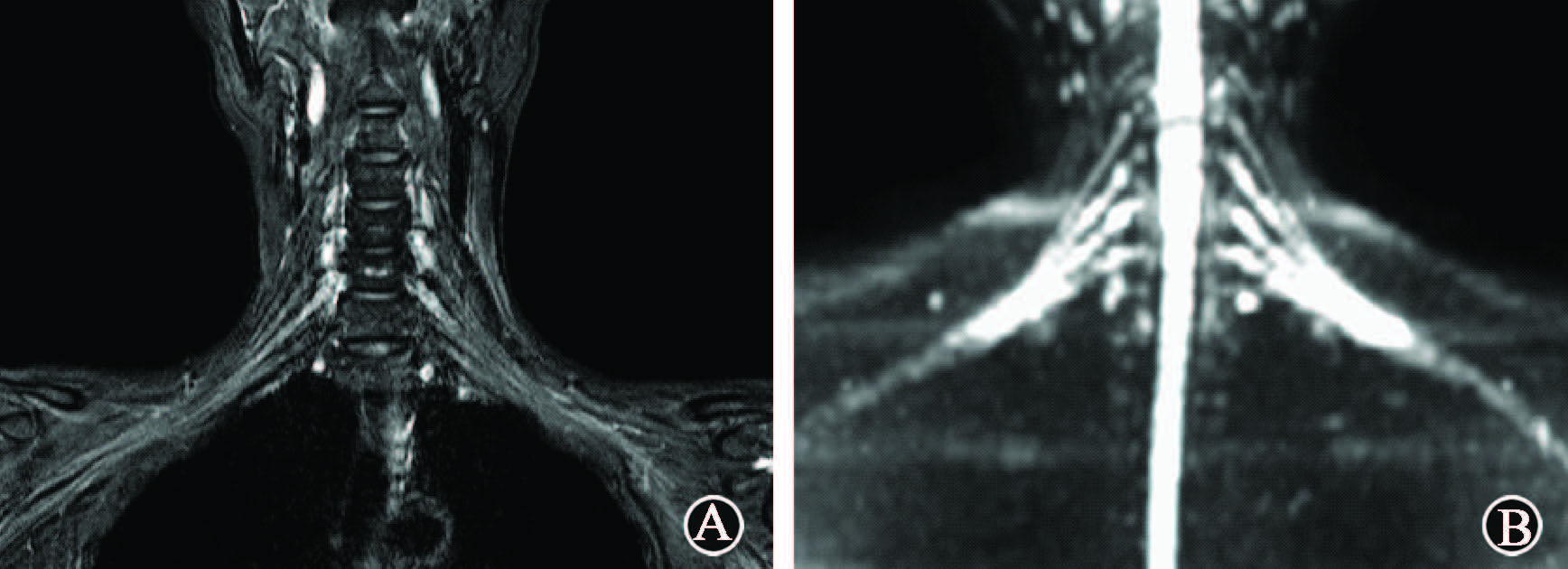
1.放射性臂丛神经损伤患者影像学表现:典型的放射性臂丛神经损伤磁共振表现为单侧或双侧神经干、神经根和斜角肌肿胀,T2序列信号增强,DWI序列呈弥散受限改变,见图1。
|
注:女,50岁,鼻咽癌放疗后臂丛神经损伤。双侧臂丛神经根、 干区稍肿胀,T2WI信号增强,增强扫描神经根鞘膜轻度强化 图1 鼻咽癌患者臂丛神经MRI表现 A.STIR序列;B.DWIBS序列 |
2.主要疗效终点的评估:对患者每周进行视觉模拟量表评分,两组患者12周后较基线水平均有下降,治疗组的评分从6.6到4.7分,对照组从6.4到5.5分。治疗组应答率为36.4%,对照组应答率为9.1%,两组差异有统计学意义(χ 2=4.98,P<0.05)。
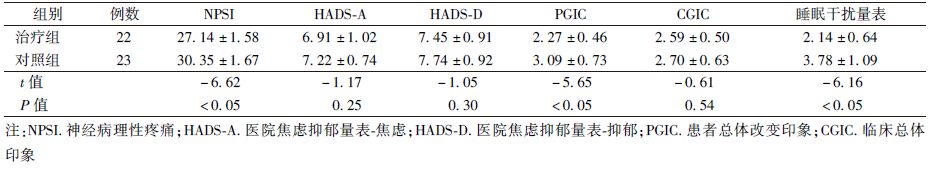
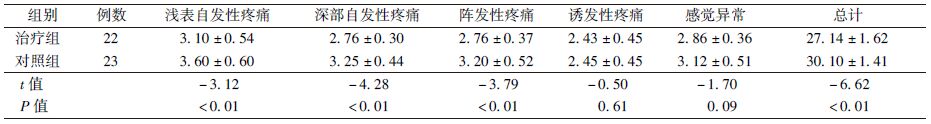
3.次要疗效终点的评估:治疗结束后,神经病理性疼痛症状量表评分治疗组总分低于对照组,差异有统计学意义(t=-6.62,P<0.05)。HADS-A和HADS-D评分治疗组与对照组比较,差异无统计学意义(P>0.05),PGIC评分治疗组低于对照组,差异有统计学意义(t=-5.65,P<0.05),而CGIC评分治疗组与对照组比较,差异无统计学意义(P>0.05)。睡眠干扰量表对睡眠质量评估显示治疗组评分低于对照组(t=-6.16, P<0.05),见表2。用NPSI量表对患者疼痛性质进一步细分,分为浅表自发性疼痛、深部自发性疼痛、阵发性疼痛、诱发性疼痛和感觉异常,对各项评分进行对比显示,普瑞巴林可以有效减少治疗组患者浅表自发性疼痛、深部自发性疼痛和阵发性疼痛,与对照组相比差异有统计学意义,而对于诱发性疼痛和感觉异常与对照组相比,差异无统计学意义,见表3。
表2 次要疗效量表评分(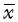 ±s) ±s)
|
表3 神经病理性疼痛症状评分量表(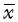 ±s) ±s)
|
4.不良反应:普瑞巴林最常见的不良反应为头晕、嗜睡、周围性水肿、头痛和体重增加。治疗组22例患者中出现头晕3例,嗜睡2例;对照组共23例患者出现头晕2例,头痛1例。两组不良反应率分别为22.7%和13%,差异无统计学意义(χ2=0.72,P>0.05)。两组患者中未出现因不良反应而停药或减药情况,能够较好地耐受当前剂量。
放疗后导致臂丛神经损伤可能的发病机制包括:神经及结缔组织纤维化,微小血管闭塞,射线对轴突及髓鞘的直接损伤[9]。放射性臂丛神经损害的形成是个动态的过程,早期为伴有慢性炎症的无症状性纤维化前期,发展到细胞外基质沉积的纤维化期,晚期为纤维营养不良期。放射性臂丛神经损伤的机制涉及到多方面的失衡,如成纤维细胞的增生,细胞外基质的沉积,细胞因子的扩增。在这个过程中起关键作用的成分是活性氧自由基。自由基在细胞分化、增生、炎症等正常的生理功能中起重要作用,但在生物化学性损伤、感染性物质、抗氧化屏障缺陷所诱导的自由基产生过多时可引起病理性应激反应。当损伤过重引起氧化应激反应过度时可诱发纤维化的形成,而反复的慢性或短暂性的应激都能导致自由基产生过多,从而促进纤维化过程。
普瑞巴林是新型γ-氨基丁酸受体激动剂,它与中枢神经系统电压门控的钙离子通道α2-δ亚基结合,减少钙离子内流,通过减少兴奋性神经递质的释放,影响疼痛传导通路的机制,从而有效缓解神经病理性疼痛。
本研究给予治疗组患者服用普瑞巴林150~600 mg持续12周,对放射后臂丛神经损伤疼痛症状的疗效及耐受性,以及患者焦虑、抑郁状态、睡眠状况进行了研究,研究结果提示,普瑞巴林可以有效地缓解放射后臂丛神经损伤患者的疼痛症状,治疗组应答率明显高于对照组,同时研究对进一步疼痛性质的改善情况进行了NPSI评分,结果发现普瑞巴林可以有效改善患者浅表、深部自发性疼痛和阵发性疼痛症状,而对诱发性疼痛和感觉异常的治疗作用与对照组相比,差异无统计学意义。本研究结果与既往普瑞巴林治疗糖尿病周围神经病效果一致[10, 11]。普瑞巴林还能改善患者PGIC和睡眠干扰评分,而对患者焦虑、抑郁症状与对照组无明显差异。既往研究中,普瑞巴林治疗卒中后中枢性疼痛可改善患者焦虑、抑郁状态[12],本研究中治疗结束后治疗组与对照组患者HADS-A评分分别为6.91 和7.22分,治疗组与对照组患者HADS-D平均评分分别为7.45和7.74分,患者的评分为5~9,其中≥8分者占总数的29.3%。本研究结果与既往研究结果不同的可能原因有:①疾病模型不同,卒中后中枢性疼痛与臂丛神经损伤引起的疼痛给患者带来的主观疼痛感觉不同;②本研究中患者焦虑抑郁程度较轻者多,而程度重的患者比例少,因此与对照组相比不易得出有差异性的结果。与以往研究一致,本研究中睡眠干扰评分结果显示,与对照组相比,普瑞巴林可以改善患者的睡眠质量。普瑞巴林的安全性方面,研究记录了两组患者中常出现的不良反应,包括头晕、嗜睡、周围性水肿、头痛及体重增加,两组不良反应发生率分别是22.7%和13%,最多出现的是头晕、嗜睡和头痛,两组患者都能很好地耐受。
普瑞巴林可治疗各种中枢性、周围性神经病理性疼痛和部分性癫痫发作。目前,临床已开展的周围性神经病理性疼痛随机对照研究包括痛性糖尿病周围神经病、带状疱疹后神经痛。一项为期13周的治疗带状疱疹后神经痛的随机对照研究证实,普瑞巴林能够减轻带状疱疹后神经痛,并能减轻疼痛对患者导致的睡眠干扰。在安全性方面,通过对不良反应时间、体格检查和神经科检查、12导联脑电图、生命体征和实验室检查的结果监测都证明患者可以很好地耐受[13]。
综上所述,普瑞巴林治疗放射性臂丛神经损伤疼痛有较好的疗效,并且患者对每天两次,总剂量150~600 mg普瑞巴林有较好的耐受性,但由于本临床研究纳入的例数较少,关于普瑞巴林治疗的最佳剂量等治疗策略仍需通过大规模多中心的临床试验进行进一步研究。
| [1] | Kori SH, Foley KM, Posner JB. Brachial plexus lesions in patients with cancer: 100 cases[J]. Neurology,1981,31(1):45-50. |
| [2] | Chen AM, Hall WH, Li J, et al. Brachial plexus-associated neuropathy after high-dose radiation therapy for head-and-neck cancer[J]. Int J Radiat Oncol Biol Phys,2012,84(1):165-169. |
| [3] | Dubinsky RM, Kabbani H, El-Chami Z, et al. Practice parameter: treatment of postherpetic neuralgia: an evidence-based report of the Quality Standards Subcommittee of the American Academy of Neurology[J]. Neurology,2004,63(6):959-965. |
| [4] | Gu B, Yang Z, Huang S, et al. Radiation-induced brachial plexus injury after radiotherapy for nasopharyngeal carcinoma[J]. Jpn J Clin Oncol,2014,44(8):736-742. |
| [5] | Raskin P, Huffman C, Yurkewicz L, et al. Pregabalin in subjects with painful diabetic peripheral neuropathy using an NSAID for other pain conditions: a double-blind crossover study[J]. Clin J Pain,2015,in print. |
| [6] | Arnold LM, Sarzi-Puttini P, Arsenault P, et al. Efficacy and Safety of Pregabalin in Patients with Fibromyalgia and Comorbid Depression Taking Concurrent Antidepressant Medication: A Randomized, Placebo-controlled Study[J]. J Rheumatol,2015,42(7):1237-1244. |
| [7] | Attal N, Cruccu G, Haanpää M, et al. EFNS guidelines on pharmacological treatment of neuropathic pain[J]. Eur J Neurol,2006,13(11):1153-1169. |
| [8] | Dworkin RH, O'Connor AB, Backonja M, et al. Pharmacologic management of neuropathic pain: evidence-based recommendations[J]. Pain,2007,132(3):237-251. |
| [9] | Delanian S, Lefaix JL, Pradat PF. Radiation-induced neuropathy in cancer survivors[J]. Radiother Oncol,2012,105(3):273-282. |
| [10] | Lesser H, Sharma U, LaMoreaux L, et al. Pregabalin relieves symptoms of painful diabetic neuropathy: a randomized controlled trial[J]. Neurology,2004,63(11):2104-2110. |
| [11] | Dworkin RH, Corbin AE, Young JJ, et al. Pregabalin for the treatment of postherpetic neuralgia: a randomized, placebo-controlled trial[J]. Neurology,2003,60(8):1274-1283. |
| [12] | Kim JS, Bashford G, Murphy TK, et al. Safety and efficacy of pregabalin in patients with central post-stroke pain[J]. Pain,2011,152(5):1018-1023. |
| [13] | van Seventer R, Feister HA, Young JP Jr, et al. Efficacy and tolerability of twice-daily pregabalin for treating pain and related sleep interference in postherpetic neuralgia: a 13-week, randomized trial[J]. Curr Med Res Opin,2006,22(2):375-384. |
| [14] | Kim JS, Bashford G, Murphy TK, et al. Safety and efficacy of pregabalin in patients with central post-stroke pain[J]. Pain,2011,152(5):1018-1023. |
| [15] | Lesser H, Sharma U, LaMoreaux L, et al. Pregabalin relieves symptoms of painful diabetic neuropathy: a randomized controlled trial[J]. Neurology,2004,63(11):2104-2110. |
 2015, Vol. 35
2015, Vol. 35