联合国原子辐射效应科学委员会(UNSCEAR)研究表明,辐射中占比最大的是医疗照射,其中X射线摄影对公众的集体剂量贡献最大[1, 2]。器官剂量是用于评价受检者辐射风险的关键物理量,然而直接测量器官剂量耗时费力,越来越多的研究者致力于计算机虚拟人体模型的开发[3, 4]。目前,对于X射线摄影中受检者剂量转换系数的数据大多是基于简单程式化数学模型(MIRD)计算得出的,包括国内现行有效的转换系数标准,也是基于MIRD模型模拟计算的结果[5]。然而MIRD模型因为只有器官位置和几何构型的大体特征,导致很多解剖学细节都被忽略,误差较大;新一代体素模型具有更精细的解剖结构,实现了人体的三维数字化重建。已有学者利用体素模型模拟计算单能平行光束的面源全身照射时剂量转换系数,但由于源与照射范围的不同,导致上述研究结果并不适用于医用X射线摄影[6, 7, 8]。因此,需要利用体素模型重新计算,为更新X射线摄影的剂量转换系数标准提供科学参考。
1. 体模选择:选用德国环境健康中心提供的成年男性体素模型,身高176 cm,体重73 kg[9]。该体模是通过CT和MRI等影像学手段,将断层照片在三维尺度上重组构成的模型,体素大小为0.213 7 cm× 0.213 7 cm × 0.8 cm,列、排和层的数量分别为254 ×127 × 222。模型包括141个解剖学区域,分别赋予特定的密度和元素组成[10]。在相同计算条件下,利用美国橡树岭国家实验室开发的MIRD成年模型开展模拟计算,进行对比分析。
2. 源项建立和摄影参数选取:X射线摄影中的源项为点源发出的锥形束,通过方形准直器校正后使达到体表的射野为规则的矩形[11]。根据不同的诊断检查和照射体位,选择相应的摄影参数作为模拟计算的源项。采用Xcomp5r作为本研究模拟计算的X射线能谱源项。
本研究选取了5种较为常见且所致受检者入射体表剂量(ESD)相对较大的照射情形展开模拟计算[12, 13],相关摄影体位的曝光参数(管电压、滤过、射野和焦皮距)选用最为常用的数据,分别为胸部后前位,120 kVp、3.0 mm Al、160 cm和40 cm×40 cm;胸部左侧位,120 kVp、3.0 mm Al、145 cm和38 cm×38 cm;胸部右侧位,120 kVp、3.0 mm Al、145 cm和38 cm×38 cm;腹部前后位,90 kVp、2.5 mm Al、75 cm和30 cm×40 cm;腰椎前后位,90 kVp、3.0 mm Al、 75cm和30 cm×40 cm。
3. 入射体表剂量和器官剂量的蒙特卡罗(MC)模拟:应用MC模拟计算软件MCNPX,分别将体素模型、MIRD数字体模和源项加载到输入文件中,并构建特定检查体位的几何空间。体模受照表面放置空气探测器来模拟得到入射体表剂量,光子在体模内各组织与器官的沉积能量通过MCNPX软件中的能量沉积卡进行计算。为了确保照射野内器官剂量模拟计算结果的相对误差 < 5%,本研究每次计算所用的光子数设定为1×107。
4. 统计学处理:采用洛斯阿拉莫斯国家实验室开发的MCNPX 2.5统计分析软件进行X射线摄影照射情形的模拟计算。两模型模拟所得转换系数的相对偏差(%)指绝对偏差占MIRD模型所得结果的百分比。
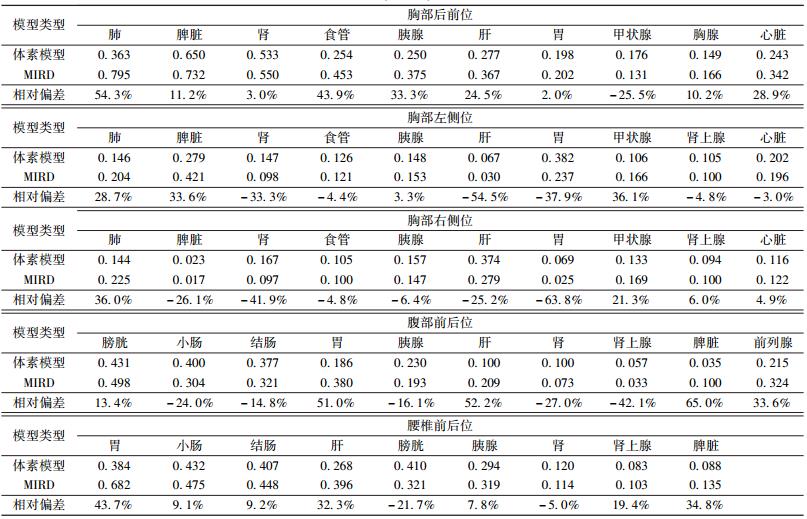
基于两种数字人体模型剂量转换系数计算结果:通过MC计算得到胸部后前位、胸部左侧位、胸部右侧位、腹部前后位和腰椎前后位的剂量转换系数值结果列于表1。结果显示,胸部后前位射野内器官剂量转换系数范围是0.149~0.650,其中脾脏转换系数最高是0.650;胸部左侧位射野内器官剂量转换系数范围是0.067~0.382,胃转换系数最高是0.382;胸部右侧位射野内器官剂量转换系数范围是0.023~0.374,肝转换系数最高是0.374;腹部前后位射野内器官剂量转换系数范围是0.035~0.431,膀胱转换系数最高是0.431;腰椎前后位射野内器官剂量转换系数范围是0.083~0.432,小肠转换系数最高是0.432。
| 表 1 利用体素模型和程式化模型模拟(MIRD)不同照射位置的剂量转换系数值结果 |
数据显示,5种不同照射体位下对应的器官剂量转换系数值,利用两种不同体模模拟得到的结果差异较大,如两模型器官剂量转换系数差异,胸部后前位照射剂量转换系数最大达54.3%,胸部左侧位照射差异最大为54.5%,胸部右侧位照射差异最大为63.8%,腹部前后位照射差异达65.0%,腰椎前后位照射的差异为43.7%。
对于胸部后前位摄影,如Wise等[14]利用MIRD模型模拟得到的肺的剂量转换系数是0.776,食管为0.378。与体素模型得到的结果相比,肺的相对偏差高达53.2%,食管为43.0%。通过比较模型参数得知,两种体模肺部、食管的密度及元素组成一致,而器官体积存在一定差异,如MIRD体模的肺部体积为3 370 cm3,体素模型的肺部体积为2 891.3 cm3,两者相差近17%。从解剖学结构上分析,MIRD体模的外部轮廓是光滑的椭圆,体素模型则体现了肩胛骨等结构,且肺部与体表的组织厚度差异很大,更加直观地说明体素模型的剂量转换系数<MIRD体模的原因。两种体模内食管解剖结构不同,周围的组织环境也相差甚远,导致剂量转换系数差异较大。
对于腹部前后位摄影,国家辐射防护委员会(NRPB)利用MIRD模型模拟得到的器官转换系数与体素模型相比存在差异,如肝脏的转换系数为0.192,相对偏差为47.9%;小肠的转换系数为0.291,相对偏差为27.2%[15]。肝脏剂量转换系数结果不同的原因可能为,两种模型的器官形态和位置差异造成,MIRD模型中的肝脏不区分左右肝叶,只是以简单的光滑椭球体代表,相对粗略。胃的剂量转换系数相差较大,主要是因为,在MIRD体模中,胃在模体左侧,而真实情况下胃组织在左右侧均有,而中心偏向左侧。由于体素模型肠道系统解剖结构和位置复杂,更接近真实人体,MIRD模型的肠道仅是由简略的圆柱管拼接而成,使得两种模型结肠和小肠的剂量转换系数结果差异明显。
对于腰椎前后位摄影,Begum[16]利用MIRD模型模拟得到的胃和膀胱的剂量转换系数分别为0.535和0.228,与体素模型模拟结果相比,差异较大,分别为28.2%和44.4%。胃肠道系统由于其复杂的解剖架构及两模型间的器官差异,必然导致剂量转换系数产生差异。膀胱的剂量转换系数不同,是由于解剖学深度不同导致,MIRD模型的膀胱由充盈的椭球体代表,而体素模型的膀胱充盈欠佳,另外,MIRD模型的膀胱与受照体表的距离大于体素模型。
综上所述,分析差异原因,主要是模拟计算用的体模不同导致。体素模型由真人断层图像数据处理得到,在外部形态上更接近人体,而MIRD体模仅仅是简单的几何体(椎体、柱体)构建而成,两者对于入射X射线的反散射效果不同;从内部结构看,各个器官在体内的位置不同,器官本身的体积大小和形状也不同,是导致器官剂量差异的主要原因;相同器官周围的组织环境也不尽相同,使得到达两个体模内相同器官的X射线剂量发生改变。因此,选用的人体模型不同,会使剂量转换系数产生较大差异。
本研究分别利用体素模型和MIRD模型结合蒙卡统计软件MCNPX,模拟了X射线摄影中5种常见的检查体位下受检者的辐射剂量,并计算得到不同检查体位下的器官剂量与入射体表剂量的转换系数。通过与其他研究结果比较得出,两种数字人体模型计算出的器官剂量转换系数差异较大。本研究利用MIRD模型模拟计算得到的剂量转换系数结果与其他MIRD的研究结果相比,偏差 < 5%,一致性较好,从而验证本研究结果的可靠性。体素模型基于人体解剖结构的彩色切片照片构建而成,相比由简单几何体组成的MIRD体模更加接近真实受检者,因此,利用体素模型模拟计算得到的辐射剂量及转换系数也更加合理准确。采用基于MIRD模型计算出的剂量转换系数来估算X射线摄影所致受检者的器官剂量,可能会引入较大的计算误差,因此,有必要采用基于体素模型的计算结果对现有的剂量转换系数进行更新。
| [1] | United Nations Scientific Committee on the Effects of Atomic Radiation. Sources and effects of ionizing radiation. Vol.Ⅰ:Sources[R]. New York:UNSCEAR, 2000. |
| [2] | 郑钧正,贺青华,李述唐,等. 我国电离辐射医学应用的基本现状[J]. 中华放射医学与防护杂志, 2001,20(S1):13-20. |
| [3] | Faulkner K, Marshall NW. The relationship of effective dose to personnel and monitor reading for simulated fluoroscopic irradiation conditions[J]. Health Phys, 1993, 64(5):502-508. |
| [4] | McCollough CH, Schueler BA. Calculation of effective dose[J]. Med Phys, 2000, 27(5):828-837. |
| [5] | 中华人民共和国卫生部. GB/T 16137-1995 X射线诊断中受检者器官剂量的估算方法[S]. 北京:中国标准社, 1995. |
| [6] | Li J, Qiu R, Zhang Z, et al. Organ dose conversion coefficients for external photon irradiation using the Chinese voxel phantom(CVP)[J]. Radiat Prot Dosim, 2009, 135(1):33-42. |
| [7] | Lee C, Lee C, Lee JK. Applicability of dose conversion coefficients of ICRP 74 to Asian adult males:Monte Carlo simulation study[J]. Appl Radiat Isot, 2007, 65(5):593-598. |
| [8] | Patni HK, Nadar MY, Akar DK, et al. Selected organ dose conversion coefficients for external photons calculated using ICRP adult voxel phantoms and Monte Carlo code FLUKA[J]. Radiat Prot Dosim, 2011, 147(3):406-416. |
| [9] | International Commission on Radiological Protection. ICRP Publication 110. Adult reference computational phantoms[R]. Oxford:Pergamon Press, 2009. |
| [10] | International Commission on Radiological Protection. ICRP Publication 89. Basic anatomical and physiological data for use in radiological protection:reference values. A report of age-and gender-related differences in the anatomical and physiological characteristics of reference individuals[R]. Oxford:Pergamon Press, 2002. |
| [11] | 孔燕. 介入放射学工作人员个人剂量检测与评价方法研究[D]. 上海:复旦大学, 2014. |
| [12] | 高林峰,姚杰,钱爱君,等. 上海市2007年X射线诊断的医疗照射应用频率及其分布[J]. 环境与职业医学, 2009,26(6):532-536. |
| [13] | 杜向阳,翁伟芳. 上海市黄浦区2007年X射线诊断的医疗照射频率分布[J]. 环境与职业医学, 2009, 26(6):563-564. |
| [14] | Wise KN, Sandborg M, Persliden J, et al. Sensitivity of coefficients for converting entrance surface dose and kerma-area product to effective dose and energy imparted to the patient[J]. Phys Med Biol, 1999, 44(8):1937-1954. |
| [15] | Hart D, Jones DG, Wall BF. Normalised organ doses for medical X-ray examinations calculated using Monte Carlo techniques. NRPB-SR262[R]. Chilton UK:NRPB, 1994. |
| [16] | Begum Z. Entrance surface, organ and effective doses for some of the patients undergoing different types of X-ray procedures in Bangladesh[J]. Radiat Prot Dosim, 2001, 95(3):257-262. |
 2015, Vol. 35
2015, Vol. 35