目前,全中枢神经系统放射治疗(craniospinal irradiation,CSI)是常见的多种中枢神经系统肿瘤的治疗方式。与常规和调强放疗两种放疗方法相比,螺旋断层放疗(helical tomotherapy,HT)技术在CSI的剂量学方面具有明显优势[1, 2, 3, 4, 5, 6, 7],该技术可以一次完成160 cm×40 cm的大范围调强照射,且治疗过程中不会出现因射野衔接而产生的剂量冷、热点。但此技术有一个不可忽略的缺陷,即治疗时间与靶区的长度成正比;常规和调强放射治疗技术在CSI中的弊端主要表现在靶区剂量分布不均匀、射野长度不够且射野衔接处容易出现冷、热点等方面[8, 9, 10, 11, 12, 13]。本研究旨在运用多中心计划设计方法(multi-ISO center planning method,M-ISO)解决调强放射治疗在CSI技术上存在的弊端,并评估该方法在全中枢神经系统调强放疗中的应用价值。
1. 研究对象:选取2013年8月至2014年11月在本院接受HT的CSI患者10例,将其CT图像经网络传输至Eclipse11.0(美国Varian公司)计划系统,利用M-ISO对该10例患者重新进行计划设计,比较两种计划方式得出放疗计划的剂量学以及机器参数之间的差异。
2. 多中心计划设计方法:该10例患者靶区长度范围为59.7~80.4 cm,而常规加速器最大射野范围为40 cm×40 cm,故而在多等中心计划设计时,计划等中心的数量设定为2~3个;为满足全脑靶区剂量均匀性以及危及器官耐受量等要求,等中心之间的间距不得超过35 cm,即射野之间必须有交叉范围。本研究中采用旋转调强(intensity-modulated arc radiotherapy,IMAT)的方式进行计划设计,可以缩短治疗计划执行时间;加速器能量为6 MV X射线,60对多叶光栅,整个多中心计划运用4个弧,全脑处等中心设计两个弧,另外的等中心设计为1个弧,弧的长度为179°~181°,准直器角度设置为10°,这样的多等中心计划可以完全覆盖长度超过40 cm的靶区,由于该计划是在一个调强计划中完成优化,因此,可以严格控制该计划中的冷、热点以及靶区和危及器官的受照剂量。螺旋断层放疗计划设计参数为:调强计划的调制因子(modulation factor)均选用3.5,螺距比(pitch)均为0.43,射野宽度(field width)选择5.02 cm。两组计划处方剂量以及分割方式一致,均为靶区PTV CSI DT 36 Gy/18次,单次剂量2 Gy;危及器官的受量以及正常组织(体表轮廓减去靶区的体积)受照剂量尽量低。
3. 治疗计划评估:对比观察两组计划的截面剂量分布、靶区和危及器官的剂量体积直方图(DVH);对靶区、危及器官以及正常组织受照剂量行统计学分析。靶区PTV(全中枢神经系统)的分析指标包括D98%、D95%、D50%、D2%、Dmean、均匀性指数(HI)和适形指数(CI),Dx%表示x%的靶区体积受到的照射剂量,Dmean为平均剂量;对眼晶状体、视神经、视交叉等评估Dmax,Dmax表示最大剂量点,腮腺、下颌腺、甲状腺等评估Dmean,双肺评估V5、V10、V20、V30和Dmean,Vx表示肺组织受到x Gy照射的体积;HI的计算公式为:HI=(D2%-D98%)/D50%[14],HI取值越接近0,表示均匀性越好;CI的计算公式为:CI=VPIV/VPTV,其中VPIV为参考等剂量线包绕的所有区域的体积,VPTV为靶区体积,CI值越接近1,适形度越好;对正常组织比较V5、V10、V20和V36;最后,比较两组计划的执行时间和机器跳数(MU)的均值。
传统的CSI加速器放射治疗计划由于射野范围限制,必须进行计划叠加才能完成CSI患者的治疗,从而在靶区剂量分布上就会产生“剂量冷点”或者“剂量热点”,M-ISO计划由于多个等中心设计,避免了“剂量冷点”和“剂量热点”的产生,但摆位误差不可避免。对多中心计划设计方法得到的治疗计划引入摆位误差(y轴方向±2 mm),重新计算该计划的剂量分布,比较新计划与原计划靶区剂量分布的差异。
4. 统计学处理:计量资料以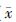 ±s表示,采用SPSS 19.0软件进行统计学分析,两种计划剂量学参数的比较采用配对t检验。P<0.05为差异有统计学意义。
±s表示,采用SPSS 19.0软件进行统计学分析,两种计划剂量学参数的比较采用配对t检验。P<0.05为差异有统计学意义。
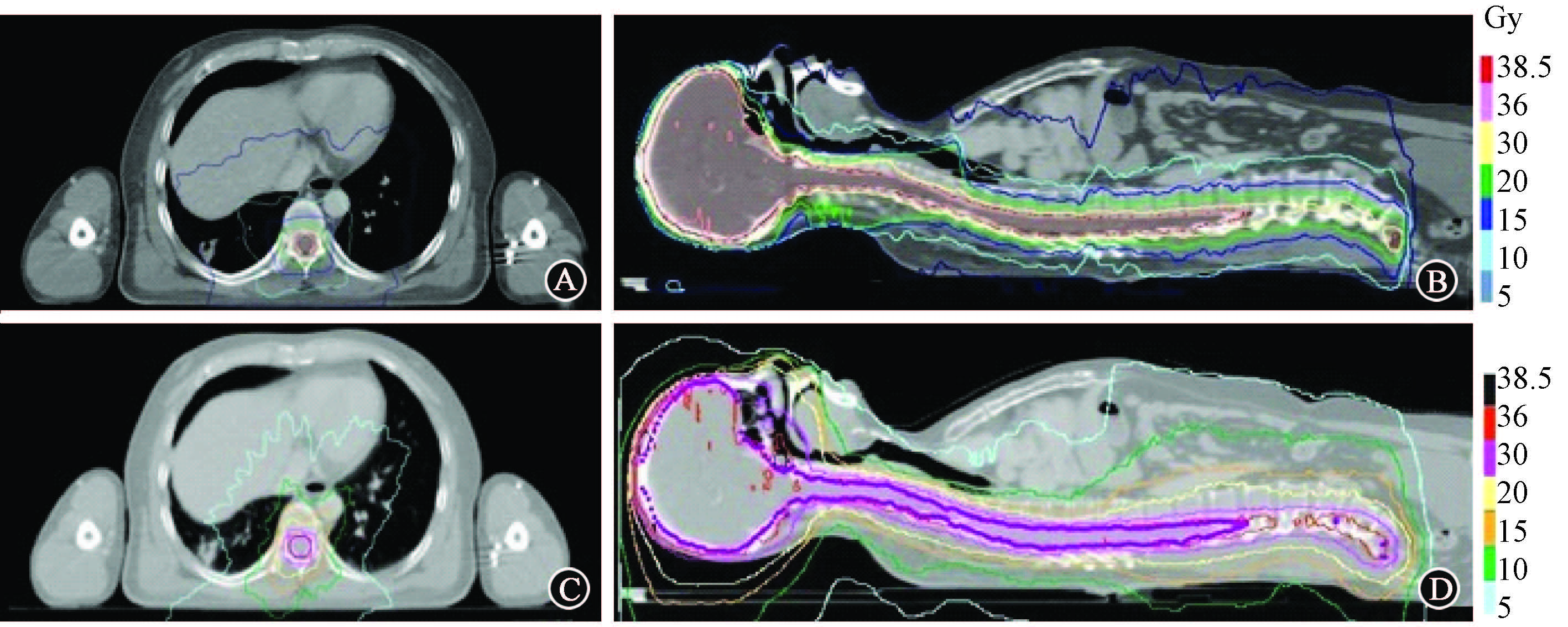
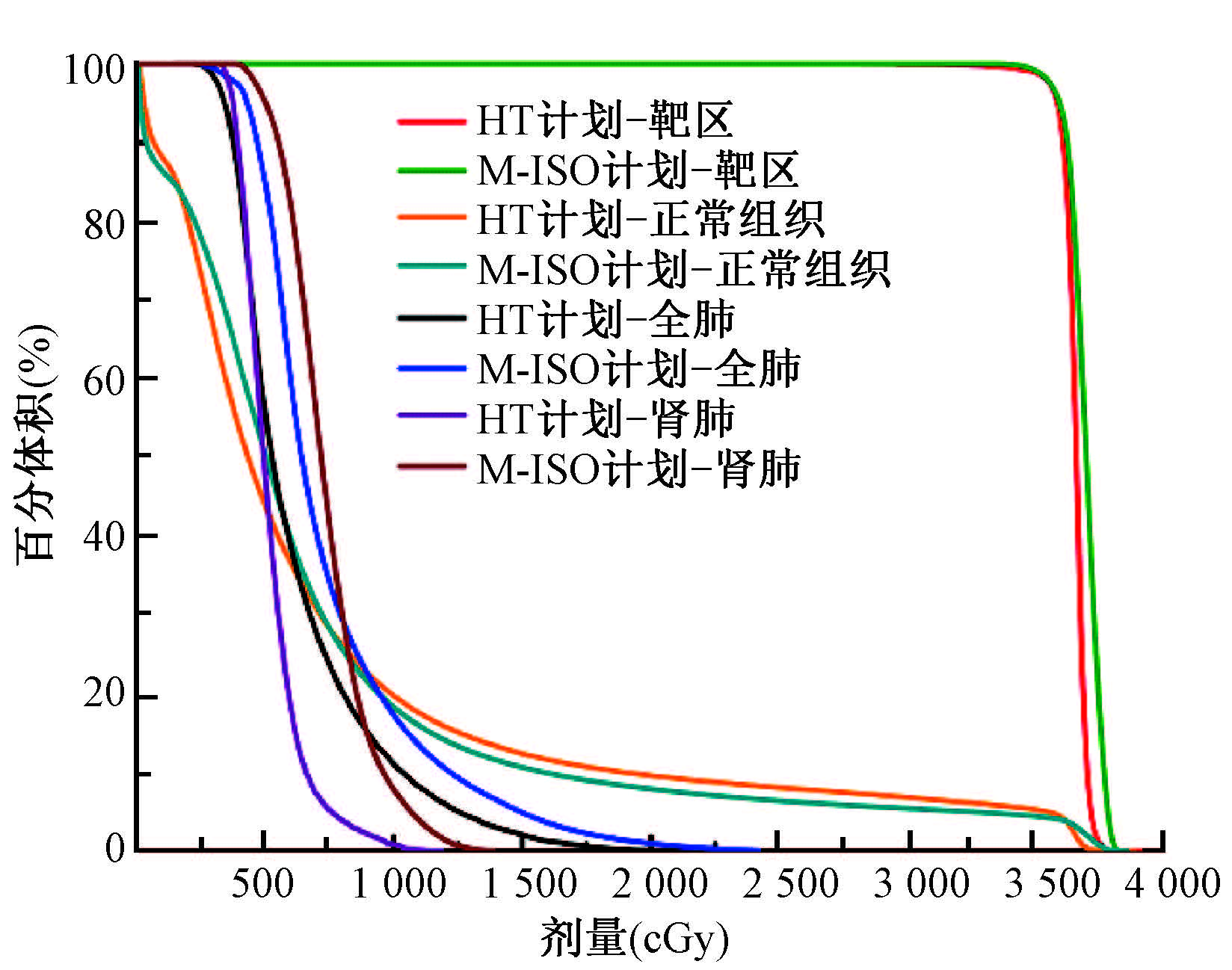
1. 靶区剂量分布及DVH图:从等剂量曲线分布图(图1)和剂量体积直方图(图2)中可以看到,两种计划靶区剂量均满足临床处方要求,M-ISO计划的低剂量区域(5 Gy覆盖范围)大于HT组计划,HT组剂量梯度更加陡峭。
|
图1 CSI患者两种计划CT图像示例的等剂量分布 A、B分别为M-ISO计划横截面、矢状面;C、D分别为HT计划横截面、矢状面 |
|
图2 CSI患者两种计划靶区和危及器官的剂量体积直方图 注:HT.螺旋断层放射治疗;M-ISO.多中心计划设计方法 |
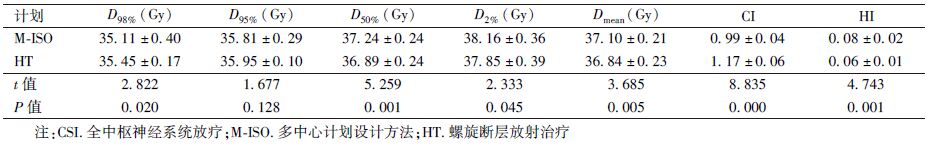
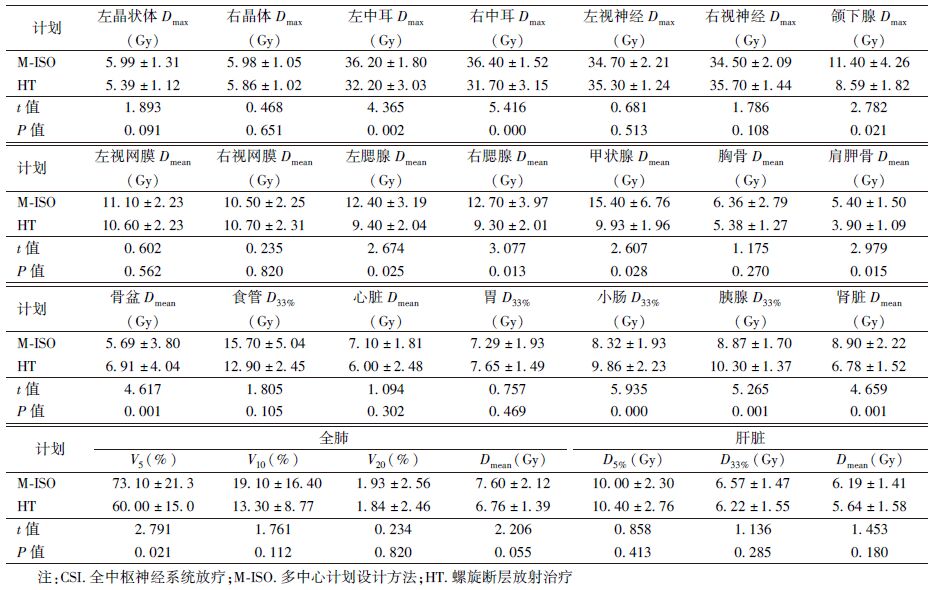
2. 靶区(PTV)和危及器官剂量学参数比较:结果列于表1,表2。两种计划方法PTV的D95%差异无统计学意义,D98%、D2%和HI参数HT组的结果优于M-ISO组优于HT组(t=5.259、3.685、8.835,P<0.05);HT组计划对于左右中耳、左右腮腺、颌下腺、甲状腺和肾脏等危及器官的保护优于M-ISO组(t=4.365、5.416、2.674、3.077、2.782、2.607、4.659,P<0.05),而M-ISO组胰腺和小肠等器官的受照剂量优于HT组(t=5.265、5.935,P<0.05)。
表1 10例CSI患者两种计划靶区(PTV)剂量体积参数(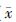 ±s) ±s)
|
表2 10例CSI患者两种计划危及器官的剂量体积参数(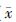 ±s) ±s)
|
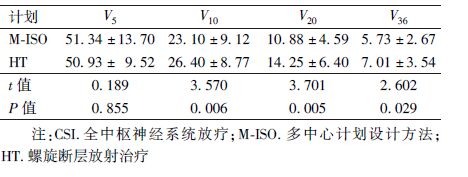
3. 正常组织剂量学参数比较:正常组织(皮肤体积减去靶区体积)M-ISO组计划的V10、V20和V36均低于HT组(t=3.57、3.701、2.602,P<0.05),两组数据V5差异无统计学意义(表3)。
表3 10例CSI患者两种计划正常组织的剂量
体积参数(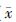 ±s) ±s)
|
4. 治疗时间及机器跳数的比较:10例患者靶区长度平均为68.43 cm。M-ISO组计划的平均治疗时间(10.43 min)较HT组(17.57 min)缩短7.2 min(41.0%),平均机器跳数(885.1 MU)较HT组(15 088.1 MU)减少14 203 MUs(94.1%),差异均具有统计学意义(t=8.477、19.313,P<0.05)。
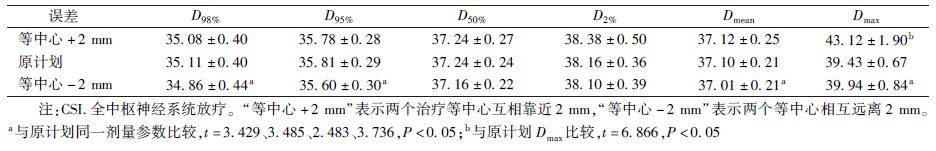
5. 摆位误差造成CSI计划靶区剂量与原计划的差异:以图像引导放疗技术为前提,摆位误差可以控制在2 mm范围以内,故本研究选取2 mm作为摆位误差的值。当等中心相互靠近2 mm时,靶区剂量参数与原计划相比,除Dmax(t=6.866,P<0.05)以外,差异均无统计学意义;当等中相互心远离2 mm时,靶区剂量参数D98%、D95%、Dmean和Dmax与原计划相比,均有明显变化(t=3.429、3.485、2.483、3.736,P<0.05,表4)。
表4 10例患者摆位误差造成CSI计划靶区(PTV)剂量参数的变化(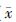 ±s) ±s)
|
随着放疗技术的发展,全中枢的放射治疗技术从最初的二维(2D)放射治疗技术发展到三维适形(3D-CRT)放疗技术、调强放疗技术,直到现在的螺旋断层放疗技术[1]。前3种技术面临的共同难题在于靶区剂量均匀性、靶区内由于射野衔接造成的剂量冷点和热点难以解决,HT技术的出现,解决了上述难题。国内外多项研究表明,HT技术在CSI放射治疗上的优势——消除了接野造成的冷点和热点,剂量分布均匀性好,且能显著减少正常组织受量[2, 3, 4, 5, 6]。本研究中,多等中心计划设计方法与常规的2D、3D以及IMRT技术不同,后三者不能避免多个治疗计划剂量叠加、靶区内剂量冷、热点等问题,而M-ISO方法本质上是将多个治疗计划融合到一个逆向调强放疗计划中,从而可以有效地控制靶区内剂量的均匀性以及冷、热点等问题。
本研究结果显示,M-ISO组计划靶区剂量满足临床要求,完全解决了靶区内剂量冷、热点和剂量分布不均的难题,靶区内剂量分布和HT组相比各有优势;在危及器官的剂量学分析中,HT组计划对于中耳、腮腺、下颌腺、甲状腺和肾脏等的保护优于M-ISO组,而M-ISO组胰腺和小肠等器官的受照剂量优于HT组。值得指出的是,CSI患者照射的总剂量为36 Gy,各个危及器官的受照剂量都很低,均在耐受剂量范围以内。在治疗出束时间和机器跳数这两项参数中,M-ISO组计划明显优于HT组,M-ISO组计划治疗时间减少41%,与Sharma等[5]研究得出的结论一致。治疗时间对于CSI患者是很重要的一项参数,特别是儿童和重病患者,在照射过程中长时间保持体位较为困难;M-ISO组计划机器跳数减少94.1%,减少了加速器的损耗。
在治疗计划执行过程中,摆位误差是不可避免的,图像引导放射治疗(IGRT)技术可以减小摆位误差。为了检验M-ISO组计划在摆位误差存在的情况下是否会产生剂量冷、热点,本研究模拟在IGRT技术的前提下执行计划,假设在y轴上的摆位误差达到2 mm,结果显示,靶区(PTV)剂量D95%、D50%和D2%与原计划相比,差异均无统计学意义,D98%、Dmean和Dmax存在差异,但均在临床可接受范围,与Myers等[15]的研究结果一致。
CSI患者照射范围较广,受到低剂量辐射的范围随之扩大,本研究结果显示,M-ISO和HT组正常组织受照剂量V5差异无统计学意义,V10、V20和V36差异有统计学意义,表明HT组辐射范围较M-ISO组明显增大,该结论与Penagaricano等[16]研究结果一致。HT组引起全身积分剂量有一定的增加,是否会对正常组织产生放射性损伤或引发第二肿瘤,还需进一步临床观察[17]。
M-ISO是一种全新的计划设计理念,与HT相比,有其独特的优势,该方法可以在各类普通常规加速器上进行运用实施,没有设备类型限制;该方法不仅仅适用于CSI患者,对于肿瘤范围超越射野范围的所有病例都可以用M-ISO进行放疗计划设计。本研究中采用的M-ISO方法可以进行一些变换处理,比如将全弧形照射变换为射野或者半弧形照射等,此研究将作为下一步的研究重点。总之,M-ISO技术作为一种全新的计划设计理念值得在CSI病例甚至更多的临床病种上进行推广。
| [1] | 杨美玲,黎静. 全中枢放射治疗的进展[J]. 医学综述,2014,20(2):276-279. |
| [2] | 杨美玲,黎静,李志强,等. 螺旋断层放疗与常规放疗在全脑全脊髓照射中的剂量学比较[J]. 临床肿瘤学杂志,2014,19(8):718-722. |
| [3] | Myers P, Stathakis S, Gutiérrez AN, et al. Dosimetric comparison of craniospinal axis irradiation (CSI) treatments using helical tomotherapy, SmartarcTM, and 3D conventional radiation therapy[J]. Int J Med Phys Clin Eng Radiat Oncol, 2013,(2):30-38. |
| [4] | 文婷, 李志强, 张晋建,等. 改进全脑全脊髓螺旋断层放射治疗计划的研究[J]. 中国医学物理学杂志,2012,29(6):3737-3741. |
| [5] | Sharma DS, Gupta T, Jalali R, et al. High-precision radiotherapy for craniospinal irradiation: evaluation of three- dimensional conformal radiotherapy, intensity-modulated radiation therapy and helical tomotherapy[J]. Br J Radiol, 2009,82(984): 1000-1009. |
| [6] | Qu B, Du L, Huang Y, et al. Clinical analysis of intracranial germinoma's craniospinal irradiation using helical tomotherapy[J]. Chin J Cancer Res, 2014, 26(3):247-254. |
| [7] | Myers PA, Mavroidis P, Papanikolaou N, et al. Comparing conformal, arc radiotherapy and helical tomotherapy in craniospinal irradiation planning[J]. J Appl Clin Med Phys, 2014, 15(5):12-28. |
| [8] | 傅玉川,李光俊,林大全,等. 通过多种技术方法的综合使用优化全脑全脊髓照射技术[J].生物医学工程学杂志,2010,27(1):193-197. |
| [9] | Lee YK, Brooks CJ, Bedford JL, et al. Development and evaluation of multiple isocentric volumetric modulated arc therapy technique for craniospinal axis radiotherapy planning[J]. Int J Radiat Oncol Biol Phys, 2012, 82(2):1006-1012. |
| [10] | 谢秋英,石锦平,祁振宇,等. 全中枢神经系统射野衔接方法研究[J]. 中华肿瘤防治杂志,2013,20(25):1190-1193. |
| [11] | 于甬华,罗立明,田世禹,等. 2100-C加速器全中枢神经系统照射方法研究[J]. 山东生物医学工程,2001,20(2):9-12. |
| [12] | 刘志杰, 朱小东, 杨海明,等. 不同全脑全脊髓放疗方式的剂量学比较及摆位误差对靶区的影响[J]. 中华放射医学与防护杂志,2014,34(7):526-529. |
| [13] | 谢秋英, 石锦平, 张利文,等. 全中枢神经系统调强放疗技术的应用[J]. 实用癌症杂志,2014,29(6):712-715. |
| [14] | Hodapp N. The ICRU Report 83: prescribing, recording and reporting photon-beam intensity-modulated radiation therapy (IMRT)[R]. Strahlenther Onkol, 2012, 188(1):97-99. |
| [15] | Myers P, Stathakis S, Mavroidis P, et al. Evaluation of localization errors for craniospinal axis irradiation delivery using volume modulated arc therapy and proposal of a technique to minimize such errors[J]. Radiother Oncol, 2013,108(1):107-113. |
| [16] | Penagaricano J, Moros E, Corry P, et al. Pediatric craniospinal axis Irradiation with helical tomotherapy: patient outcome and lack of acute pulmonary toxicity[J]. Int J Radiat Oncol Biol Phys, 2009, 75(4):1155-1161. |
| [17] | Parker W, Filion E, Roberge D, et al. Intensity-modulated radiotherapy for craniospinal irradiation: Target volume considerations, dose donstrains, and competing risk[J]. Int J Radiat Oncol Biol Phys, 2007, 69(1) :251-257. |
 2015, Vol. 35
2015, Vol. 35